Чем заменить фамвир для кошек
Опубликовано: 14.05.2024
Автор: Ильченко Е. И., Ильченко А. А., Московская обл., г. Сергиев Посад, Ветконсультация; Ожерелков С. В., г. Москва, Институт полиомиелита и вирусных энцефалитов им. М. П. Чумакова

Вирусные заболевания в Московской области очень распространены — владельцы прививают кошек гораздо реже, чем собак. Поэтому проблема лечения вирусных инфекций кошек актуальна.
Почти 90% всех респираторных инфекций у кошек вызывают вирусы, относящиеся к двум семействам: ДНК-содержащих герпесвирусов и РНК-содержащих калицивирусов. Герпесвирусы вызывают инфекционный ринотрахеит (ИРТ), а калицивирусы — калицивироз. Из кишечных вирусных инфекций наиболее часто выявляется панлейкопения.
Диагноз ставили на основании клинических признаков. Для ИРТ это сухой кашель, слизистые или гнойные выделения из носа, конъюнктивит, вялость, потеря аппетита, часто повышенная температура. При калицивирозе к перечисленным симптомам добавляются язвенные поражения в полости рта и обильное слюнотечение. При панлейкопении наиболее распространенными симптомами являются рвота, понос, сильная болезненность живота, сначала повышение температуры до 40,5 ºС, а затем снижение до 36 – 35 ºС с быстро нарастающей дегидратацией.
Учитывая большую распространенность этих инфекций, мы столкнулись с проблемой выбора оптимальной схемы терапии.
Это конечно симптоматическая терапия. При респираторных инфекциях — антибиотики группы пенициллина — амоксициллин (кламоксил), ампициллин (альбипен) и пенициллин (бициллин 3 и неопен). Отхаркивающие средства, санация полости рта при калицивирозе, введение растворов глюкозы, витаминов и микроэлементов истощенным животным. При панлейкопении — антибиотики, к которым чувствительна грамотрицательная микрофлора кишечника — гентамицин, неопен (неомицин). Введение солевых растворов: 0,9% NaCl, р-р Рингера, р-р 5%-ной глюкозы. Мы также в обязательном порядке используем атропин, дроперидол, но-шпу, сульфокамфокаин, в тяжелых случаях — преднизолон.
Основным для лечения вирусных заболеваний, особенно респираторных, является этиотропная терапия. Мы испробовали много препаратов — камедон, анандин, витафел, кинорон, фоспренил, но в итоге остановились на максидине. Максидин апробирован более чем на 50 кошках: 23 с ИРТ, 19 с калицивирозом и 12 с панлейкопенией. Использовали следующую схему лечения: по 0,5 мл 2 раза в день, подкожно в течение 5 дней. Поскольку препарат болезненный, котятам его вводили с 0.5% новокаином. Возраст животных колебался от 1 месяца до 14 лет. С диагнозом ИРТ все животные выздоровели. Обычно улучшение наступало на 3-й день после начала лечения. Лишь у 3 животных болезнь приобрела хроническое течение, и они выздоровели на 12 – 14-й день.
При калицивирозе улучшение также наступало на 2 – 3-й день, кошки быстро выздоравливали, лишь одна пала — в результате длительного голодания и сильной дегидратации наступили необратимые изменения в организме. С панлейкопенией картина несколько иная. Из 12 пациентов пали 4, что составляет 33%. Причем некоторых из них лечить начали с самого начала заболевания. Причину столь высокой смертности мы обсудим ниже. Почему же мы выбрали максидин в качестве основного средства этиотропной терапии при вирусных заболеваниях кошек?
Максидин это новый металлоорганический иммуностимулятор, разработанный фирмой «Микро-плюс». В экспериментах на базе кафедры ветеринарной вирусологии Ветакадемии им. К. И. Скрябина было показано, что максидин обладает выраженным противовирусным эффектом в отношении вируса герпеса 1-го типа — возбудителя ИРТ (данный эффект был показан на чувствительной к вирусу линии клеток Таурус-1; при добавлении препарата, титры вируса снижались более чем в 100 раз по сравнению с контролем). Кроме того, в опытах на мышах была показана выраженная протективная активность максидина при экспериментальном клещевом энцефалите (при однократном введении препарата одновременно с летальной дозой вируса более 50% животных выживало, тогда как в контрольной, не обработанной препаратом группе, летальность составила 100%. Также в опытах на мышах было показано, что максидин является индуктором общего сывороточного интерферона (ИФН): высокие титры ИФН обнаруживали в сыворотке крови через 5, 24, 48, 72 часа после введения препарата.

С другой стороны, экспериментальные исследования показали, что максидин не обладает прямым противовирусным действием в отношении аденовирусов. Эти вирусы не содержат внешней оболочки. Возможно, что маловыраженный эффект препарата при панлейкопении, вызываемой парвовирусами, также не содержащими оболочки, связан с тем, что максидин не обладает прямым противовирусным действием в отношении безоболочечных вирусов.
В настоящее время механизмы иммуномодулирующего действия максидина находятся в стадии изучения, поэтому схема его применения как иммуномодулятора уточняется.
Вывод: максидин может быть рекомендован для включения в схему комплексной терапии при калицивирозе и ИРТ у кошек в качестве основного средства этиотропной терапии.
Материалы конференции г. Ставрополь, 1999 г .
Конъюнктивиты у кошек / Conjunctivitis in cats
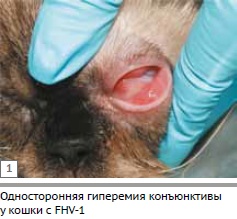
Еще фото
Автор (ы): Л.А. Соломахина, Главный врач, врач-офтальмолог Воронежского ветеринарного комплекса «Кот м@троскин», член RSVO и ESVO / L. Solomakhina, Chief doctor, DVM, Ophthalmologist, Voronezh Veterinary complex «Cat m@troskyn», member of the RSVO and of the ESVO
Журнал: №2 - 2016
Ключевые слова: конъюнктивиты, кошки
Key words: conjunctivitis, cats
Условные обозначения: FHV-1 – Герпесвирусная инфекция кошек 1-го типа
Микоплазма прежде была описана как причина конъюнктивитов у кошек. тем не менее, примерно 90% нормальных кошек являются носителями этих микроорганизмов, и их клиническое значение в качестве причины кошачьих конъюнктивитов является спорным. аналогично, значение Mycoplasma spp. в инфекционном кератоконъюнктивите овец и крупного рогатого скота, а также во многих инфекционных конъюнктивитах других видов животных вызывает сомнения или не определено. Вероятно, культура Mycoplasma spp. в ослабленных глазах дает чрезмерно быстрый рост флоры.
Mycoplasma spp. have formerly been described as a cause of conjunctivitis in cats. However, approximately 90% of normal cats harbor the organisms, and their clinical significance as a cause of feline conjunctivitis is debatable. Likewise, the importance of Mycoplasma spp. in infectious ovine and bovine keratoconjunctivitis and in many infectious conjunctivitides in other animals is questionable or undetermined. It is possible that culture of Mycoplasma spp. from debilitated eyes represents only an overgrowth of flora.
Конъюнктивит – воспаление конъюнктивы – возникает в ответ на повреждение. Поврежденная конъюнктива может реагировать развитием гиперемии (покраснения) (рис. 1, 9), отеком (хемозом) (рис. 2, 8), выделениями (рис. 3–7), образованием фолликулов (особенно распространено при хламидиозе кошек) (рис. 10.1–10.3).
Дифференциальная диагностика конъюнктивитов
Конъюнктивит следует рассматривать как потенциальный признак множества различных, часто приводящих к слепоте заболеваний и иногда как признак системного и потенциально угрожающего жизни заболевания. Дифференциальная диагностика данных состояний, а также дифференциальная диагностика конъюнктивальной и эписклеральной гиперемии были подробно изложены в статье предыдущего номера «Конъюнктивиты у собак».
Причины конъюнктивита у кошек
Наиболее частая этиология конъюнктивита у кошек (в отличие от собак) – инфекционная.
К основным патогенам, которые вызывают инфекционные конъюнктивиты у кошек, относятся герпес-вирусная инфекция кошек 1-го типа (FHV-1) и хламидиоз кошек. Как уже было сказано ранее, роль микоплазм как первичного патогена, вызывающего конъюнктивиты кошек, спорна. Микоплазмоз можно отнести к оппортунистической инфекции (заболевание, возникающее из-за снижения иммунитета и общей резистентности организма).
Герпесвирусная инфекция кошек 1-го типа (FHV-1)
Наиболее частый патоген, вызывающий конъюнктивиты у кошек. Кроме того, это единственный вирус, который вызывает поражение роговицы у данного вида (рис. 11, 14). FHV-1 является типичным альфа-вирусом, который реплицируется в эпителиальных тканях во время первичной инфекции и далее находится в латентном состоянии в тройничном ганглии. Под действием стрессовой ситуации происходят реактивация латентного вируса и распространение его вдоль сенсорных аксонов с обострением заболевания.
Первичная инфекция
Наблюдается в основном у новорожденных котят – неонатальная офтальмия (поражение вирусом до открытия век, обычно со скоплением большого количества воспалительного органического вещества в конъюнктивальном мешке) и молодых кошек (рис. 12, 13).
После первичного внедрения в слизистую рта, носа или конъюнктивы следует начальный период быстрой репликации внутри и сопутствующий цитолиз эпителиальных клеток на этих участках. Это иногда может наблюдаться прямо на роговице в виде патогномоничных ветвистых язв (при детальном осмотре роговицы при помощи лиссаминового зеленого или бенгальского розового красителя можно выявить микродендритные нарушения роговичного эпителия) (рис. 14). Эта фаза разрушения клеток вызывает ринит и конъюнктивит. Если цитолиз достаточно сильный, могут наблюдаться серозно-кровянистые глазные или носовые выделения (рис. 15). Кроме того, в качестве осложнения данного состояния часто развивается спаечный процесс в носослезном канале, который проявляется в синдроме слезостояния и отсутствии или замедленном прохождении флюоресцеинового красителя в нос (тест Джонса 1) (рис. 27, 28.1–28.2). На рис. 29 показан нормальный выход флюоресцеинового красителя из двух ноздрей. Выделение собственного вещества конъюнктивы и стромы роговицы позволяет сформироваться симблефарону (это слипание любой части конъюнктивы с самой собой или с роговицей) (рис. 16.1–16.4). Симблефарон чаще всего развивается у молодых кошек и возникает после тяжелого воспаления конъюнктивы практически с полной потерей эпителиальных клеток при FHV-1.
Первичная FHV-1 характеризуется двусторонним конъюнктивитом и симптомами инфекции верхних дыхательных путей. По мере прогрессирования заболевания первоначальные серозные выделения становятся гнойными, а конъюнктива сильно гиперемированной и отекшей (хемозированной). При FHV-1 преобладает гиперемия конъюнктивы, а при хламидиозе – хемоз.
Дифференциальная диагностика FHV-1 и хламидиоза представлена в табл. 1.
Рецидивирующая инфекция
Клинические признаки рецидивирующей инфекции FHV-1 могут быть различными. Если сравнивать данное состояние с первичной инфекцией, поражение дыхательных путей обычно отсутствует, а вовлечение глаз может быть как одно-, так и двусторонним. Наиболее частым проявлением рецидива инфекции является хронический и/или рецидивирующий конъюнктивит с незначительным блефароспазмом и персистирующие выделения из конъюнктивального мешка.
Кроме того, при FHV-1 может наблюдаться поражение кожи век, спинки носа и носового зеркальца (рис. 26.1–26.2).
Хламидийный конъюнктивит кошек
Члены семейства Chlamydiaceae прошли реклассификацию и поменяли названия в результате использования новых молекулярно-биологических методик (табл. 2). Однако число вызываемых ими болезней осталось, в основном, неизменным. Хламидии вызывают выраженный конъюнктивит у кошек, птиц и мелких жвачных животных. Вероятность зооноза существует, особенно от птиц, от других видов животных она мала.
Clamidofila psittaci (felis) – внутриклеточные грамотрицательные бактерии. Заболеванию подвержены кошки любых возрастов. В первую очередь возбудитель поражает конъюнктиву (персистирующие конъюнктивиты), редко возникает респираторная инфекция. В отличие от FHV-1, роговица не вовлечена. У кошек хламидийный конъюнктивит изначально может быть односторонним, но, как правило, распространяется на другой глаз в течение 7 дней с начала первичного инфицирования (рис. 17.1–17.3). Легкий ринит, незначительное повышение температуры и увеличение подчелюстных лимфатических узлов обычно сопутствуют глазным симптомам в начале болезни, но часто проходят полностью и быстрее, чем конъюнктивальные признаки, которые могут длиться довольно долго. Хемоз является преобладающей чертой. С течением болезни может проявиться мембранный или фолликулярный конъюнктивит (рис. 10.1–10.3). Болезнь без лечения может длиться месяцами, и пациент получает статус носителя на длительное время (присутствует также носительство в желудочно-кишечном тракте и гениталиях).
Основной дифференциальный диагноз – герпетический конъюнктивит, вызываемый FHV-1. Часто хламидиоз и FHV-1 протекают совместно (рис. 18.1, 18.2, 18.3). Если говорить про дифференциальную диагностику этих двух заболеваний, то зачастую диагноз ставится на основании данных осмотра и клинических признаков, так как результаты лабораторных исследований могут быть как ложноположительными, так и ложноотрицательными. Особенно это касается герпесвирусной инфекции кошек. Выявить первичную инфекцию FHV-1 не составляет труда. Основная проблема заключается в выявлении латентного FHV-1 (в этом случае результаты ПЦР-тестирования могут быть ложноотрицательными, что не говорит об отсутствии FHV-1). Важным для интерпретации результатов диагностического теста на герпес и ведения кошек, зараженных этим организмом, является знание, что герпес дает статус постоянного латентного носителя у большинства инфицированных кошек. Кроме того, герпес повсеместно распространен во всем мире. Серологические исследования дают предположение, что по крайней мере 95% кошек подверглись воздействию вируса.
При хламидиозе преобладает хемоз, а при FHV-1 – гиперемия конъюнктивы. При хламидиозе тест Ширмера обычно в норме или его значения повышены, а при FHV-1 – в норме или его значения снижены. При окраске роговицы лиссаминовым зеленым или бенгальским розовым окрашивание будет отрицательно в случае хламидиоза кошек и может быть положительно в случае FHV-1 (характерное древовидное окрашивание) (рис. 14). При FHV-1 более выражены симптомы общего недомогания и респираторные симптомы (чихание, выделения из носа и т.д.) по сравнению с хламидиозом кошек. Кроме того, клеточные реакции, связанные с FHV-1 и хламидиозом кошек, подробно описаны в табл. 3.
При калицивирусной инфекции кошек иногда может возникать конъюнктивит, но клинические признаки поражения конъюнктивы незначительные, преобладают респираторные симптомы с поражением ротовой полости (см. табл. 1, рис. 19). Экспериментальные исследования показали незначительную патогенность этого вируса для конъюнктивы кошек.
Гораздо реже у кошек (в отличие от собак) встречаются неинфекционные причины, которые вызывают конъюнктивит (табл. 4).
Общие положения лечения конъюнктивита у кошек
Как уже было отмечено ранее, конъюнктивиты у кошек чаще всего являются инфекционными (FHV-1 и хламидиоз кошек). Поэтому мы остановимся на терапии именно этих состояний.
Лечение хламидиоза кошек
Согласно последней информации, кошки могут «изолировать» Chlamydophila в неглазных локациях. Это открытие, вместе с контролируемыми исследованиями по сравнению местной и системной терапии, привело к рекомендации, что системные антибиотики (обычно доксициклин 10 мг/кг в день ориентировочно 30 дней) должны использоваться вместе или вместо местных офтальмологических мазей (тетрациклиновая 1% глазная мазь/эритромициновая глазная мазь/хлортетрациклиновая глазная мазь). Азитромицин изначально уменьшает клинические признаки и выделение C. felis у экспериментально инфицированных кошек, но имеет временное и менее эффективное воздействие, чем доксициклин. Эффективность хламидийных вакцин трудно установить из-за расходящихся результатов. В большинстве последних экспериментальных исследований использование живой вакцины уменьшает тяжесть глазной болезни, но не имеет никакого влияния на выделение организмов или их способность инфицировать и проявляться в других системах (желудочно-кишечной, мочеполовой).
Лечение герпесвирусной инфекции 1-го типа у кошек
Противовирусная терапия. Противовирусные препараты местного действия
Не было разработано ни одного ветеринарного противовирусного препарата. Однако на животных были опробованы различные противовирусные препараты, разработанные для людей.
Безопасность редко принимается во внимание при назначении местного медикамента, но обычно важна для системно назначаемого противовирусного средства. Эффективность всегда принимается во внимание, независимо от способа назначения. Главные исследования в ветеринарной медицине включали безопасность этих средств у кошек и их эффективность против герпеса. Эта тенденция редко ограничивает местное назначение этих препаратов, но существенно ограничивает их системное использование.
Препаратами выбора в лечении инфекции глаз FHV-1 являются идоксуридин (Герплекс, Allegran), видарабин (Вира-А, Parke-Davis) или трифтортимидин (Вироптик, Glaxo Wellcome). Данные препараты являются виростатиками, поэтому их необходимо применять животным не менее 5 раз в день, особенно на ранних стадиях заболевания. В некоторых случаях рекомендуется ежечасное применение данных препаратов в течение по крайней мере 24 часов терапии у людей. Лечение необходимо продолжать как минимум 1 неделю после устранения глазных повреждений, которое обычно происходит в течение 2–3 недель.
Каждый из этих препаратов действует как конкурирующий нуклеозидный аналог или ингибитор ДНК-полимеразы. По данным исследования in vitro, Вироптик является самым эффективным из вышеперечисленных препаратов, но, к сожалению, этот препарат имеет высокую стоимость и обладает раздражающим действием на конъюнктиву кошек. Поэтому рекомендуется начинать терапию с идоксуридина (по 1 капле 5 раз в день) и далее, при отсутствии положительной динамики, в течение недели переходить на Вироптик.
Системные противовирусные препараты
Так как вирусы заставляют клетки хозяина продуцировать их ДНК и белки, трудно найти противовирусные препараты, не нарушающие функции клеток хозяина, но нарушающие вирусный синтез.
Ацикловир (Зовиракс, Glaxo Wellcome) стал прорывом в противогерпесвирусной терапии у людей.
Ацикловир является ациклическим нуклеотидом, который должен фосфорилироваться, чтобы проявились его антивирусные свойства. Так как для фосфорилирования ацикловира нужен фермент тимидинкиназа, который продуцирует герпесвирус, этот препарат оказывается нетоксичным для неинфицированных клеток. Поэтому ацикловир широко применяется для лечения герпесвирусной инфекции у людей. К сожалению, герпесвирусная инфекция кошек 1-го типа менее чувствительна к ацикловиру, чем другие герпесвирусы. И самое важное – трудно создать нужную концентрацию препарата в крови кошек даже после введения больших доз. Кроме того, ацикловир вызывает угнетение костного мозга с лейкопенией и анемией. Именно поэтому ацикловир обычно не используется для лечения кошек. Есть данные о применении ацикловира кошкам в начальной дозе 30–40 мг/кг внутрь 2 раза в день ориентировочно 3 недели с еженедельным анализом крови для мониторинга уровня лейкоцитов, но такое лечение можно применять только при отсутствии эффективности других видов терапии и информировании владельца об огромных рисках такого лечения. Препаратами выбора для системной противовирусной терапии кошек являются Cidofovir (Vistide) и Penciclovir/Famciclovir (Famvir).
Cidofovir (Vistide) представляет собой раствор для внутривенного введения, который применяется в дозе 5 мг/кг в виде часовой инфузии 1 раз в неделю 2 недели подряд.
Famciclovir (Famvir) представляет собой таблетированную форму по 125, 250 и 500 мг. По разным источникам, применяются дозы этого препарата от 40 до 90 мг/кг 3 раза в день ориентировочно 21 день. Более высокие дозы Фамвира рекомендовались ранее. На данный момент в большинстве случаев рекомендуется доза 40 мг/кг 3 раза в день 21 день, и, по некоторым данным, применяются даже гораздо меньшие дозы. Данный препарат является наиболее безопасным для кошек.
Иммунотерапия
Интерфероны
Клиническая эффективность интерферонов в лечении FHV-1 спорна. Считается, что лечение интерферонами эффективно, только если оно начато до заражения вирусом. Тем не менее, многие врачи используют эту группу препаратов для терапии кошек с FHV-1.
Рекомбинантный человеческий альфа-интерферон применяется в среднем в минимальной пероральной дозе 25 единиц. Есть исследования, которые выявили, что данная доза способна частично минимизировать клинические симптомы инфекции FHV-1, даже если ее назначали после заражения. Для кошек считается предпочтительным использование кошачьих интерферонов: Virbagen Omega (Virbac) или Фелиферон, так как к «чужим» видовым интерферонам у кошек возникает быстрое привыкание – выработка антител, подобно реакции на вирус.
Вакцинация снижает тяжесть заболевания при последующем заражении FHV-1, но не предотвращает инфекцию и переход вируса в латентное состояние.
Лечение L-лизином
Репликация FHV-1 сильно зависит от аминокислоты аргинина. В культурах тканей высокая концентрация лизина конкурентно подавляет соединение аргинина внутри вируса, что приводит к подавлению вирусной репликации. Применение L-лизина, как и интерферонов, является спорным, тем не менее, многие врачи используют данный препарат в своей практике. Рекомендуемая доза – 500 мг 2 раза в день курсом от 1 до 3 месяцев.
Если конъюнктивит у кошки все же является неинфекционным, то после выявления и по возможности устранения причины его возникновения (коррекция заворота век/пролапса слезной железы/устранение залома хряща третьего века и т.д.) требуется назначение симптоматической терапии, которая была подробно описана в предыдущем номере.
Есть некоторые нюансы в лечении неинфекционных конъюнктивитов кошек:
• преимущественно используются антибиотики группы фторхинолонов или левомицетиновые глазные капли (то есть препараты, к которым чувствительна хламидия, так как зачастую у таких кошек может наблюдаться сопутствующее заболевание хламидиозом);
• местные кортикостероиды у кошек не должны быть использованы рутинно и применяются четко по показаниям (эозинофильный кератоконъюнктивит кошек, острый аллергический конъюнктивит и т.д.).
Выводы
Диагностика и лечение конъюнктивитов у кошек должны проходить со знанием отличительных моментов от лечения собак.
1. Gelatt K.N. Veterinary Ophthalmology: John Wiley & Sons, 2013.
2. Риис Р.К. офтальмология мелких домашних животных. ООО «Аквариум-принт», 2006.
3. Brooks D.E. Canine conjunctive and nictitating membrane. In: Gelatt K.N., ed. Veterinary Ophthalmology, 2nd ed. Philadelphia: Lea and Febiger, 1991: 290–306.
4. Slatter D. Conjunctiva. In: Slatter D., ed. Fundamentals of Veterinary Ophthalmology, 2nd ed. Philadelphia: WB Sanders, 1990: 204–225.

ФАМВИР 0,25 N21 ТАБЛ П/О Новартис Фармасьютика С.А.

ФАМВИР 0,125 N10 ТАБЛ П/О Новартис Фармасьютика С.А.

ФАМВИР 0,5 N3 ТАБЛ П/О Новартис Фармасьютика С.А.
Фамвир Инструкция по применению
Общее описание
Группа товаров
Производитель
Abbott Nutrition Ltd Новартис Фарма АГ Новартис Фармасьютика С.А.
Страна происхождения
Испания Соединенное королевство
Описание лекарственной формы
10 - блистеры (1) - пачки картонные. 3 - блистеры (1) - пачки картонные. 7 - блистеры (3) - пачки картонные.
Лекарственная форма
Таблетки, покрытые оболочкой белого цвета, круглые, двояковыпуклые, со скошенными краями, с гравировкой "FV" на одной стороне и "125" - на другой. Таблетки, покрытые оболочкой белого цвета, круглые, двояковыпуклые, со скошенными краями, с гравировкой "FV" на одной стороне и "250" - на другой. Таблетки, покрытые оболочкой белого цвета, овальные, двояковыпуклые, со скошенными краями, с гравировкой "FV500" на одной стороне.
Состав
фамцикловир 125 мг Вспомогательные вещества: гидроксипропилцеллюлоза, лактоза безводная, натрия крахмала гликолат, магния стеарат. Состав оболочки: гипромеллоза, титана диоксид, полиэтиленгликоль 4000 (макрогол), полиэтиленгликоль 6000 (макрогол). фамцикловир 250 мг Вспомогательные вещества: гидроксипропилцеллюлоза, лактоза безводная, натрия крахмала гликолат, магния стеарат. Состав оболочки: гипромеллоза, титана диоксид, полиэтиленгликоль 4000 (макрогол), полиэтиленгликоль 6000 (макрогол) фамцикловир 500 мг Вспомогательные вещества: гидроксипропилцеллюлоза, лактоза безводная, натрия крахмала гликолат, магния стеарат. Состав оболочки: гипромеллоза, титана диоксид, полиэтиленгликоль 4000 (макрогол), полиэтиленгликоль 6000 (макрогол).
Описание
Противовирусный препарат. После приема внутрь фамцикловир быстро превращается в пенцикловир, обладающий активностью в отношении вирусов герпеса человека, включая вирус Varicella zoster (вирус опоясывающего герпеса) и Herpes simplex типов 1 и 2 (лабиальный и генитальный вирус простого герпеса), а также вируса Эпштейна-Барр и цитомегаловируса. Пенцикловир попадает в инфицированные вирусом клетки, где под действием вирусной тимидинкиназы быстро превращается в монофосфат, который, в свою очередь, при участии клеточных ферментов переходит в трифосфат. Пенцикловира трифосфат находится в инфицированных вирусами клетках более 12 ч, подавляя в них репликацию вирусной ДНК. Концентрация пенцикловира трифосфата в неинфицированных клетках не превышает минимальную определяемую, поэтому в терапевтических концентрациях пенцикловир не оказывает влияния на неинфицированные клетки. Пенцикловир активен в отношении недавно обнаруженных устойчивых к ацикловиру штаммов вируса Herpes simplex с измененной ДНК-полимеразой. Частота возникновения резистентности к фамцикловиру (пенцикловиру) не превышает 0.3%, у пациентов с нарушенным иммунитетом - 0.19%. Резистентность выявлялась в начале лечения и не развивалась в процессе лечения или после окончания терапии. Было показано, что фамцикловир существенно снижает выраженность и длительность постгерпетической невралгии у пациентов с опоясывающим герпесом. Было показано, что у пациентов с нарушенным иммунитетом вследствие ВИЧ-инфицирования фамцикловир в дозе 500 мг 2 уменьшает число дней выделения вируса простого герпеса (как с клиническими проявлениями, так и без них).
Особые условия
Лечение следует начинать сразу после установления диагноза. Следует соблюдать осторожность при лечении больных с нарушением функции почек, для которых может потребоваться коррекция режима дозирования. Специальных предосторожностей у пожилых пациентов не требуется. Генитальный герпес – заболевание, передающееся половым путем. Во время рецидивов риск заражения увеличивается. При наличии клинических проявлений заболевания, даже в случае начала противовирусного лечения, пациенты должны избегать половых контактов. Во время поддерживающего лечения противовирусными средствами частота распространения вирусной инфекции значительно уменьшается, однако риск передачи инфекции теоретически существует. Поэтому пациентам следует предпринимать соответствующие защитные меры при половых контактах. В состав таблеток препарата 125 мг, 250 мг и 500 мг входит лактоза (26.9 мг, 53.7 мг и 107.4 мг соответственно). Фамвир не следует применять у пациентов с редкими наследственными нарушениями, связанными, с непереносимостью галактозы, тяжелой лактазной недостаточностью или глюкозо-галактозной мальабсорбцией. Переносимые дозы Фамвира и длительность лечения. Фамвир хорошо переносился при лечении инфекции, вызванной вирусом Varicella zoster, при его применении в дозе 750 мг 3 в течение 7 дней; у пациентов с генитальным герпесом при применении препарата в дозе до 750 мг 3 в течение 5 дней и в дозе до 500 мг 3 в течение 10 дней. Было также показано, что препарат хорошо переносился при приеме 250 мг 3 в течение 12 мес для лечения генитального герпеса. Фамвир хорошо переносился у пациентов со сниженным иммунитетом при лечении инфекции, вызванной вирусом Varicella zoster, при приеме 500 мг 3 в течение 10 дней, а также инфекций, вызванных вирусами Herpes simplex, при приеме до 500 мг 2 в течение 7 дней или 500 мг 2 в течение 8 недель. Использование в педиатрии Эффективность и безопасность применения Фамвира у детей не установлена. Таким образом, не рекомендуется применять фамцикловир у детей, за исключением случаев, когда ожидаемая польза лечения оправдывает потенциальный риск, связанный с применением препарата. Влияние на способность к вождению автотранспорта и управлению механизмами Не ожидается влияния Фамвира на способность пациентов управлять автомобилем и другими механизмами, однако пациентам, у которых на фоне применения препарата Фамвир возникает головокружение, сонливость, спутанность сознания или другие нарушения со стороны ЦНС, следует воздержаться от вождения автомашины или управления механизмами в период применения препарата.
Лекарственное взаимодействие
Клинически значимого фармакокинетического взаимодействия фамцикловира с другими препаратами не отмечалось. Не выявлено воздействия фамцикловира на систему цитохрома Р450. Лекарственные препараты, блокирующие канальцевую секрецию, могут повышать концентрацию пенцикловира в плазме. В ходе проведенных клинических исследований не отмечено взаимодействия зидовудина и фамцикловира при их совместном приеме.
Фармокинетика
Всасывание После приема внутрь фамцикловир быстро и почти полностью всасывается и быстро превращается в активный пенцикловир. Биодоступность пенцикловира после перорального приема Фамвира составляет 77%. Cmax пенцикловира после приема внутрь в дозах 125 мг, 250 мг или 500 мг фамцикловира достигается в среднем через 45 мин и составляет 0.8 мкг/мл, 1.6 мкг/мл и 3.3 мкг/мл соответственно. Распределение Фармакокинетические кривые "концентрация -время" совпадают при однократном приеме фамцикловира и при разделении суточной дозы на 2 или 3 приема. Связывание с белками плазмы пенцикловира и его 6-дезокси-предшественника составляет менее 20%. При повторных приемах препарата кумуляции не отмечено. Выведение T1/2 пенцикловира из плазмы в конечной фазе после приема однократной и повторных доз составляет около 2 ч. Фамцикловир выводится в основном в форме пенцикловира и его 6-дезокси-предшественника, которые экскретируются с мочой в неизмененном виде; фамцикловир в моче не обнаруживается.
Показания
— инфекции, вызванные вирусом Varicella zoster (опоясывающий герпес), включая офтальмогерпес и постгерпетическую невралгию; — инфекции, вызванные вирусом Herpes simplex (тип 1 и 2): первичная инфекция, обострение хронической инфекции, супрессия рецидивирующей инфекции (для профилактики обострений); — инфекции, вызванные вирусами Varicella zoster и Herpes simplex (тип 1 и 2) у пациентов со сниженным иммунитетом.
Противопоказания
— повышенная чувствительность к фамцикловиру или любому из компонентов препарата; — повышенная чувствительность к пенцикловиру.
Передозировка
Описанные случаи передозировки (10.5 г) препарата Фамвир не сопровождались клиническими проявлениями.
Побочные действия
В клинических исследованиях показана хорошая переносимость Фамвира, в т.ч. у пациентов со сниженным иммунитетом. Сообщалось о случаях головной боли и тошноты, однако эти явления были слабо или умеренно выражены и отмечались с такой же частотой у пациентов, получавших плацебо. Ниже приведены нежелательные реакции и частота их возникновения на основе данных о спонтанных сообщениях, а также случаев, описанных в литературе, за весь период, в течение которого Фамвир применяется в клинической практике. Нежелательные явления, о которых сообщалось в ходе клинических исследований у больных со сниженным иммунитетом, совпадали с теми, которые отмечались у пациентов с нормальным иммунитетом. Для оценки частоты развития нежелательных реакций использованы следующие критерии: очень часто (> 1/10); часто (от > 1/100, 1/1000, 1/10000,
Категории



Фамвир инструкция по применению
Активное вещество
Название на латинском
Состав, дозировка формы выпуска
Фармакологическое действие
Противовирусное средство. После приема внутрь фамцикловир in vivo быстро превращается в пенцикловир, обладающий in vivo и in vitro активностью в отношении вирусов герпеса человека, включая вирус Varicella zoster и Herpes simplex типов 1 и 2, а также вируса Эпштейна-Барр и цитомегаловируса.
Пенцикловир попадает в инфицированные вирусом клетки, где под действием вирусной тимидинкиназы быстро превращается в монофосфат, который в свою очередь при участии клеточных ферментов переходит в трифосфат. Пенцикловира трифосфат находится в инфицированных вирусами клетках более 12 ч, подавляя в них синтез вирусной ДНК и репликацию вирусов. Период полужизни пенцикловира трифосфата в клетках, пораженных Varicella zoster, Herpes simplex, составляет 9, 10 и 20 ч соответственно. Концентрация пенцикловира трифосфата в неинфицированных клетках не превышает минимальную определяемую, поэтому в терапевтических концентрациях пенцикловир не оказывает влияния на неинфицированные клетки.
Пенцикловир активен в отношении недавно обнаруженных устойчивых к ацикловиру штаммов вируса Herpes simplex с измененной ДНК-полимеразой.
Фамцикловир существенно снижает интенсивность и длительность постгерпетической невралгии у пациентов с опоясывающим герпесом.
В плацебо-контролируемом исследовании у пациентов с иммунодефицитом вследствие ВИЧ-инфицирования было показано, что фамцикловир в дозе 500 мг 2 раза/сут уменьшал число дней выделения вируса Herpes simplex (как с клиническими проявлениями, так и без них).
Показания к применению
- Инфекции, вызванные вирусом Varicella zoster (опоясывающий лишай, включая опоясывающий лишай с глазными осложнениями);
- инфекции, вызванные вирусом Herpes simplex (первичная инфекция, обострение хронической инфекции, супрессия рецидивирующей инфекции).
Противопоказания
Повышенная чувствительность к фамцикловиру и пенцикловиру.
С осторожностью: следует соблюдать осторожность при лечении больных с нарушением функции почек, для которых может потребоваться коррекция режима дозирования.
Специальных предосторожностей у пожилых пациентов и пациентов с нарушениями функции печени не требуется. Опыта применения препарата у больных с тяжелыми (декомпенсированными) нарушениями функции печени нет.
Способ применения и особенности приема
Суточная доза и курс лечения определяется индивидуально в зависимости от показаний, клинического состояния пациента и данных лабораторного обследования.
Особые указания
Лечение следует начинать сразу после установления диагноза.
Генитальный герпес – заболевание, передающееся половым путем. Во время рецидивов риск заражения увеличивается. При наличии клинических проявлений заболевания даже в случае начала противовирусного лечения пациенты должны избегать половых контактов.
Во время супрессивной терапии противовирусными средствами частота распространения вирусной инфекции значительно уменьшается, однако, риск передачи инфекции теоретически существует. Поэтому пациентам следует предпринимать соответствующие защитные меры при половых контактах.
В состав таблеток препарата 125 мг, 250 мг и 500 мг входит лактоза (26.9 мг, 53.7 мг и 107.4 мг соответственно). Фамвир не следует применять у пациентов с редкими наследственными нарушениями, связанными с непереносимостью галактозы, тяжелой лактазной недостаточностью или глюкозо-галактозной мальабсорбцией.
Фамцикловир не оказывает выраженного влияния на спермограмму, морфологию или подвижность сперматозоидов человека. Снижение фертильности было отмечено в экспериментальной модели у крыс мужского пола, получавших фамцикловир в дозе 500 мг/кг массы тела; у крыс женского пола выраженного снижения фертильности не отмечено.
Переносимые дозы Фамвира и длительность лечения. Фамвир хорошо переносился при лечении Herpes Zoster при его применении в дозе до 750 мг 3 раза в сутки в течение 7 дней; у пациентов с генитальным герпесом при его применении в дозе до 750 мг 3 раза в сутки в течение 5 дней и в дозе до 500 мг 3 раза в сутки в течение 10 дней. Было также показано, что препарат хорошо переносился при супрессивной терапии в дозе 250 мг 3 раза в сутки в течение 12 месяцев для лечения генитального герпеса.
Фамвир хорошо переносился у пациентов со сниженным иммунитетом при лечении Varicella zoster при приеме 500 мг 3 раза в сутки в течение 10 дней, а также Herpes Simplex, при приеме до 500 мг 2 раза в сутки в течение 7 дней или 500 мг два раза в сутки в течение 8 недель.
Беременным
Поскольку безопасность фамцикловира при беременности и в период лактации не изучена, применение не рекомендуется, за исключением случаев, когда ожидаемая польза терапии для матери превышает потенциальный риск для плода или грудного ребенка.
Неизвестно, выделяется ли пенцикловир с грудным молоком у человека.
Фамцикловир не оказывает выраженного эффекта на спермограмму, морфологию или подвижность сперматозоидов человека.
В экспериментальных исследованиях не выявлено эмбриотоксического и тератогенного действия фамцикловира и пенцикловира.
Исследования на крысах, получавших фамцикловир внутрь, показали, что пенцикловир выделяется с грудным молоком.
Снижение фертильности было отмечено в экспериментальной модели у крыс мужского пола, получавших фамцикловир в дозе 500 мг/кг массы тела, у крыс женского пола выраженного снижения фертильности не отмечено.
Побочные эффекты
Возможны: слабые и умеренные головные боли, тошнота.
Редко: рвота, головокружение, кожная сыпь; преимущественно у пациентов пожилого возраста - спутанность сознания, галлюцинации.
У пациентов со сниженным иммунитетом: возможны боли в животе, лихорадка; редко – гранулоцитопения и тромбоцитопения.
Совместимость с другими препаратами
Совместное применение с пробенецидом может привести к повышению концентрации пенцикловира в плазме крови. Для предупреждения развития токсических реакций и возможного снижения дозы необходимо осуществлять наблюдение за пациентами, получающими препарат Фамвир в дозе 500 мг одновременно с пробенецидом.
Не отмечалось клинически значимых изменений фармакокинетических параметров пенцикловира при его однократном применении (в дозе 500 мг) сразу поле приема антацидных препаратов (магния или алюминия гидроксид) или у пациентов, получавших до этого лечение (многократный прием) аллопуринолом, циметидином, теофиллином, зидовудином, прометазином. При однократном приеме фамцикловира (в дозе 500 мг) вместе с эмтрицитабином или зидовудином не было выявлено изменений фармакокинетических параметров пенцикловира, зидовудина, метаболита зидовудина (зидовудина глюкуронид) и эмтрицитабина.
При однократном или многократном применении фамцикловира (в дозе 500 мг 3 раза в сутки) вместе с дигоксином не наблюдалось изменений фармакокинетических параметров пенцикловира и дигоксина. Учитывая, что превращение неактивного метаболита 6-дезоксипенцикловира (образующегося при дезацетилирования фамцикловира) в пенцикловир катализируется ферментом алъдегидоксидазой, возможно развитие лекарственного взаимодействия при применении препарата Фамвир вместе с препаратами, метаболизирующимися при участии данного фермента или ингибирующими его активность. При применении фамцикловира вместе с циметидином и прометазином, являющимися ингибиторами альдегидоксидазы in vitro, не было выявлено снижения образования пенцикловира из фамцикловира. Однако при приеме фамцикловира вместе с мощным ингибитором альдегидоксидазы in vitro, ралоксифеном, возможно снижение образования пенцикловира из фамцикловира, и как следствие, эффективности фамцикловира. Необходимо оценивать клиническую эффективность противовирусной терапии при одновременном применении с ралоксифеном.
Учитывая, что фамцикловир является слабым ингибитором альдегидоксидазы in vitro, возможно его влияние на фармакокинетические параметры препаратов, метаболизирующихся при участии данного фермента.
В экспериментальных исследованиях фамцикловир не оказывал индуцирующего влияния на систему цитохрома Р450 и не ингибировал изофермент CYP3A4.
| Лек. форма | Дозировка | Кол-во, шт | Производитель |
|---|---|---|---|
| таблетки, покрытые пленочной оболочкой | 125 мг 250 мг 500 мг | 3 6 7 9 10 12 14 . | |
| таблетки, покрытые оболочкой | 125 мг 250 мг 500 мг | 3 6 7 9 10 12 14 . |
Сервисы РЛС ® Аврора Информация о лекарствах для медицинских систем
Содержание
- Действующее вещество
- Аналоги по АТХ
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- 3D-изображения
- Состав
- Фармакологическое действие
- Способ применения и дозы
- Форма выпуска
- Производитель
- Условия отпуска из аптек
- Условия хранения препарата Фамвир
- Срок годности препарата Фамвир
- Заказ в аптеках Москвы
- Отзывы
Действующее вещество
Аналоги по АТХ
Фармакологическая группа
Нозологическая классификация (МКБ-10)
3D-изображения
Состав
| Таблетки, покрытые оболочкой | 1 табл. |
| активное вещество: | |
| фамцикловир | 125 мг |
| 250 мг | |
| 500 мг | |
| вспомогательные вещества: натрия крахмал гликолят — 8,26/16,52/27,35 мг; гидроксипропилцеллюлоза — 3,86/7,73/15,48 мг; лактоза безводная — 26,85/53,69/- мг; магния стеарат — 1,24/2,48/4,1 мг | |
| оболочка (Opadry OY-S-28924): гипромеллоза — 2,42/4,84/8,01 мг; титана диоксид — 0,99/1,98/3,28 мг; полиэтиленгликоль 4000 — 0,36/0,72/1,2 мг; полиэтиленгликоль 6000 — 0,36/0,72/1,2 мг |
Фармакологическое действие
Способ применения и дозы
Внутрь, независимо от приема пищи, не разжевывая, запивая водой. Лечение препаратом следует начинать как можно раньше, сразу после появления первых симптомов заболеваний (покалывание, зуд и жжение).
Инфекция, вызванная вирусом Varicella zoster (опоясывающий герпес), у пациентов с нормальным иммунитетом. Рекомендуемая доза составляет 500 мг 3 раза в сутки в течение 7 дней. Такой способ применения позволяет снизить продолжительность постгерпетической невралгии. В острую фазу заболевания для разрешения кожных проявлений рекомендуемая доза составляет 250 мг 3 раза в сутки или 500 мг 2 раза в сутки или 750 мг 1 раз в сутки в течение 7 дней.
Офтальмогерпес, вызванный вирусом Varicella zoster, у пациентов с нормальным иммунитетом. Рекомендуемая доза составляет 500 мг 3 раза в сутки в течение 7 дней.
Инфекция, вызванная вирусом Varicella zoster (опоясывающий герпес), у пациентов со сниженным иммунитетом. Рекомендуемая доза составляет 500 мг 3 раза в сутки в течение 10 дней.
Инфекция, вызванная вирусом Herpes simplex (лабиальный или генитальный герпес), у пациентов с нормальным иммунитетом. При первичном генитальном герпесе рекомендуемая доза составляет 250 мг 3 раза в сутки в течение 5 дней. При рецидивах генитального герпеса назначают 1000 мг 2 раза в сутки в течение 1 дня или 125 мг 2 раза в сутки в течение 5 дней или 500 мг однократно с последующим применением 3 доз по 250 мг каждые 12 ч. При рецидивах лабиального герпеса — 1500 мг однократно в течение 1 дня или 750 мг 2 раза в сутки в течение 1 дня.
Инфекция, вызванная вирусом Herpes simplex (лабиальный или генитальный герпес), у пациентов со сниженным иммунитетом. Рекомендуемая доза составляет 500 мг 2 раза в сутки в течение 7 дней.
Для профилактики обострений рецидивирующей инфекции, вызванной вирусом Herpes simplex, — супрессивная терапия — назначают 250 мг 2 раза в сутки. Длительность терапии зависит от тяжести заболевания. Рекомендуется периодическая оценка возможных изменений течения заболевания через 12 мес. У ВИЧ-инфицированных пациентов эффективная доза составляет 500 мг 2 раза в сутки.
Пациенты в возрасте ≥65 лет. У пожилых пациентов с нормальной почечной функцией коррекция режима дозирования фамцикловира не требуется.
Пациенты с нарушениями функции почек. У пациентов с нарушениями функции почек отмечается уменьшение клиренса пенцикловира. Коррекция режима дозирования в зависимости от Cl креатинина представлена в таблицах.
Коррекция режима дозирования в зависимости от Cl креатинина при инфекции, вызванной вирусом Varicella zoster (опоясывающий герпес), у пациентов с нормальным иммунитетом
| Режим дозирования в течение 7 дней | Cl креатинина, мл/мин | Скорректированный режим дозирования в течение 7 дней |
| 500 мг 3 раза в сутки | ≥60 | 500 мг 3 раза в сутки |
| 40–59 | 500 мг 2 раза в сутки | |
| 20–39 | 500 мг 1 раз в сутки | |
| Cl креатинина при инфекции, вызванной вирусом Varicella zoster (опоясывающий герпес), у пациентов со сниженным иммунитетом |
| Режим дозирования в течение 10 дней | Cl креатинина, мл/мин | Скорректированный режим дозирования в течение 10 дней |
| 500 мг 3 раза в сутки | ≥60 | 500 мг 3 раза в сутки |
| 40–59 | 500 мг 2 раза в сутки | |
| 20–39 | 500 мг 1 раз в сутки | |
| Cl креатинина при инфекции, вызванной вирусом Herpes simplex, у пациентов с нормальным иммунитетом |
| Режим дозирования | Cl креатинина, мл/мин | Скорректированный режим дозирования |
| Первый эпизод | ||
| 250 мг 3 раза в сутки в течение 5 дней | ≥40 | 250 мг 3 раза в сутки в течение 5 дней |
| 20–39 | 250 мг 2 раза в сутки в течение 5 дней | |
| Cl креатинина при профилактике обострений рецидивирующей инфекции, вызванной вирусом Herpes simplex (супрессивная терапия) | ||
| Режим дозирования | Cl креатинина, мл/мин | Скорректированный режим дозирования |
| 250 мг 2 раза в сутки | ≥40 | 250 мг 2 раза в сутки |
| 20–39 | 125 мг 2 раза в сутки | |
| Cl креатинина при инфекции, вызванной вирусом Herpes simplex (лабиальный или генитальный герпес), у пациентов со сниженным иммунитетом |
| Режим дозирования в течение 7 дней | Cl креатинина, мл/мин | Скорректированный режим дозирования в течение 7 дней |
| 500 мг 2 раза в сутки | ≥40 | 500 мг 2 раза в сутки |
| 20–39 | 500 мг 1 раз в сутки | |
| ® в дозе 1000 мг 2 раза в сутки для лечения рецидива генитального герпеса у иммунокомпетентных пациентов негроидной расы не превышала таковую для плацебо. Клиническая значимость режимов дозирования препарата для лечения как рецидивов генитального герпеса (в течение 2 или 5 дней), так и других инфекционных поражений, вызванных вирусами Varicella zoster и Herpes simplex, неизвестна. |
Форма выпуска
Таблетки, покрытые оболочкой, 125 мг и 250 мг. По 7 или 10 табл. в блистере; по 1, 2, 3 или 4 блистера в картонной пачке.
Таблетки, покрытые оболочкой, 500 мг. По 3, 7 или 10 табл. в блистере; по 1, 2, 3 или 4 блистера в картонной пачке.
Производитель
Новартис Фарма АГ. Швейцария, Лихтштрассе, 35, 4056 Базель.
Произведено: Новартис Фармасьютика С.А. Испания.
Дополнительную информацию о препарате можно получить по адресу: 115035, Москва, Садовническая ул., 82/2.
Тел.: (495) 967-12-70; факс: (495) 967-12-68.
Продвижение на территории РФ: представительство фирмы «Д-р Редди'c Лабораторис Лтд.». 115035, Москва, Овчинниковская наб., 20, стр. 1.
Тел.: (495) 795-39-39, 783-29-01; факс: (495) 795-39-08.
Условия отпуска из аптек
Условия хранения препарата Фамвир ®
Хранить в недоступном для детей месте.
Срок годности препарата Фамвир ®
Не применять по истечении срока годности, указанного на упаковке.
Читайте также:

