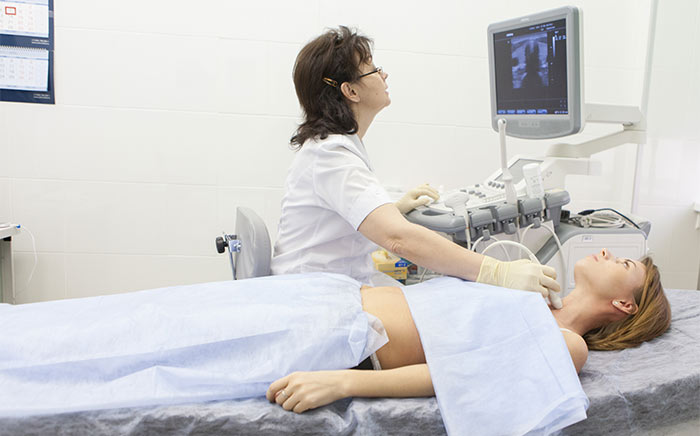
Что такое кошачий пищевод у человека
Опубликовано: 17.04.2024
| Приглашаем в Telegram-канал @Gastroenterology | Если лечение не помогает | Популярно о болезнях ЖКТ | Кислотность желудка |
Эозинофильный эзофагит (англ. eosinophilic esophagitis; EoE) — клиническая форма поражения пищевода, развивающаяся на фоне аутоимунных заболеваний. Характеризуется увеличенным количеством эозинофилов в слизистой оболочке пищевода (эозинофилы — один из видов лейкоцитов крови). Предполагают, что причиной такой формы эзофагита является пищевая или респираторная аллергия и она требует иной тактики лечения, отличной от рефлюкс-эзофагита.
Эозинофильный эзофагит имеет тенденцию к увеличению частоты. В США в настоящее время зафиксировано 150 000 больных эозинофильным эзофагитом, 75 % из которых — взрослые.
Эозинофильный эзофагит является распространенной причиной рефрактерной терапии к гастроэзофагельной рефлюксной болезни (ГЭРБ). Пациенты с эозинофильным эзофагитом обычно молодые люди, имеющие в анамнезе указания на перемежающуюся дисфагию, появляющуюся после приёма твердой пищи, и часто — на задержку пищи в пищеводе. Довольно частым ошибочным диагнозом при наличии эзофагита у этих больных является ГЭРБ. У многих больных имеется связь с развитием астмы или наличием пищевой аллергии, особенно против молока, яиц, арахиса или дынь. На предполагаемый диагноз эозинофильного эзофагита указывают эндоскопические проявления: множественные кольца в просвете пищевода, продольные бороздки, или экссудат белого цвета (Пасечников В.Д.).

Эндоскопические признаки эозинофильного эзофагита. (А) Кольца в слизистой оболочке пищевода, образовавшиеся вследствие преходящих сокращений пищевода или фиксированных стриктур -"трахееподобный пищевод". (В) Белесоватый экссудат в виде точечных белых узелков, диспергированный хлопьеобразующий материал гранулярного происхождения. (С) Продольные бороздки (белая стрелка и белесоватый экссудат) вдоль складок пищевода. Furuta G. et al, Gastroenterology, 2007; 133: 1342-1363

Гистологическое исследование биоптата. Гиперплазия клеток базального слоя многослойного плоского эпителия (а). Эозинофилы в межклеточных пространствах – более 20 в 1 поле высокого разрешения в многослойном плоском эпителии пищевода (б). Окраска гематоксилином и эозином. Увел. а) х120, б) х500 (Валитова Э.Р. и др.).
При биопсии проксимального и дистального отделов пищевода в гистологических препаратах определяются более 15-20 эозинофилов в поле зрения.

Эозинофильный абсцесс в слизистой оболочке пищевода. Furuta G. et al, Gastroenterology, 2007; 133: 1342-1363.
Периферическая эозинофилия не является распространенным патологическим признаком. Патогенез эозинофильного эзофагита не известен. Предполагают, что развитие этого состояния провоцируется приемом пищи и аэроаллергенов, стимулирующих ответ цитокинов, обусловленных активацией Т-хелперов 2 типа, другие исследования предполагают, что у некоторых пациентов имеется атипичный вариант ГЭРБ. Естественное течение эозинофильного эзофагита плохо изучено, но известно, что оно не связано с исходом в рак пищевода. Симптомы этого заболевания и снижение количества эозинофилов в ткани достигается после трёхмесячного назначения ингаляционных стероидов (флутиказона пропионата дважды в день утром и вечером по 440 мкг). Для гарантированного адекватного поступления стероидов в пищевод, а не в легкие, спейсер не должен использоваться вместе с ингалятором. В случае, если ингаляционные стероиды не приводят к разрешению симптомов, используется иная терапия, включающая применение антагониста лейкотриена D4 (монтелюкаста 10-40 мг в день) или пероральных стероидов (преднизон 30 мг в день в течение 2 недель) с постепенным снижением дозы в течение 6 недель. У других пациентов используются ингибиторы протонной помпы с последующим бужированием стриктур (Пасечников В.Д.).
Имеются исследования, доказывающие, что после исключения из рациона больных шести групп наиболее вероятных аллергенов (молочные продукты, соя, пшеница, орехи, морепродукты, яйца) у большинства отмечаются клинические, эндоскопические и гистологические улучшения (Wolf WA et al, Clin Gastroenterol Hepatol. 2014;12:1272-1279).

Распространённость эозинофильного эзофагита в США. Максимум приходится на мужчин в возрасте 35-39 лет. Delon E.S. et al, Clin Gastroenterol Hepatol 2014; 12: 589-96
Лечение эозинофильного эзофагита
Ингибиторы протонной помпы 20–40 мг (в зависимости от выбранного препарата) 1–2 раза в день в течение 8–12 недель или 1 мг/кг на 1 прием дважды в день в течение 8–12 недель у детей значительно облегчают симптомы и приводит к нормализации гистологической картины у значительной группы пациентов.
Специальная диета приводит в большинстве случаев к практически полному купированию симптомов и нормализации гистологической картины у больных эозинофилией детей и даже к обратному развитию фиброза стенки пищевода. Эффективны следующие диетические режимы:
- Элементные диеты с использованием смесей со строгим аминокислотным составом, что в 90% приводит к достижению гистологической ремиссии у детей.
- Элиминационные диеты с исключением продуктов, вызывающих аллергию у конкретного индивида. Диета основывается на результатах мультимодального аллергологического тестирования (кожные тесты и определение сывороточного IgE). Положительный эффект удается достичь в 77% случаев.
- Эмпирическая диета с исключением из рациона продуктов с высоким аллергенным потенциалом (яйца, молоко, соя, грибы, орехи, пшеница, рыба и др.). Гистологический ответ наблюдается в среднем у 74% пациентов.
Системное применение кортикостероидов имеет строгие показания: тяжелая дисфагия как результат осложнений эозинофильного эзофагита (стриктуры и узкий пищевод); связанная с осложнениями госпитализация; потеря массы тела. Из-за значительных побочных эффектов длительное применение системных стероидов при эозинофильном эзофагите не рекомендовано.
Топические стероиды применяют у детей и взрослых для индукции ремиссии и поддерживающей терапии. Они хорошо переносимы и имеют минимальные побочные эффекты, среди которых наиболее частыми являются кандидоз полости рта и пищевода, герпетическая инфекция. Для индукции ремиссии применяют флутиказон в дозе 440–880 мкг дважды в день по схеме впрыск–глоток и будесонид (густая суспензия) 2 мг в день. После приема топических стероидов не рекомендуется принимать пищу и пить в течение 30 минут. После успешной индукции ремиссии необходима длительная поддерживающая терапия.
Раздел «Лечение. » написан на основе статьи Ивашкина В.Т. и др.
Е. В. Иванова, Н. Н. Щеголева, Л. М. Михалева, З. В. Галкова, Е. Д. Федоров
Научно-образовательный центр абдоминальной хирургии и эндоскопии РГМУ им. Н. И. Пирогова (Зав. — проф. С. Г. Шаповальянц)
ГКБ № 31 (гл. врач член-корр. РАМН, проф. Г. Н. Голухов)
г. Москва
Эозинофильный эзофагит (ЭоЭ) (синонимы: первичный-, аллергический-, идиопатический ЭоЭ) — это воспалительное заболевание пищевода со специфическими клиническими и патоморфологическими проявлениями, характеризующееся плотной эозинофильной инфильтрацией стенки пищевода, с выраженной гиперплазией плоскоклеточного эпителия. В норме в слизистой оболочке пищевода эозинофилы отсутствуют. Их выявление у пациентов с симптомами гастроэзофагеальной рефлюксной болезни (ГЭРБ) ранее, с конца 70-х до середины 90-х годов, относили к ее проявлениям. Однако к 1995 году появилось достаточно данных, чтобы утверждать, что изолированная эозинофильная инфильтрация пищевода может быть проявлением отдельного заболевания [5]. Интерес к проблеме усилился в последние годы; в частности, за последние 5 лет опубликовано более половины всех научных работ посвященных ЭоЭ. На сегодняшний день ЭоЭ считается наиболее частым «эозинофильным заболеванием» желудочно-кишечного тракта. Заболеванию подвержены, как дети, так и взрослые; конкретные цифры его распространенности до конца не ясны [8]. ЭоЭ чаще встречается у мужчин (3:1) и у детей. Вопросы этиологии данного заболевания дискутабельны. Рассматривается роль пищевых и воздушных аллергенов. Также обсуждается возможность аутоиммунного характера заболевания. Считается, что пищевая аллергия при ЭоЭ носит характер пищевой гиперчувствительности и является аллергической реакцией IV типа.
Клиническая диагностика ЭоЭ затруднительна, так как симптомы заболевания подобны таковым при ГЭРБ. Они включают изжогу, срыгивание, рвоту, боль в эпигастрии, дисфагию, ощущение остановки пищевого комка и одинофагию. Симптомы, особенно рвота и дисфагия, чаще носят интермитирующий характер с частотой 1-2 раза в месяц. Изжога и боль в эпигастрии более постоянны. Около 35-45 % пациентов имеют семейный анамнез пищевой аллергии или астмы. Сопутствующий бронхоспазм, экзема или ринит встречается у 45-50 % больных. Важно то, что несмотря на схожесть клинической картины ЭоЭ и ГЭРБ, симптомы и патоморфологические изменения слизистой оболочки пищевода характерные для ЭоЭ не устраняются при приеме медикаментов, подавляющих кислотопродукцию, в том числе при приеме ингибиторов протонной помпы в высоких дозах. Однако исключение специфического пищевого аллергена (ов) способно нивелировать симптомы заболевания. Основные критерии дифференциальной диагностики ЭоЭ и ГЭРБ приведены в таблице 1.
Табл. 1. Дифференциальная диагностика эозинофильного эзофагита и ГЭРБ
| Эозинофильный эзофагит | ГЭРБ |
| Симптомы дисфункции пищевода — интермитирующие | Симптомы — постоянные |
| Нормальные данные рН-метрии | Патологические данные рН-метрии |
| Антисекреторная терапия без эффекта | Антисекреторная терапия эффективна |
| В биоптате слизистой оболочки имеется более 15 эозинофилов в поле зрения | В биоптате слизистой оболочки имеется 1-5 эозинофилов в поле зрения |
Эндоскопическая картина и эндосонография. ЭоЭ не имеет патогномоничных эндоскопических признаков, хотя часть авторов настаивает на существовании ряда критериев, позволяющих заподозрить эту патологию при выполнении эндоскопии. Основные изменения слизистой оболочки пищевода – множественные циркулярные кольца (трахееподобный вид, «кошачий пищевод»), отек, вертикальные борозды, узловатость, белесые точки или наложения; возможно сужение просвета и наличие стриктур пищевода [1, 6, 7]. Однако специфичность этих признаков невысока, а у 40-50 % пациентов с ЭоЭ эндоскопическая картина соответствует норме. В последнее время появились сообщения, что для эозинофильного эзофагита характерна высокая ранимость слизистой, для ее описания даже был предложен термин — слизистая типа «папиросной бумаги» [10]. В исследовании Fox V. L. с соавт. [3] у 11 детей с эозинофильным эзофагитом было выполнено ультразвуковое исследование пищевода. По данным ЭУС было отмечено значительное утолщение всей стенки пищевода или её отдельных слоёв.
Морфология.
Для ЭоЭ характерна «выраженная» изолированная эозинофильная инфильтрация пищевода. Несмотря на то, что однозначного толкования понятия «выраженная» не достигнуто, большинство авторов соглашается с тем, что наличие более 15-20 эозинофилов в поле зрения является достоверным диагностическим критерием ЭоЭ [8]. Однако, эозинофилия пищевода, правда менее выраженная, встречается не только при ЭоЭ. Она наблюдается и при других заболеваниях, таких как ГЭРБ, болезнь Крона, заболевания соединительной ткани, инфекционный эзофагит (герпес, кандидоз), лекарственно-ассоциированный эзофагит, гиперэозинофильный синдром и эозинофильный гастроэнтерит. Отличительной особенностью ЭоЭ при морфологическом исследовании является выраженная стойкая эозинофилия слизистой оболочки пищевода, зачастую с эозинофильными микро-абсцессами. Слизистая оболочка желудка и двенадцатиперстной кишки при ЭоЭ, как правило, не изменена.
Осложнения, встречающиеся при ЭоЭ.
Считается, что хроническое эозинофильное воспаление является причиной истонченности, ранимости и потери эластичности слизистой оболочкой пищевода. Это, в свою очередь, способно привести к разрывам слизистой в ходе проведения эндоскопического исследования и дилатации пищевода, а также к трансмуральной перфорации при ЭГДС и к разрыву пищевода при вклинении в просвет органа пищевого комка [9]. С учетом этого, сразу несколько авторов призывают к соблюдению осторожности при эндоскопическом лечении сужений и стриктур пищевода, вызванных ЭоЭ. В настоящее время принято считать, что эндоскопическую дилатацию пищевода следует выполнять только у тех пациентов, у которых местная терапия стероидами в течение 8 недель была не эффективной [4].
Лечение.
Терапия при ЭоЭ включает элиминационную диету (исключение из питания аллергогенных групп продуктов — молока, сои, яиц, пшеницы, рыбы, моллюсков и орехов) и применение местных кортикостероидов, таких как флутиказон, будесонид или беклометазон [2]. Рекомендуется два распыления этих препаратов в ротовой полости с последующим проглатыванием два раза в день в течение 6 недель. Единственным описанным осложнением такой терапии является кандидоз пищевода, который наблюдался при применении флyтиказона в дозе 220 мг два раза в день [11]. Кроме того, в лечении используются селективные антагонисты лейкотриенов и препараты, направленные на снижение продукции цитокинов. Антисекреторная терапия и антирефлюксные операции при ЭоЭ не эффективны.
Клинический пример.
Пациент С., 17 лет, обратился в нашу клинику 13.07.2010г. с жалобами на чувство дискомфорта в эпигастрии для проведения диагностической ЭГДС. Позже, при более тщательном сборе анамнеза, мы выяснили, что при аллергической реакции на употребление даже незначительного количества «запрещенных» продуктов или пищи их содержащей, например, орехов, пациент достаточно часто наблюдал тошноту, затруднение прохождения пищи по пищеводу, чувство комка за грудиной. Боли и изжоги его не беспокоили. С первых лет жизни наш пациент страдал выраженной пищевой и лекарственной аллергией, которая проявлялась сыпью на коже, ринитом, отеком Квинке; ранее перенёс анафилактический шок. В детском возрасте часто и длительно, до 6-7 раз в год, болел простудными заболеваниями. В возрасте 4-х лет был поставлен диагноз атопическая бронхиальная астма. По данным результатов общего анализа крови, на протяжении всей жизни, отмечалась эозинофилия. Нами при первичной ЭГДС высокой чёткости и в узком спектре света были выявлены: небольшая хиатальная грыжа; рефлюкс-эзофагит степени В по Лос-Анжелесской классификации; ультракороткий пищевод Барретта (С0М0,8) – единственный «язычок», выстланный эпителием кардиального типа, в т. ч. по данным морфологического исследования; воспалительно-гиперпластические изменения в основании эрозий в зоне пищеводно-желудочного перехода; эндоскопические признаки кандидомикоза пищевода (множественные белесоватые несмываемые бляшки, но без морфологического подтверждения!); Нр-ассоциированный эрозивный антрум-гастрит и эрозивный бульбит. Было проведено лечение (нексиум, де-нол, вильпрофен, флемоксин, мотилиум, флуконазол). При повторном осмотре через 3 месяца (19.10.2010г.) жалоб нет. На фоне полной эпителизации эрозий пищевода и желудка нами было отмечено наличие характерных признаков эозинофильного эзофагита: «кошачий» пищевод (Рис.1), отек слизистой, вертикальные борозды (Рис. 2), множественные белесые наложения (Рис. 3), которые ранее расценивались как проявления кандидозной инфекции.

Рисунок 1. Множественные, часто расположенные поперечные кольцевидные складки слизистой оболочки по ходу пищевода (трахееподобный вид пищевода, «кошачий» пищевод)

Рисунок 2. Вертикальные борозды на слизистой оболочке пищевода (более четко видны при затекании в них крови после взятия биопсии)

Рисунок 3. Наложения на слизистой оболочке пищевода в виде множественных белесоватых точек

Рисунок 4. ЭУС стенки пищевода: смазанность слизистого и подслизистого слоев стенки органа
Для более точной верификации диагноза 28.12.2010г. мы выполнили пациенту ЭУС и повторную множественную щипцовую биопсию слизистой оболочки пищевода. При ЭУС выраженного утолщения стенки пищевода выявлено не было, однако отмечалась некоторая смазанность слизистого и подслизистого слоев (Рис. 4). По данным морфологического исследования выявлена выраженная эозинофильная инфильтрация в слизистом и подслизистом слоях: от 10 до 80 эозинофилов в поле зрения, при ув. х360 (Рис. 5, 6). При этом наличия мицелл грибка Candida albicans обнаружено не было (!), несмотря на то, что при этом предновогоднем исследовании размеры и количество несмываемых бляшек увеличилось и внешне они выглядели, как кандидомикоз пищевода. Подобные белесоватые наложения, судя по данным литературы и нашим находкам служат проявлением эозинофильных микроабсцессов.

Рисунок 5. Множественные эозинофилы (розовые клетки) в многослойном плоском эпителии (окр. гематоксилин-эозин, ув. х40)

Рисунок 6. Множественные эозинофилы (розовые клетки) в подслизистом слое (окр. гематоксилин-эозин, ув. х40)
Таким образом, по совокупности клинических и инструментальных находок, пройдя этап недиагностированного заболевания, а затем этап клинических, эндоскопических и морфологических сомнений, в конечном итоге пациенту был установлен диагноз эозинофильный эзофагит. В настоящий момент консилиумом с «семейным» иммунологом и гастроэнтерологом обсуждается тактика ведения и подбирается оптимальное лечения нашего пациента.
- Ahmed A, Matsui S, Soetikno R. A novel endoscopic appearance of idiopathic eosinophilic esophagitis. Endoscopy 2000;32: S33.
- Dobbins JW, Sheahan DG, Behar J. Eosinophilic gastroenteritis with esophageal involvement. Gastroenterol 1977;72:1312-6.
- Fox VL, Nurko S, Teitelbaum JE, et al. High-resolution EUS in children with eosinophilic «allergic» esophagitis. Gastrointest Endosc 2003;57:30–36.
- Kaplan M, Mutlu E, Jakate S, et al., «Endoscopy in eosinophilic esophagitis: «Feline» esophagus and perforation risk», Clinical Gastroenterology and Hepatology (2003);1: pp. 433–437.
- Kelly KJ, Lazenby AJ, Rowe PC, Yardley JH, Perman JA, Sampson HA. Eosinophilic esophagitis attributed to gastroesophageal re. ux: improvement with an amino acid-based formula. Gastroenterology 1995;109:1503-12.
- Langdon DE. Congenital esophageal stenosis, corrugated ringed esophagus, and eosinophilic esophagitis. Am J Gastroenterol 2000;95:2123-4.
- Lim J, Gupta S, Fitzgerald J, Cro. e J, Pfe. erkorn M, Molleston J. White specks in esophageal mucosa (WSEM): a true endoscopic manifestation of severe eosinophilic esophagitis (EE) in children [abstract]. J Pediatr Gastroenterol Nutr 2001;33:411.
- Markowitz JE, Liacouras CA. Eosinophilic esophagitis. Gastroenterol Clin North Am. 2003 Sep;32(3):949-66.
- Riou P, Nicholson A, Pastorino U, «Esophageal Rupture in a patient with idiopathic eosinophilic esophagitis», Annals of Thoracic Surgery (1996);62: pp. 1,854–1,856.
- Straumann A, Rossi L, Simon HU, Heer P, Spichtin HP, Beglinger C. Fragility of the esophageal mucosa: a pathognomonic endoscopic sign of primary eosinophilic esophagitis? Gastrointest Endosc. 2003 Mar;57(3):407-12.
- Teitelbaum JE, Fox VL, Twarog FJ, Nurko S, Antonioli D, Gleich G, et al. Eosinophilic esophagitis in children: immunopathological analysis and response to futicasone propionate. Gastroenterology 2002;122:1216-25
Пищевод. Строение пищевода. Мышцы пищевода. Кровоснабжение и иннервация пищевода. Рентгеноанатомия пищевода. Эндоскопия пищевода. Лифатические узлы и пути лимфооттока от пищевода
Esophagus, пищевод, представляет узкую и длинную активно действующую трубку, вставленную между глоткой и желудком и способствующую продвижению пищи в желудок. Он начинается на уровне VI шейного позвонка, что соответствует нижнему краю перстневидного хряща гортани, и оканчивается на уровне XI грудного позвонка.
Так как пищевод, начавшись в области шеи, проходит дальше в грудную полость и, прободая диафрагму, входит в брюшную полость, то в нем различают части: partes cervicalis, thoracica et abdominalis.
Длина пищевода 23 — 25 см. Общая длина пути от передних зубов, включая сюда полость рта, глотку и пищевод, равняется 40 — 42 см (на такое расстояние от зубов, прибавив 3,5 см, надо продвинуть в пищевод желудочный резиновый зонд для взятия желудочного сока на исследование).
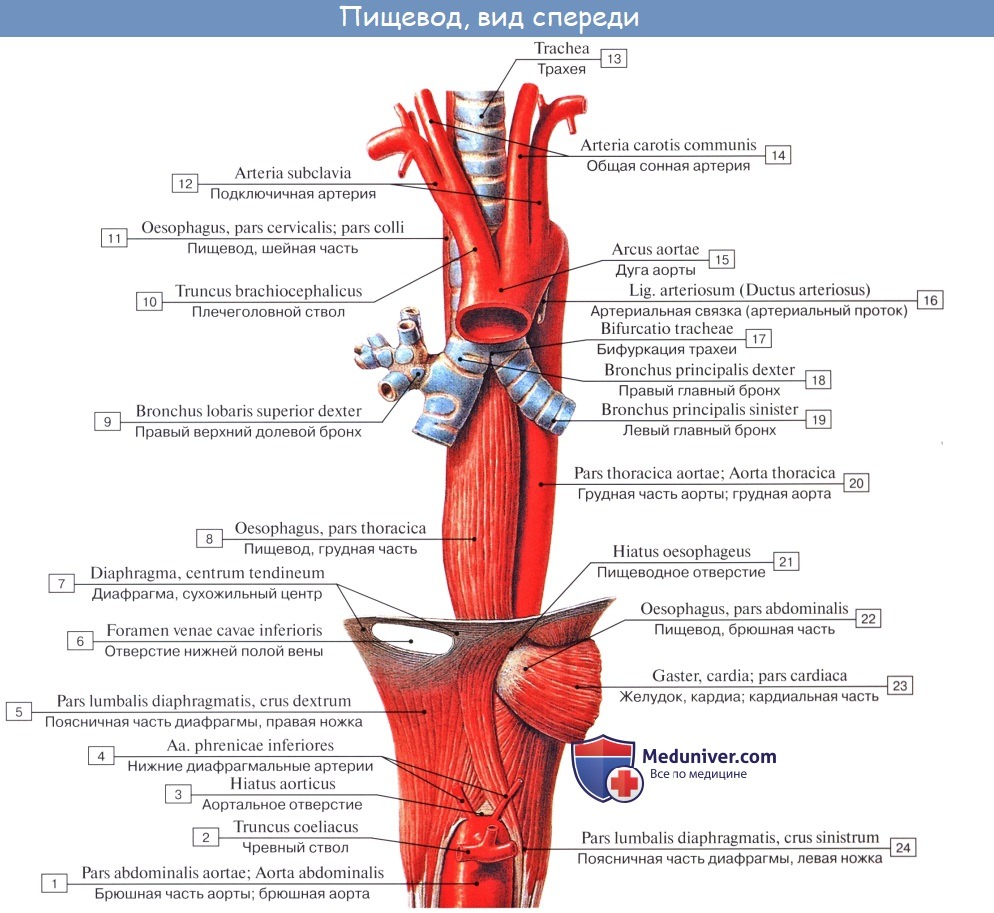
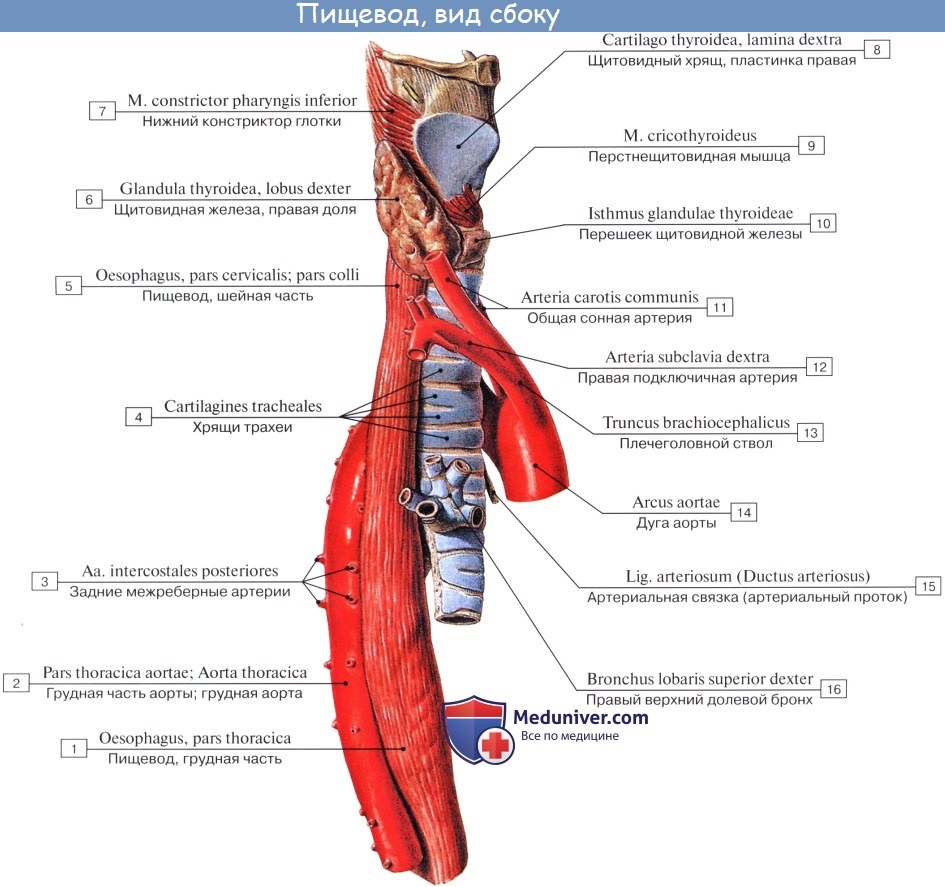
Топография пищевода
Шейная часть пищевода проецируется в пределах от VI шейного до II грудного позвонка. Спереди от него лежит трахея, сбоку проходят возвратные нервы и общие сонные артерии.
Синтопия грудной части пищевода различна на разных уровнях его: верхняя треть грудного отдела пищевода лежит позади и левее трахеи, спереди к ней прилежат левый возвратный нерв и левая a. carotis communis, сзади — позвоночный столб, справа — медиастинальная плевра.
В средней трети к пищеводу прилежит спереди и слева на уровне IV грудного позвонка дуга аорты, несколько ниже (V грудной позвонок) — бифуркация трахеи и левый бронх; сзади от пищевода лежит грудной проток; слева и несколько кзади к пищеводу примыкает нисходящая часть аорты, справа — правый блуждающий нерв, справа и сзади — v. azygos.
В нижней трети грудного отдела пищевода сзади и справа от него лежит аорта, кпереди — перикард и левый блуждающий нерв, справа — правый блуждающий нерв, который внизу смещается на заднюю поверхность; несколько кзади лежит v. azygos; слева — левая медиастинальная плевра.
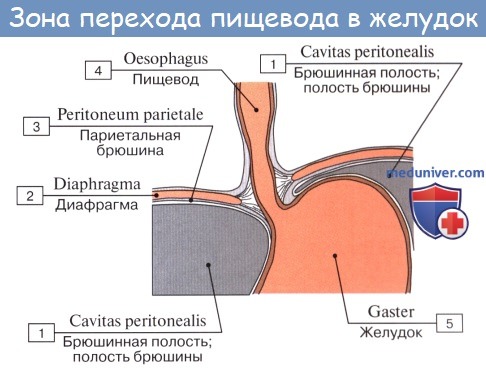
Брюшная часть пищевода спереди и с боков покрыта брюшиной; спереди и справа к нему прилежит левая доля печени, слева — верхний полюс селезенки, у места перехода пищевода в желудок располагается группа лимфатических узлов.
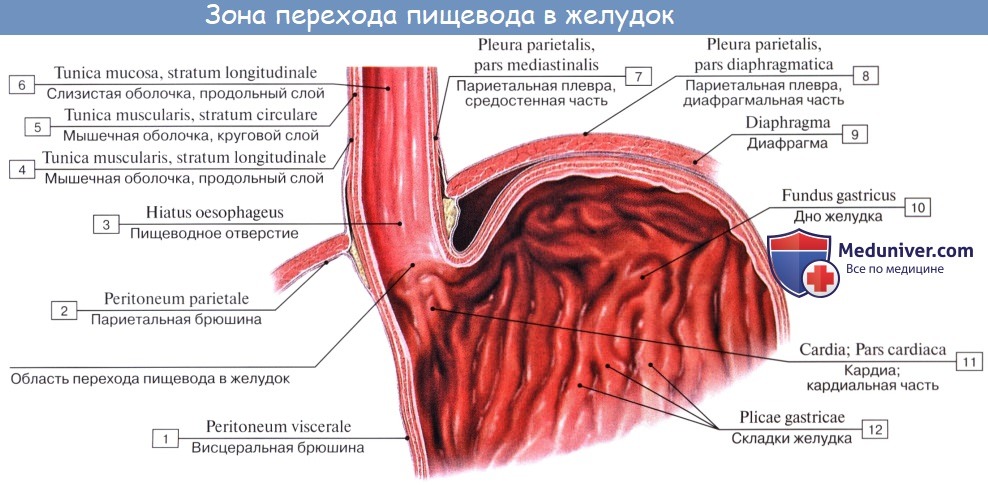
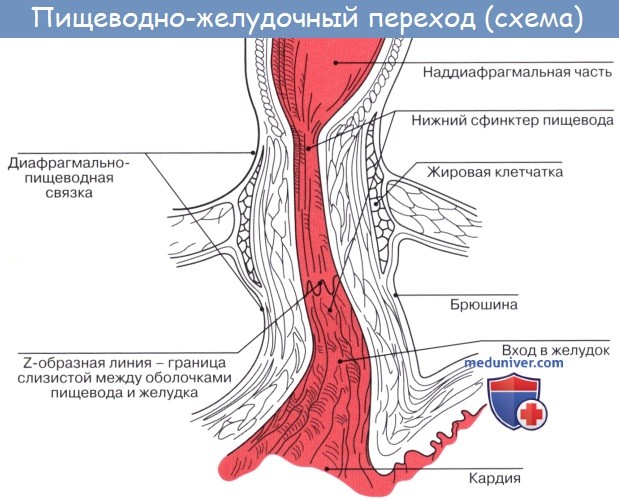
Строение пищевода
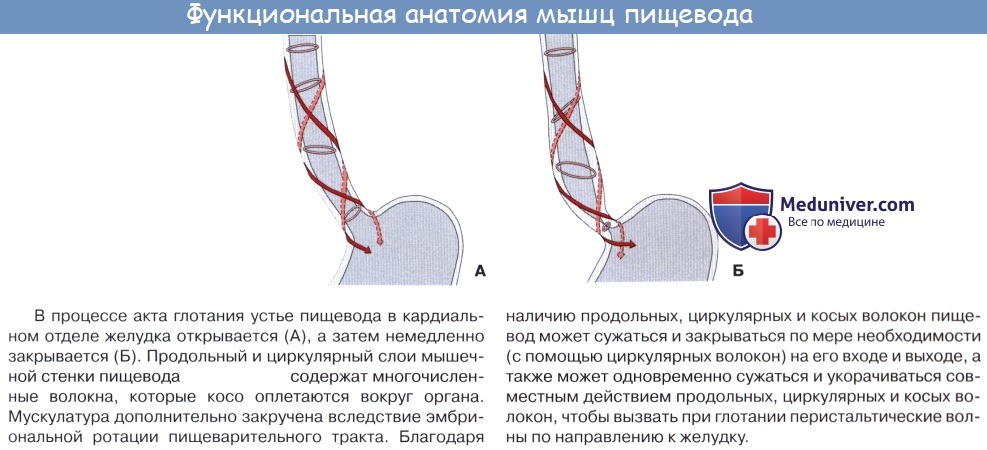
На поперечном разрезе просвет пищевода представляется в виде поперечной щели в шейной части (вследствие давления со стороны трахеи), в грудной же части просвет имеет кругловатую или звездчатую форму.
Стенка пищевода состоит из следующих слоев: самый внутренний — слизистая оболочка, tunica mucosa, средний — tunica muscularis и наружный — соединительнотканного характера — tunica adventitia. Tunica mucosa содержит слизистые железы, облегчающие своим секретом скольжение пищи при глотании. Кроме слизистых желез, встречаются еще в нижнем и, реже, в верхнем отделе пищевода маленькие железки, сходные по своему строению с кардиаль-ными железами желудка.
При нерастянутом состоянии слизистая собирается в продольные складки. Продольная складчатость есть функциональное приспособление пищевода, способствующее продвижению жидкостей вдоль пищевода по желобкам между складками и растяжению пищевода при прохождении плотных комков пищи. Этому содействует рыхлая tela submucosa, благодаря которой слизистая оболочка приобретает большую подвижность, а ее складки легко то возникают, то сглаживаются.
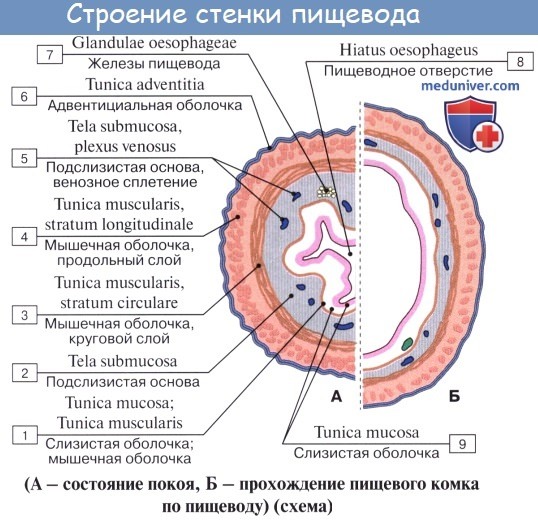
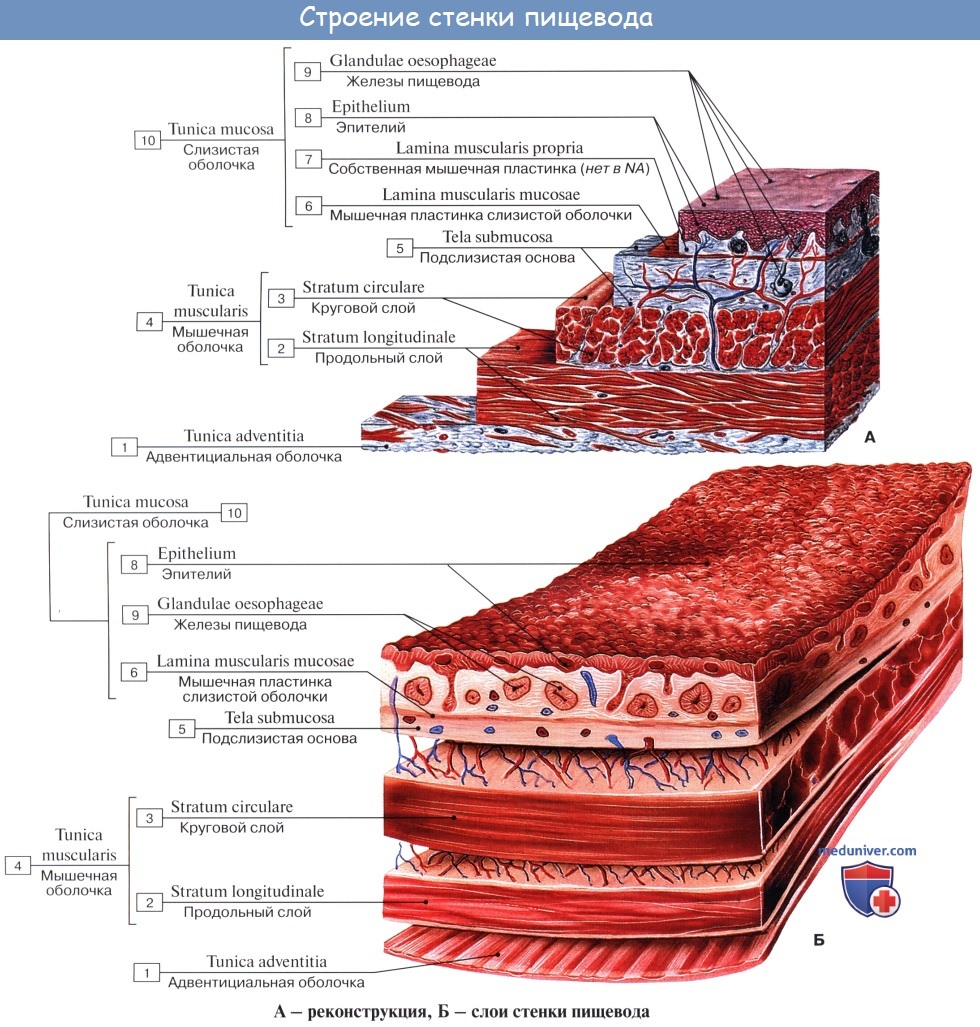
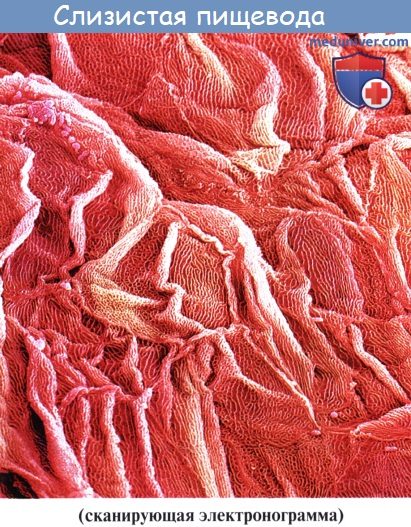
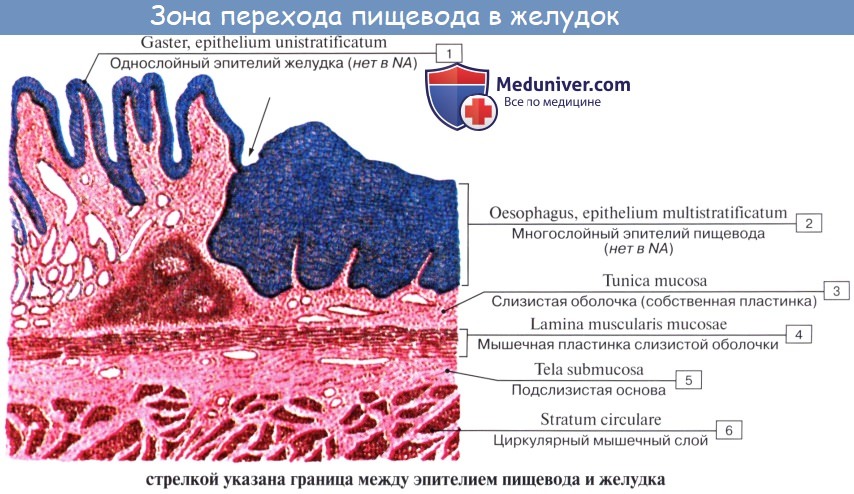
В образовании этих складок участвует и слой неисчерченных волокон самой слизистой оболочки, lamina muscularis mucosae. В подслизистой основе есть лимфатические фолликулы.
Tunica muscularis, соответственно трубчатой форме пищевода, который при выполнении своей функции проведения пищи должен расширяться и сжиматься, располагается в два слоя — наружный, продольный (расширяющий пищевод), и внутренний, циркулярный (суживающий). В верхней трети пищевода оба слоя складываются из исчерченных волокон, ниже они постепенно замещаются неисчерченными миоцитами, так что мышечные слои нижней половины пищевода состоят почти исключительно из непроизвольных мышц.
Tunica adventitia, окружающая пищевод снаружи, состоит из рыхлой соединительной ткани, с помощью которой пищевод соединяется с окружающими органами. Рыхлость этой оболочки позволяет пищеводу изменять величину своего поперечного диаметра при прохождении пищи. Pars abdomi-nalis пищевода покрыта брюшиной.
Рентгенологическое исследование пищеварительной трубки производится при помощи метода создания искусственных контрастов, так как без применения контрастных сред она не видна. Для этого исследуемому дается «контрастная пища» — взвесь вещества с большой атомной массой, лучше всего нерастворимый сульфат бария.
Эта контрастная пища задерживает рентгеновские лучи и дает на пленке или экране тень, соответствующую полости наполненного ею органа. Наблюдая при помощи рентгеноскопии или рентгенографии за движением таких контрастных пищевых масс, можно изучать рентгенологическую картину всего пищеварительного канала. При полном или, как говорят, «тугом» заполнении контрастной массой желудка и кишок рентгенологическая картина этих органов имеет характер силуэта или как бы слепка их; при небольшом заполнении контрастная масса распределяется между складками слизистой оболочки и дает изображение рельефа ее.
Рентгеноанатомия пищевода
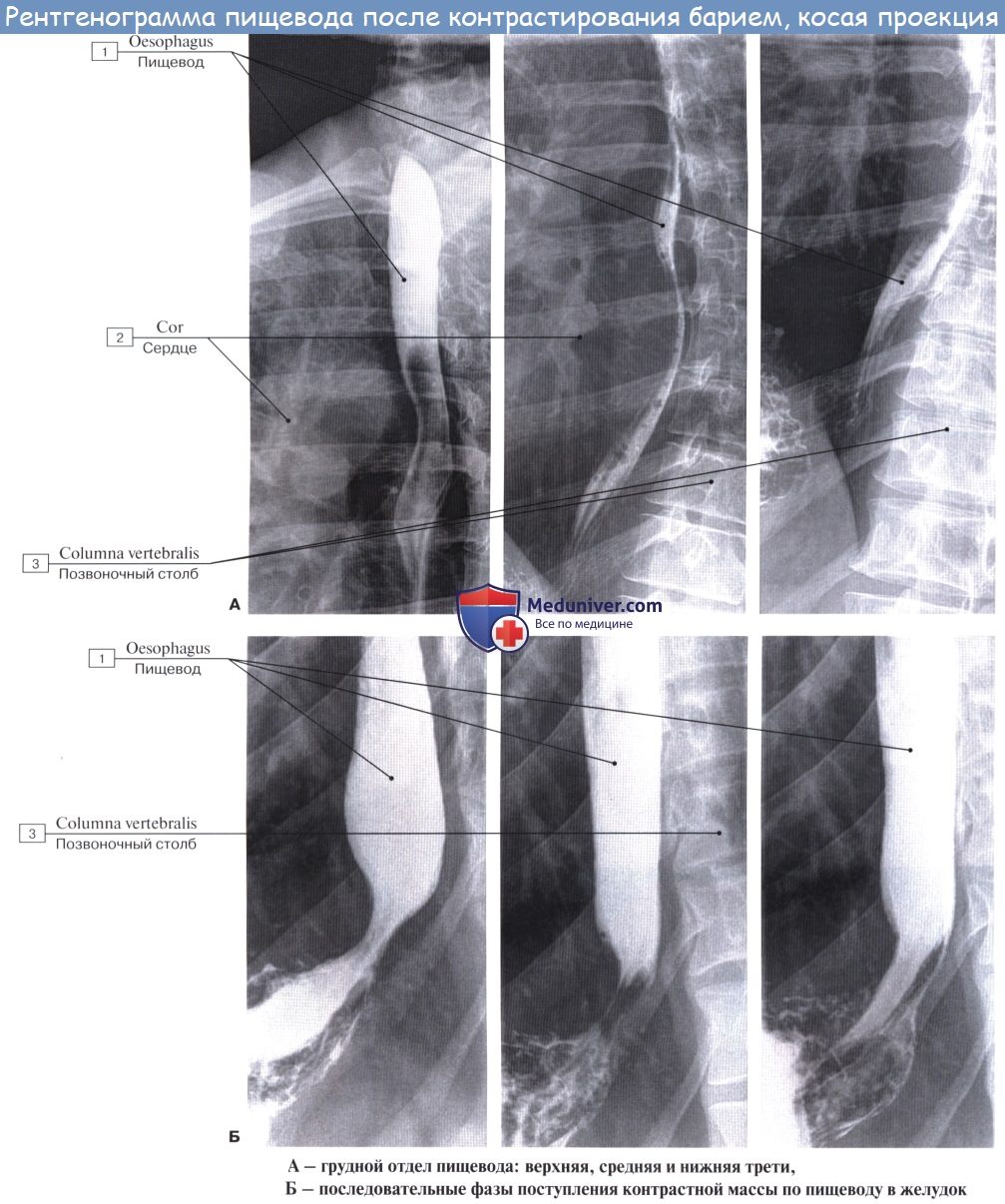
Пищевод исследуется в косых положениях — в правом сосковом или левом лопаточном. При рентгенологическом исследовании содержащий контрастную массу пищевод имеет вид интенсивной продольной тени, ясно заметной на светлом фоне легочного поля, расположенного между сердцем и позвоночным столбом. Эта тень является как бы силуэтом пищевода.
Если основная масса контрастной пищи проходит в желудок, а в пищеводе остается проглоченный воздух, то в этих случаях можно видеть контуры стенок пищевода, просветление на месте полости его и рельеф продольных складок слизистой оболочки. На основании данных рентгенологического исследования можно заметить, что пищевод живого человека отличается от пищевода трупа рядом особенностей, обусловленных наличием у живого прижизненного мышечного тонуса. Это прежде всего касается положения пищевода.
На трупе он образует изгибы: в шейной части пищевод сначала идет по средней линии, затем слегка отклоняется от нее влево, на уровне V грудного позвонка он возвращается к средней линии, а ниже вновь отклоняется влево и вперед к hiatus esophageus диафрагмы. На живом изгибы пищевода в шейном и грудном отделах меньше выражены.
Просвет пищевода имеет ряд сужений и расширений, имеющих значение при диагностике патологических процессов:
1) фарингеальное (у начала пищевода),
2) бронхиальное (на уровне бифуркации трахеи) и
3) диафрагмальное (при прохождении пищевода сквозь диафрагму). Это анатомические сужения, сохраняющиеся на трупе.
Но имеются еще два сужения — аортальное (у начала аорты) и кардиальное (при переходе пищевода в желудок), которые бывают выражены только у живого человека.
Выше и ниже диафрагмального сужения имеются два расширения. Нижнее расширение можно рассматривать как своего рода преддверие желудка.
Рентгеноскопия пищевода живого человека и серийные снимки, сделанные с промежутками в 0,5 — 1 с, позволяют исследовать акт глотания и перистальтику пищевода.
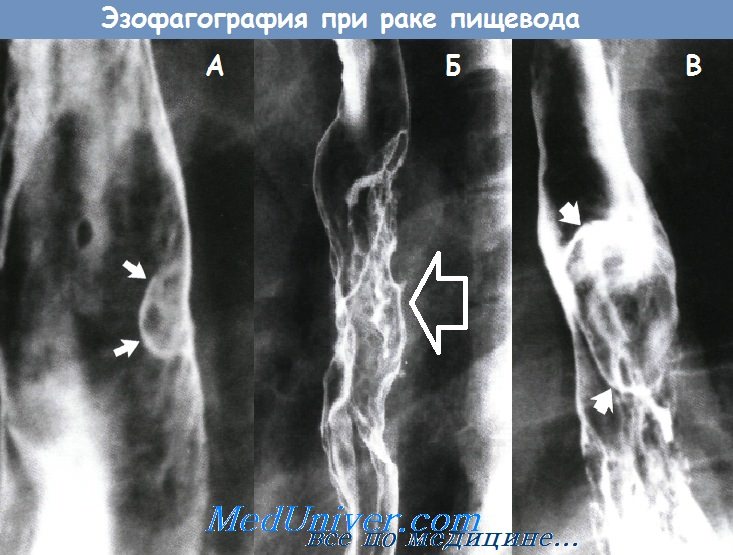
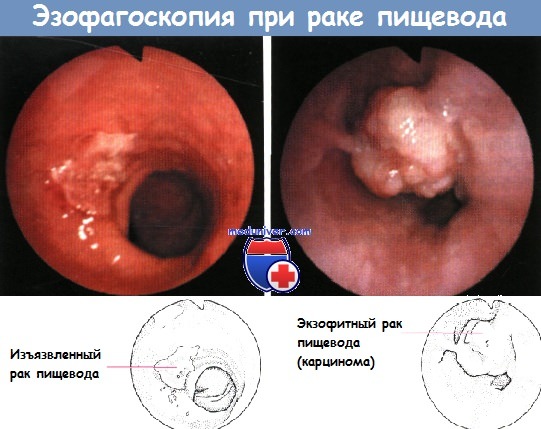
А - рак пищевода в виде полипа на широком основании
Б - инфильтрирующий рак пищевода
В - полипозный рак пищевода 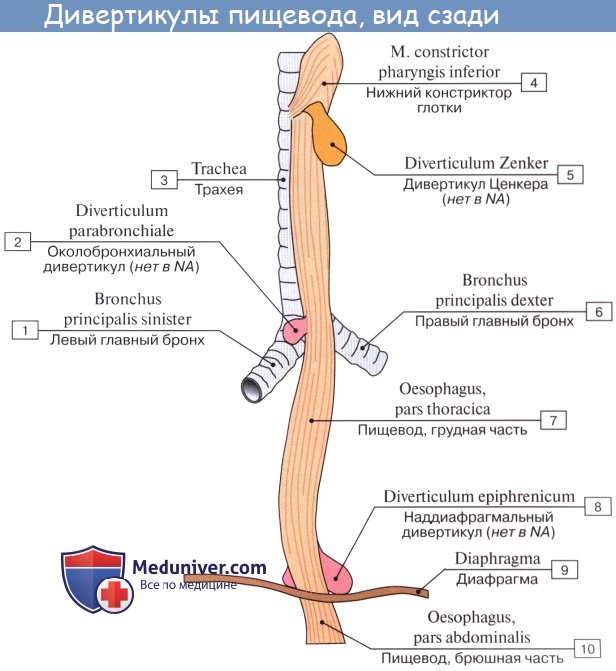
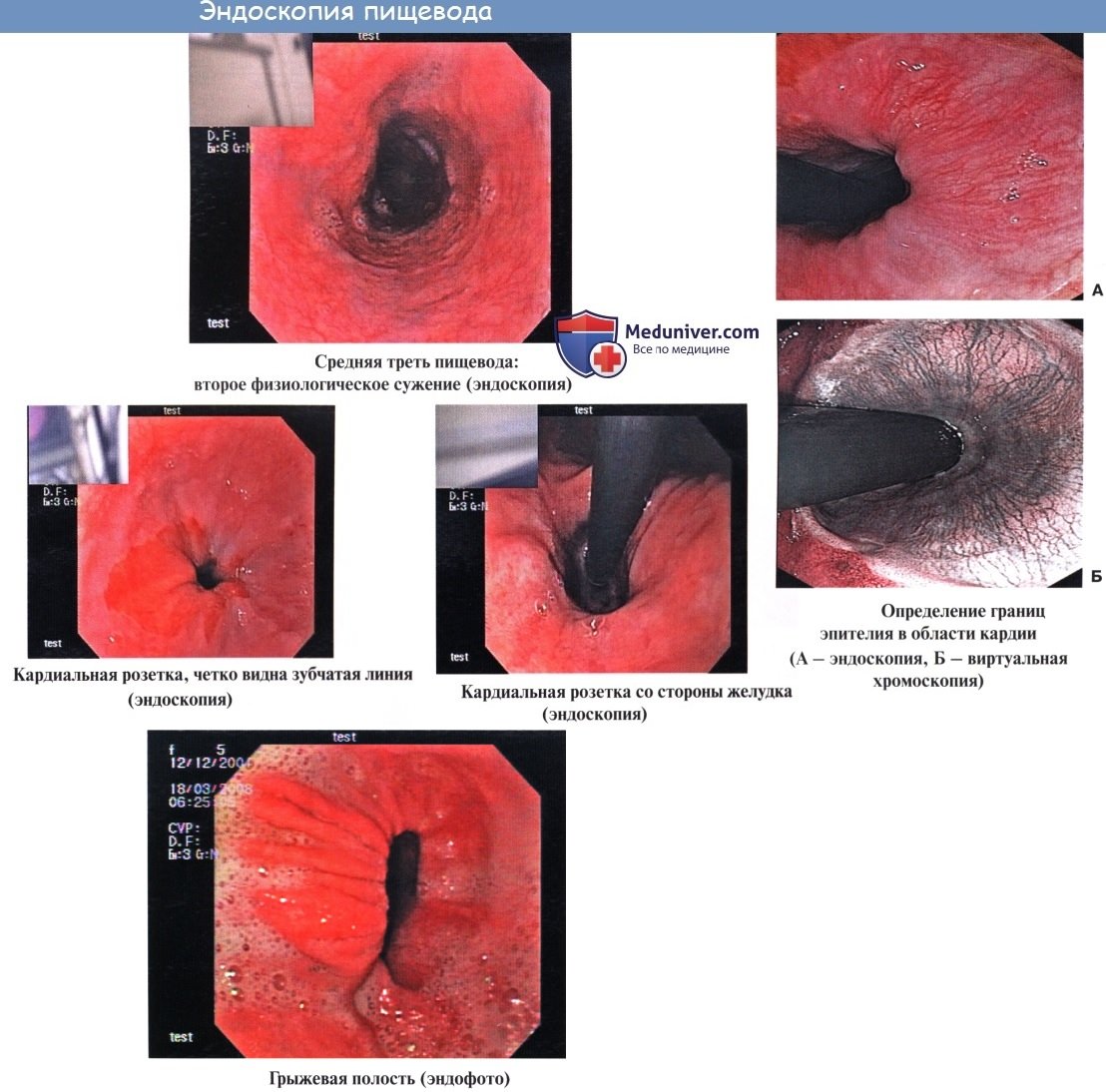
Эндоскопия пищевода
При эзофагоскопии (т. е. при осмотре пищевода больного человека с помощью особого прибора — эзофагоскопа) слизистая оболочка гладкая, бархатистая, влажная. Продольные складки мягкие, пластичные. Вдоль них идут продольные сосуды с разветвлениями.
Кровоснабжение и иннервация пищевода. Лифатические узлы и пути лимфооттока от пищевода
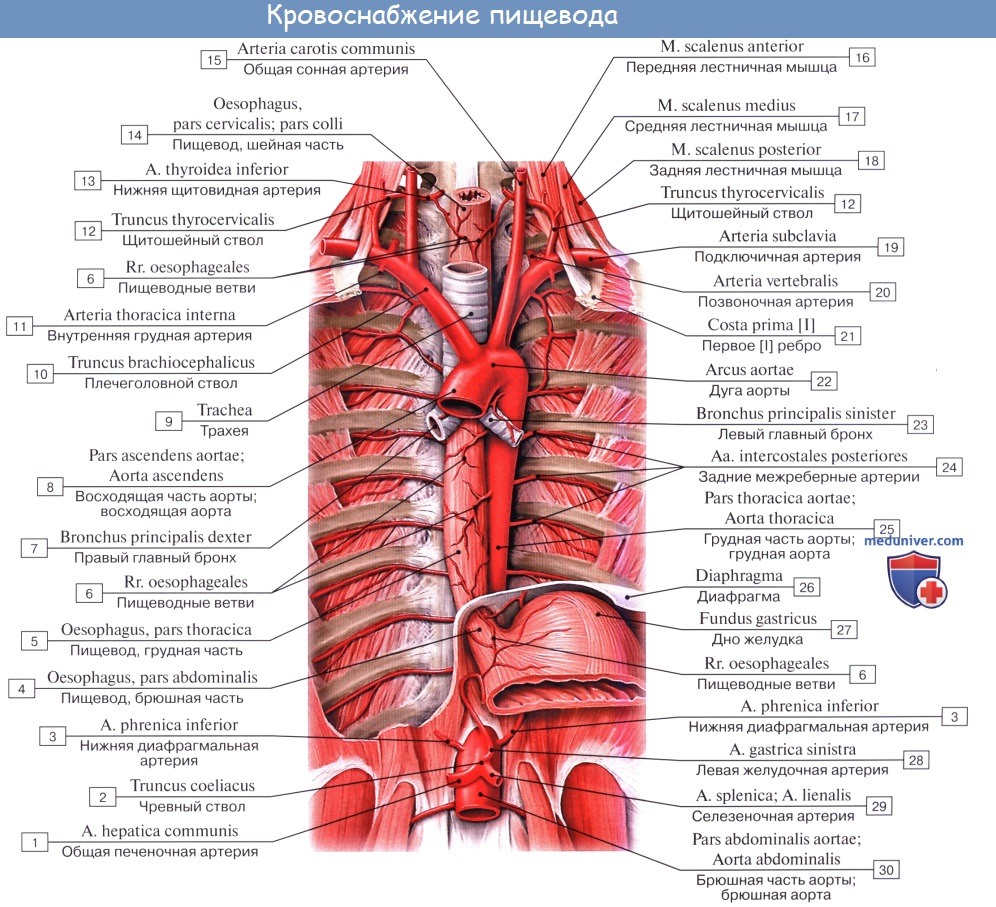
Питание пищевода осуществляется из нескольких источников, причем питающие его артерии образуют между собой обильные анастомозы. Аа. esophageae к pars cervicalis пищевода происходят из a. thyroidea inferior. Pars thoracica получает несколько веточек непосредственно из aorta thoracica, pars abdominalis питается из аа. phrenicae inferiores et gastrica sinistra. Венозный отток из шейной части пищевода происходит в v. brachiocephalica, из грудного отдела — в vv. azygos et hemiazygos, из брюшного — в притоки воротной вены.
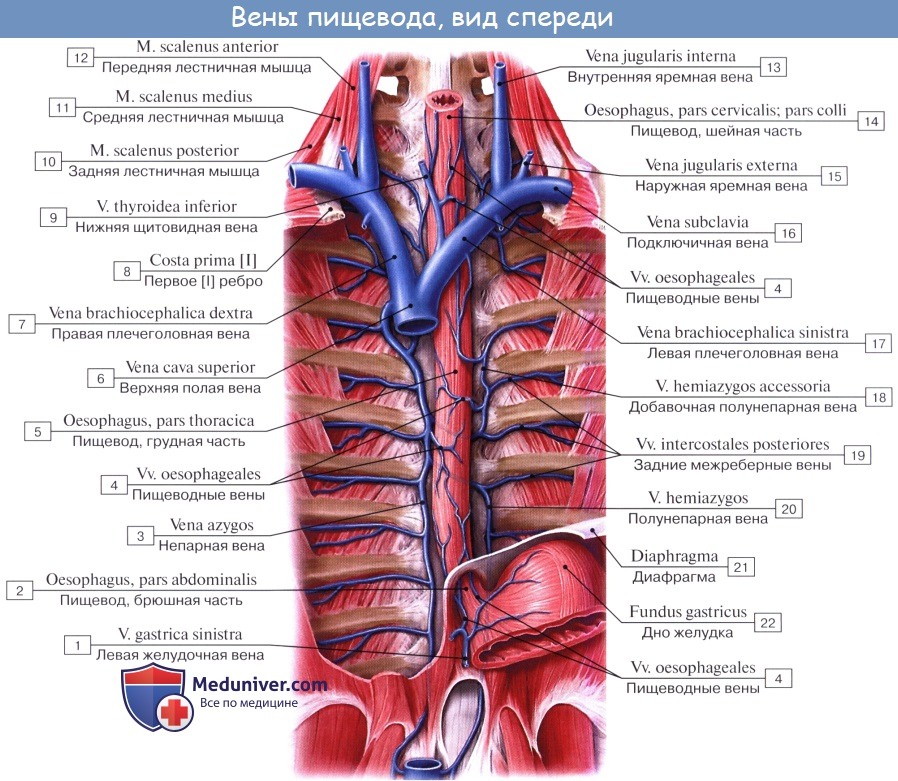
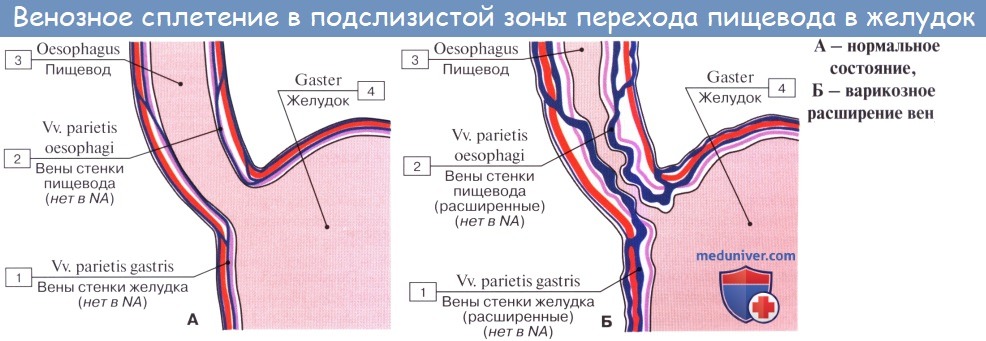
От шейного и верхней трети грудного отдела пищевода лимфатические сосуды идут к глубоким шейным узлам, предтрахеальным и паратрахеальным, трахеобронхиальным и задним средостенным узлам. От средней трети грудного отдела восходящие сосуды достигают названных узлов грудной клетки и шеи, а нисходящие (через hiatus esophageus) — узлов брюшной полости: желудочных, пилорических и панкреато дуоденальных. В названные узлы впадают сосуды, идущие и от остальной части пищевода (наддиафрагмального и брюшного отделов его).
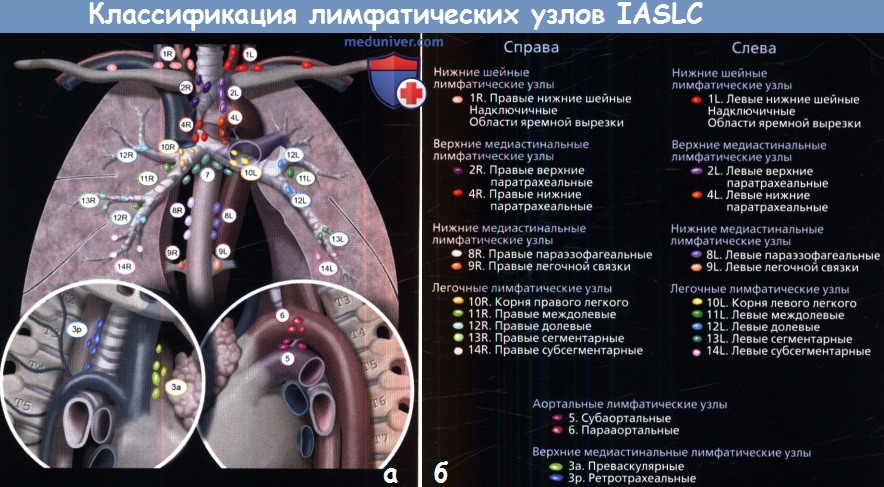
а - На рисунке изображены группы лимфатических узлов, поражение которых типично при раке легких.
Карта их расположения составлена Международной Ассоциацией по изучению рака легких (IASCL).
б - Обозначения групп определенных лимфатических узлов, входящих в классификацию лимфатических узлов (IASLC) и изображенных на соседнем рисунке. 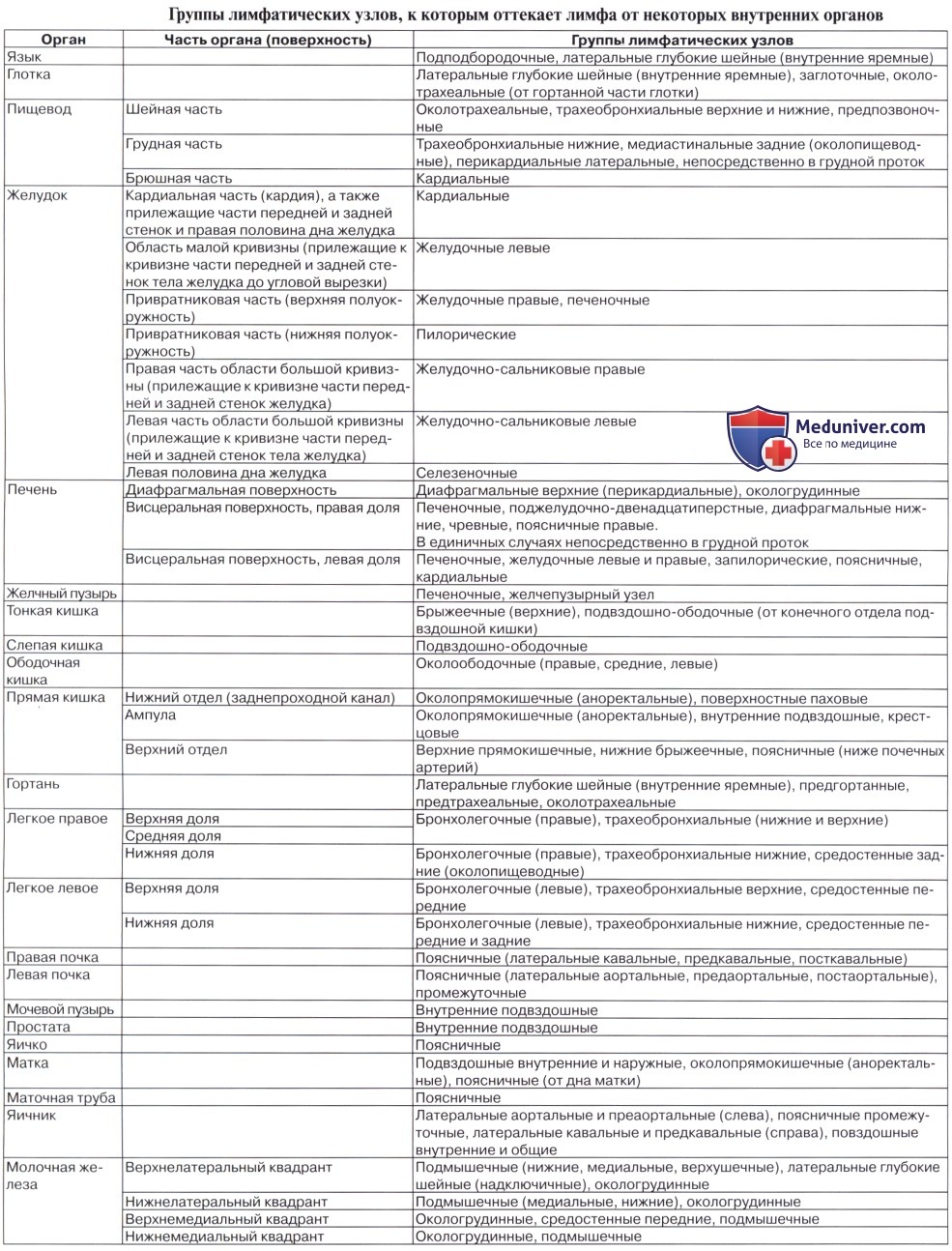
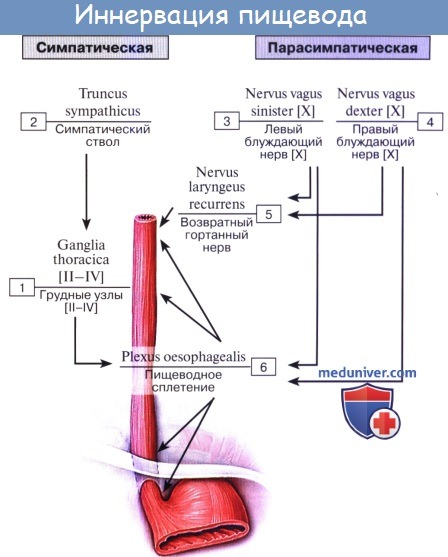
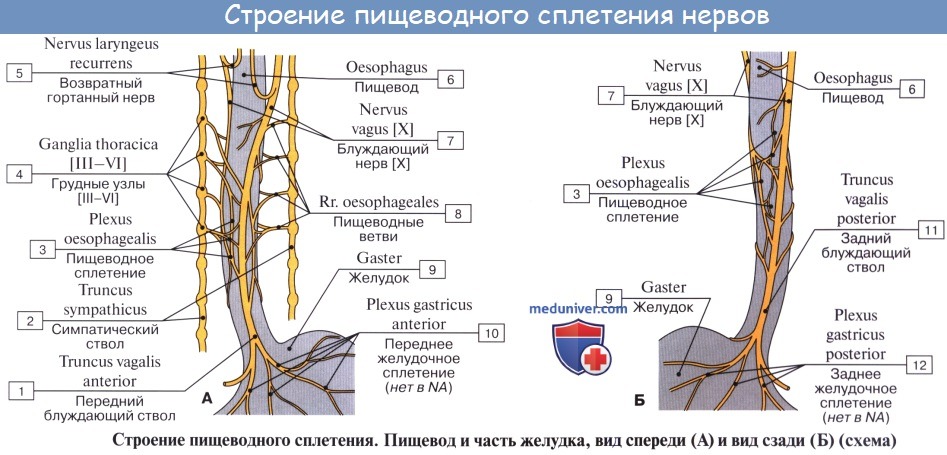
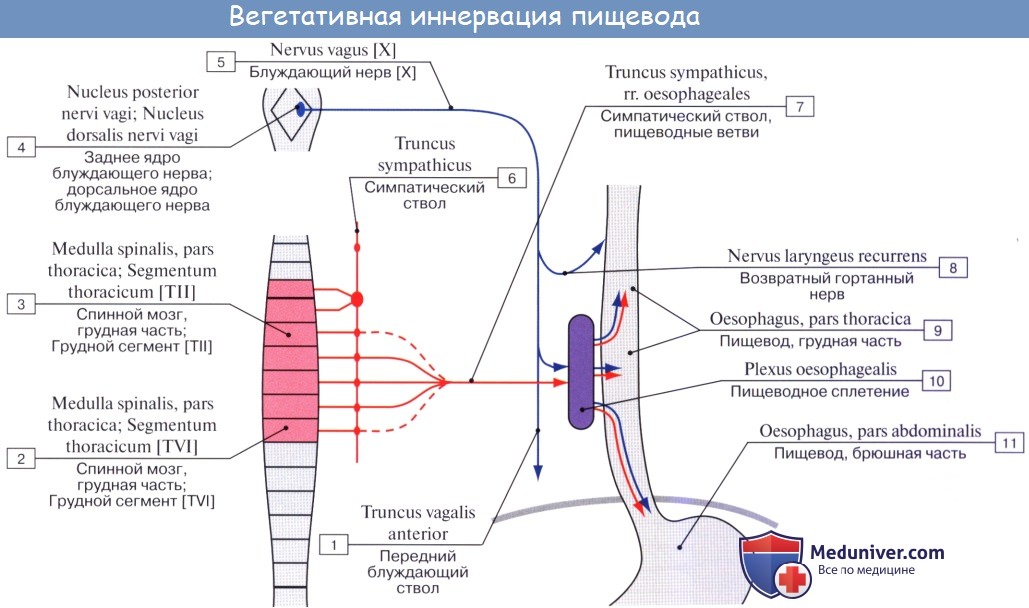
Иннервируется пищевод из n. vagus et tr. sympathicus.
По ветвям tr. sympathicus передается чувство боли; симпатическая иннервация уменьшает перистальтику пищевода. Парасимпатическая иннервация усиливает перистальтику и секрецию желез.
Учебное видео по анатомии пищевода и его сужений
Учебное видео оценки рентгенограмм органов желудочно-кишечного тракта
Редактор: Искандер Милевски. Дата последнего обновления публикации: 19.8.2020

Актуальная проблема
Для большинства людей, изжога – это просто случайно возникший дискомфорт. Примерно 20% населения высокоразвитых стран испытывают ее не реже одного раза в месяц.
Но для 6% людей, которые имеют хроническую форму изжоги, известную как гастроэзофагеальная рефлюксная болезнь (ГЭРБ), не купированные (не леченные) симптомы могут привести к различным осложнениям для здоровья. Люди с эрозиями на слизистой пищевода из-за кислого рефлюкса часто не осознают вреда от ГЭРБ, пока у них не разовьется запущенная стадия болезни.
Если вы испытываете частую или длительную изжогу (два раза в неделю на регулярной основе), обратитесь к врачу. Вот девять причин, почему Вы не должны игнорировать симптомы гастроэзофагеальной рефлюксной болезни.
1. Развитие воспаление в пищеводе (эзофагит)
При гастроэзофагеальной рефлюксной болезни пища, кислота и пищеварительные соки забрасываются в пищевод. Со временем это вызывает раздражение и отек слизистой, выстилающей пищевод изнутри. Это и есть эзофагит. Если кислотное воздействие в пищеводе наблюдается в течение всего лишь нескольких недель, то уже может развить воспаление слизистой. Это может вызывать дискомфорт и, даже боль, по срединной линии брюшной стенки, «под ложечкой», где сходятся правые и левые ребра у грудины. Это воспаление делает пищевод уязвимым для еще более опасных состояний – эрозий или рубцов.
2. Стриктура пищевода
Если эзофагит продолжается слишком долго, то возникающая рубцовая ткань, может сузить пищевод. Это стриктура может привести к трудностям прохождения и глотания пищи, которая может застревать на уровне образования рубцовой ткани, вызывая боль.
Большие куски пищи могут застрять и эта ситуация может потребовать эндоскопического вмешательства для их удаления. Стриктура может вызывать частые подавливания при приеме пищи. Из-за этого пациенты часто отказываются от еды и теряют много в весе.
Стриктура лечится расширением или растяжением пищевода (бужирование или дилятация). Эти лечебные процедуры могут быть неоднократными по воздействию на стрикутуру. Но прием блокаторов продукции кислоты в желудке (ингибиторы протонной помпы, ИПП или Н2-блокаторы) могут помешать возвращению рубцовых изменений в пищеводе в дальнейшем.
3. Проблемы с горлом и голосом
Основным симптомом гастроэзофагеальной рефлюксной болезни является изжога, но не все люди ее чувствуют и описывают. У них могут быть другие, более сложные для диагностики симптомы. Врачи называют эти случаи «немой рефлюкс», или бессимптомный рефлюкс. У пациента может не быть изжоги, как это классически описано в учебниках, но у них могут быть различные другие проблемы, которые происходят за пределами пищевода, такие как хрипота, изменения голоса, боль в горле или хронический кашель. У них такое ощущение, как будто в горле комок или волос, и им постоянно приходится очищать горло, покашливая и откашливаясь.
4. Проблемы с дыханием
Если кислота желудка случайно затечет в дыхательное горло после того, как она попадет при гастроэзофагеальной рефлюксной болезни в пищевод, то ГЭРБ может ухудшить течение бронхиальной астмы или пневмонии. Даже без проблем с легкими ГЭРБ может вызывать одышку и затруднение дыхания. А лечение в данной ситуации может быть обоюдоострым мечом. Так как, препараты ГЭРБ, такие как ингибиторы протонной помпы, могут фактически увеличить риск пневмонии. (Они могут способствовать росту бактерий и подавлять кашель, который призван на помощь для очищения легких).
Обращайте внимание Вашего лечащего врача на функцию Ваших легких при лечении рефлюкса.
5. Разрушение зубов
Когда желудочная кислота и пищеварительные соки попадают через пищевод в ротовую полость, это может вызвать кислый вкус и, если это происходит достаточно часто, то разрушается зубная эмаль, что способствуют кариесу.
6. Язвы пищевода
Желудочная кислота может разрушать слизистую пищевода, вызывая раны и язвы. Язвы пищевода отличаются от язв желудка, которые обычно вызваны бактериями. Люди с ранами и язвами могут сплевывать кровью, у них также может быть рвота кровью. Они могут увидеть кровь в своих испражнениях. Кровь может быть красной, вишневой, или как частицы кофе. В стуле обычно кровь из пищевода и желудка при прохождении через тонкий кишечник приобретает черный цвет, цвет и вид нефти — вязкой, скользкой, плохо смываемой.
Обратитесь к врачу немедленно, если у Вас имеются такие симптомы. При эндоскопии можно обнаружить язвы пищевода. Кислотно-блокирующие или кислотно-снижающие лекарства могут привести к их исчезновению.
7. Пищевод Барретта
Если не лечить в течение многих лет, постоянный кислотный рефлюкс могут образоваться изменения в клетках, известное как пищевод Барретта, считающееся предраковым состоянием. Это состояние не вызывает особых симптомов, кроме симптомов рефлюкса. Врач может диагностировать его, выполняя эндоскопию.
Если у вас есть изжога более двух раз в неделю в течение длительного времени, или если у вас есть симптомы гастроэзофагеальной рефлюксной болезни, которые ухудшаются или вы обнаружили новые, которых у вас не было раньше, это все причины, чтобы провериться и пройти эндоскопию.
8. Рак пищевода
В очень серьезных случаях не леченая гастроэзофагеальная рефлюксная болезнь (и последующий пищевод Барретта) может привести к раку пищевода. Основные факторы риска – это употребление алкоголя, курение, плохое питание, а также хронические заболевания пищевода с рефлюксом.
Симптомы включают потерю веса, проблемы с глотанием, или желудочно-кишечные кровотечения. Это то, что происходит в течение десятилетий не леченного рефлюкса (30-40 лет), поэтому у тех, кому 30 лет и в остальном здоровы, нет причин подозревать рак. Но если вам больше 50 лет, и у вас была изжога в течение многих лет, и вы внезапно теряете вес, например, это определенно то, что врач заподозрит в первую очередь.
9. Более низкое качество жизни
В дополнение к рискам для здоровья, симптомы гастроэзофагеальной рефлюксной болезни могут повлиять на здоровье и качество жизни, которые могут быть подорваны из-за проблем с питанием и сном, а также социальных и физических ограничений. У мужчин отчетливо снижалось либидо при длительном рефлюксе.
Европейская клиникаРак пищевода встречается нечасто, ежегодно поражает чуть более 7,5 тысяч россиян или 8–9 человек из 100 тысяч населения, преимущественно пожилого возраста. Самые высокие показатели, двадцатикратно превышающие российские, отмечены в Китае, Корее, Японии, Монголии, Иране и Бразилии.
В структуре мужской онкологической заболеваемости рак пищевода взял 2, 5%, тогда как среди женских раков — только 0,5%. Это совсем не женское заболевание, мужчины болеют почти в четыре раза чаще и начинают болеть раньше. В мужской когорте средний возраст выявления онкологического поражения пищевода 64 года, то в женской — после 70 лет.
- Факторы риска
- Клиническая картина
- Диагностика
- Лечение рака пищевода
- Паллиативное лечение распространённого рака пищевода
Факторы риска
Рак пищевода одна из самых скрытно текущих опухолей, поскольку пищеводная трубка достаточно растяжима и даёт знать о неблагополучии при сужении просвета более чем на две трети. Пациенты обращаются к врачу, когда может просочиться только вода. При эндоскопическом исследовании желудка пищевод «пролетают», планируя осмотр слизистой желудка в плане диспансеризации или контроль хронической язвы желудка, и если не иметь намерения что-то прицельно найти в пищеводе, то походя ничего и не обнаружат.
Есть ещё одна проблема — проблема личности. Для жителей Средней Азии, пьющих обжигающий чай, рак пищевода — традиционная болезнь. Злокачественная опухоль пищевода поражает пьющих крепкие алкогольные напитки, курящих, потребляющих некачественную пищу. Не минует рак пищевода и граждан с избыточным весом.
Также вероятность развития злокачественного новообразования повышает наличие грыжи пищеводного отверстия диафрагмы при которой происходит заброс желудочного содержимого в неприспособленный для такой агрессивной среды пищевод. Регулярно «обжигаемый» соляной кислотой пищевод даёт знать о себе гастро-эзофагеальной рефлюксной болезнью, коротко именуемой ГЭРБ.
Второе заболевание, с довольно высокой частотой приводящее к развитию аденокарциномы пищевода — пищевод Барретта. При пищеводе Барретта нормальный природный плоский эпителий слизистой оболочки в месте перехода в желудок локально, буквально гнёздами, замещается нетрадиционным цилиндрическим эпителием, такое состояние частичной замены называется метаплазией. И то воздействие различных жизненных факторов, которое легко переносит плоский эпителий, совершенно не подходит цилиндрическому, он страдает и сбивается с курса, давая рост раковым клеткам. Все больные пищеводом Барретта должны наблюдаться и лечиться, во избежание развития рака.
Эти факторы риска развития рака пищевода устранимы. Но есть и неустранимый — ахалазия пищевода, двадцатикратно увеличивающая вероятность рака. Заболевание обусловлено ненормальным регулированием нервной системой сокращений пищевода при передвижении по нему пищи и правильного открытия сфинктера у входа в желудок. Пищевод сужается циркулярными рубцами, а над сужением возникает чрезмерное расширение. Особенность в том, что твёрдая пища проходит легко, а вот жидкая — плохо. При этом состоянии пища проходит очень плохо, подолгу застаиваясь в расширении и формируя хроническое воспаление слизистой оболочки. При воспалении начинается избыточное деление клеток эпителия слизистой, и сбой одной клетки с правильной программы может дать начало раку.
Клиническая картина
В пищеводе есть физиологические сужения, где преимущественно и начинается злокачественный рост. Сужения эти обусловлены прохождением вблизи других анатомических образований — аорты и развилки трахеи на бронхи, в местах перехода глотки в пищевод и пищевода в желудок тоже имеется небольшое сужение. Считается, что здесь слизистая более подвержена мелким травмам грубой пищей, значит, чаще возникает воспаление. Тем не менее, в шейном отдела частота рака составляет 10%, в нижней трети пищевода — 30%, а 60% раков образуется в среднем сегменте.
Злокачественные клетки не только растут в толщу органа, как бывает при большинстве раковых образований, они ещё и мигрируют по мелким лимфатическим сосудикам. Сосудики формируют внутри пищеводной стенки полноценную лимфатическую сеть, распространяя опухоль внутри, поэтому протяжённость опухоли может быть и 5, и 10, и 15 сантиметров.
В запущенной стадии локализация определяет симптоматику, а первыми признаками считается ощущение прилипания пищи к одному и тому же месту или царапание слизистой кусочком еды. По мере прогрессирования появляется затруднённое прохождение сначала твёрдых кусочков, потом каши, далее жидкости. Всё этот называется дисфагия. Сначала пациент запивает кусочки еды водой, проталкивая их, после это уже не помогает, нарушается питание, человек худеет. Соприкосновение опухоли с пищей приводит к воспалению, появляется неприятный гнилостный запах, при регулярной травме рыхлая слизистая опухоли начинает кровоточить, может развиться опасное для жизни кровотечение.
Присоединяются боли, поскольку пищевод сокращается перистальтическими волнами, боль имеет спастический характер. Прорастание опухоли через всю толщу пищеводной стенки делает боль постоянной, локализуется она между лопатками. Инфильтрация опухолью клетчатки средостения вовлекает в процесс возвратный нерв, отвечающий за движение голосовых связок, появляется осиплость и попёрхивание при питье. Нерв могут сдавить увеличенные метастазами лимфатические узлы и пропадёт звучность голоса.
Как и при ахалазии, над сужением пищевода опухолью образуется расширение, где копится еда. Ночной заброс скопившихся пищевых масс в дыхательное горло тоже может привести к пневмонии. А днём беспокоит сильная слабость, температура. Если в процесс вовлечены дыхательные пути, то может сформироваться соустье между пищеводом и трахеей или крупными бронхами — свищ, по которому крошки еды будут попадать в дыхательную трубку, вызывая кашель и пневмонию. Если такой свищ откроется из пищевода в клетчатку средостение, то её воспаление приведёт к смерти.
Диагностика
Современная диагностика, сделавшая с конца прошлого века рывок в развитии, активному выявлению опухоли пищевода помогает мало, только у 6,4% из всех заболевших опухоль находят до появления ярких клинических признаков. Как и в докомпьютерную медицинскую эру рак пищевода на I–II стадии выявляют только у 28,2%, на III стадии — у 36,4%, и треть попадает к доктору уже с отдалёнными метастазами. По причине запущенности 60% больных с момента выявления рака не проживут и года, а 5 лет проживают только 32,3%.
Статистические показатели у россиян хуже только при раке печени и поджелудочной железы, действительно высокозлокачественных опухолях с весьма высоким метастатическим потенциалом. По степени злокачественности рак пищевода отнюдь не под стать им, просто у 73% рак выявляется в распространённом варианте, когда возможности терапии ограничены сугубо паллиативной помощью.
Лечение рака пищевода
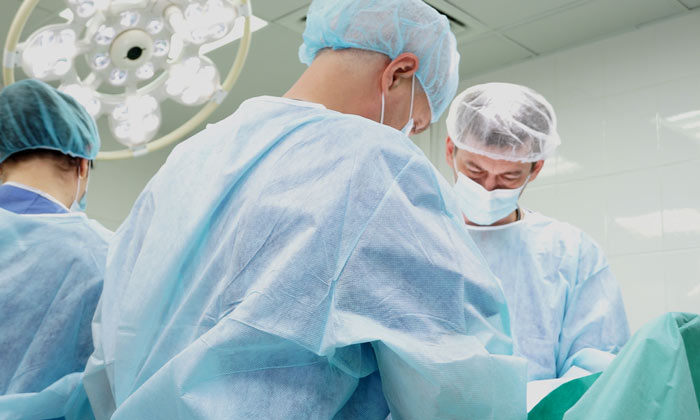
Главный и основной метод терапии — хирургия, но выявление опухоли в запущенном состоянии при невозможности замены всей пищеводной трубки аналогичной анатомической структурой — техническое ограничение хирургических возможностей, не всегда даёт желаемый результат. Поэтому к операции подключают лекарственную и лучевую терапии. Выбор ведущего метода лечения диктуется размерами и локализацией опухоли, состоянием больного и сопутствующими заболеваниями.
- При очень небольшой опухоли, не прорастающей слизистую, выполняют резекцию только слизистой с подлежащим слоем с помощью гастроскопа, и результаты лечения очень хорошие.
- При I‑II стадии рака часть пищевода удаляется, дефект заполняют сегментом кишки или формируют трубку из желудка. Сегодня возможно использовать эндоскопическое оборудование при этих операциях.
- При распространении опухоли в мышечный слой и далее тоже делается операция, но в этом случае результаты не очень хороши, поэтому её дополняют предоперационной химиотерапией или облучением. В некоторых случаях, когда невозможно радикально удалить опухоль, ограничиваются химиолучевой терапией.
- Предоперационная химиотерапия максимальный выигрыш даёт при аденокарциноме, в некоторых случаях проводят несколько курсов до операции и несколько после.
- Профилактическую терапию после радикальной операции не проводят из-за малой эффективности.
- Без химиотерапии эффективность лучевой терапии тоже невысока, методы лучше совмещать, тогда операцию делают через 6–8 недель после завершения консервативного лечения, такой комплексный подход позволяет прожить 5 лет ещё 13% больных.
- Иногда химиолучевое лечение проводят при недостаточной радикальности операции.
- Химиолучевое лечение может проводиться при невозможности операции, когда опухоль слишком большая, или при маленькой опухоли, но с общими противопоказаниями к операциям. В этом консервативном варианте выживаемость сравнима с хирургическим лечением.
- При наличии свищей химиолучевое лечение невозможно.
- Химиолучевое лечение может осложниться острым воспалением слизистой пищевода, которое потребует перевода на питание «через капельницу».
В онкологической гастроэнтерологии для восстановления просвета пищевода часто используется стентирование. Это решает серьезные задачи, не прибегая к «большой хирургии», малоинвазивным способом.

Паллиативное лечение распространённого рака пищевода
В этой ситуации на передний план выходит полная невозможность питания через практически закрытый опухолью пищевод. Часто прибегают к расширению — реканализации или установке специального стента в пищеводе. Стенты обязательны при соединении пищевода и трахеи или бронхов соустьем — опухолевым свищом, что предотвращает заброс пищи в дыхательное дерево и уберегает от пневмонии. В некоторых случаях во время эндоскопии опухоль частично разрушают лазером, используя фотодинамическую терапию. Вариантов лечения рака пищевода достаточно, надо вовремя и умело их использовать.
Читайте также:

