Повышен креатинин и мочевина у кота лечение
Опубликовано: 15.05.2024
Когда фиксируется повышенный креатинин у кота, то это может сигнализировать о почечной недостаточности и других патологических состояниях, угрожающих здоровью и жизни питомца. Высокий уровень конечного продукта креатин-фосфатной реакции сопровождается постоянной жаждой и слабостью у кошки в мышцах. При выявлении первых патологических признаков, стоит показать животное ветеринару, который подберет лечение для снижения креатина.
Что собой представляет и какова норма у котов?
При азотном обмене в кошачьем организме образуются конечные продукты, в частности, креатинин. У здорового питомца он выходит наружу вместе с уриной, если же происходят какие-то патологические изменения, то его уровень в крови повышается. Креатинин формируется из креатинового белка, служащего питательным веществом для скелетной мускулатуры. При нормальном сокращении волокон мышц происходит распад компонентов на креатинин, воду и фосфор. В дальнейшем продукты выходят через почки и мочевыводящую систему.
Врачи-ветеринары утверждают, что средняя суточная норма креатинина у молодых и активных котов выше, нежели у взрослых и малоподвижных особей.
Норма креатинина у кошек находится в пределах 40—130 мкмоль/литр. При лабораторных исследованиях крови показатели могут отклоняться в сторону увеличения либо снижения. Это не всегда свидетельствует о патологии, при условии, что домашнее животное себя хорошо чувствует. На искажение результатов способны повлиять следующие факторы:

Если у питомца есть лишний вес, то этот фактор может сказаться на результате исследования.
- проблемы с лишним весом;
- нехватка энергетических либо пластических компонентов в кошачьем организме;
- слишком молодой или зрелый возраст питомца;
- диетическое питание, при котором коту поступает мало белка.
Почему возникают проблемы?
Причины повышения
В большинстве случаев высокая концентрация креатинина в крови кота говорит о хронической почечной недостаточности (ХПН). Завышенный уровень также порой свидетельствует о нефропатии разного типа. Установить окончательный диагноз и подобрать оптимальные методы лечения может только ветеринар после лабораторной диагностики. Если причиной повышенного креатинина выступает ХПН, то также в крови возрастает мочевина и ее азот. Также проблема бывает вызвана сильным обезвоживанием кошачьего организма, вследствие чего повышается и уровень плотности урины. Распознать повышение креатинина и мочевины удается по следующим симптомам:
- слабость и вялое поведение;
- бледные видимые слизистые оболочки;
- рвотные позывы и тошнота;
- нежелание принимать пищу;
- резкое снижение количества выведения урины, при этом кот может за день помочиться только раз;
- неприятный запах из ротовой полости питомца.
Почему показатель бывает снижен?

Если питомец испытывает сильную жажду, то величина показателя может опускаться ниже нормы.
Не всегда кота тревожит креатинин больше нормы, порой его уровень существенно снижается, что также негативно сказывается на самочувствии питомца. Нарушение в большей степени связано с сильным истощением. Выделяют и другие причины, сказывающиеся на патологическом снижении креатинина в крови у кота:
- увеличенное скопление урины;
- пониженная мышечная масса;
- сильная и неутолимая жажда.
Диагностические мероприятия
Повышенный креатинин в крови кота не стоит пытаться самостоятельно снижать, поскольку можно спровоцировать серьезные осложнения. При этом домашнее решение проблемы может быть безрезультативным, поскольку не выяснив причины патологии, повлиять на нее не удается. При первых тревожных симптомах обращаются с домашним животным в ветеринарную клинику. Сам по себе креатинин не представляет опасности, но он свидетельствует о прогрессировании серьезного заболевания, которое требуется как можно скорее лечить. Для подтверждения диагноза требуется провести лабораторное исследование цельной крови, сыворотки либо плазмы. Способы диагностики выбирает ветеринар. Забор материала проводится круглосуточно. Если у кота имеется почечная недостаточность или другие болезни со стороны мочевыделительной системы, то в крови специалисты обнаруживают мочевину и повышенный креатинин.
Необходимое лечение
В некоторых случаях оправдано проведение диализа животному.
Если показатель был завышен только один раз, при этом состояние питомца в норме, то не стоит тревожиться. В подобном случае нарушение вскоре проходит самостоятельно и не требуется никакого особого лечения. Когда же креатинин в крови у кошек постоянно выше нормальных значений, то стоит проконсультироваться с ветеринаром. После комплексного обследования и выяснения источника проблемы специалист подскажет, как снизить концентрацию вещества и стабилизировать состояние домашнего животного. В большинстве случаев измененные показатели спровоцированы почечной недостаточностью, протекающей в острой либо хронической форме. Заболевание требуется как можно скорее лечить, поскольку происходит сильная интоксикация кошачьего организма, которая может привести к преждевременной гибели. Ветеринар при обострении недостаточности почек у кота принимает решение о проведении диализа, посредством которого удается вывести токсические вещества. Процедура выполняется следующим образом:
- Выполняется разрез на брюшной стенке.
- Вставляют трубку, содержащую особую жидкость.
- При манипуляции токсические вещества переходят в раствор и выводятся из организма питомца.
Если уровень креатинина превышает норму из-за острого течения почечной недостаточности, то диализ проводится лишь при серьезном нарушении электролитного баланса.
Медикаментозная терапия
Эритропоэтин врач назначает животному в случае низкого уровня гемоглобина в крови.
Сложнее поддается лечению хроническая форма заболевания, при которой мочевыводящая система длительное время функционирует неправильным образом. Такой тип болезни не поддается полному излечению. Ветеринар назначает медикаментозную терапию, с помощью которой удается понизить креатинин и устранить другие неприятные симптомы на время. Коту требуется пожизненно принимать лекарства. Нередко назначается введение «Эритропоэтина» если снижена концентрация гемоглобина. При развитии ацидоза на фоне ХПН прописывается гидрокарбонат натрия. Помимо лекарств коту требуется соблюдать определенную диету, при которой рекомендованы специальные корма, предназначенные для животных с нарушенной почечной функцией.
Профилактика
Чтобы креатинин в крови у кота не повышался, рекомендуется регулярно следить за его здоровьем. Важно правильно и сбалансировано кормить питомца, не позволяя ему употреблять острую, жирную и жареную пищу. Рацион домашнего животного должен быть разнообразным и содержать много витаминов и микроэлементов. Если хозяева решили кормить кота сухими кормами, то требуется выбирать их тщательно, при этом не экономить, поскольку в дешевых вариантах содержится много красителей и других вредных компонентов, которые могут привести к нарушенной функции почек. Снизить вероятность развития почечной недостаточности, сопровождающейся высоким содержанием креатинина, помогает регулярное обследование домашнего животного у ветеринара. Стоит проводить профилактический осмотр кота минимум 1 раз в год, а если питомцу более 10 лет, то рекомендуется посещать специалиста единожды в полгода.
Хроническая почечная недостаточность (ХПН) видимое клиническое проявление нарушения функции почек, вызванное необратимой гибелью нефронов при прогрессирующем заболевании почек. Это обычно наблюдается при потере 75% функциональной массы почек и проявляется многосимптомным комплексом, отражающим участие в этом процессе практически всех органов и систем больного животного. В ретроспективных исследованиях, где преобладали кошки старше 7 лет, не было выявлено ни половой ни породной предрасположенности [1].
Хроническая почечная недостаточность (ХПН)
В опыте нашего ветеринарного центра подтверждаются данные приведенные Di Bartola. Среди наших пациентов также преобладали животные старше 7 лет, самцы и самки встречались с одинаковой периодичностью.

В ветеринарных клиниках кошек с ХПН среди всех пациентов от 10 до 30% [3]. В нашей клинике кошек с ХПН на терапевтическом отделении порядка 28-30% от общего количества пациентов.
Этиология
ХПН развивается там, где есть давние, необратимые повреждения почек, вследствие чего они теряют свою экскреторную (выведение продуктов обмена), регулирующую (поддержка объема и состава жидкости в организме) и эндокринную функции (выработка гормонов ренина, эритропоэтина и др.).
Причинами ХПН являются первичные или вторичные ренальные процессы, которые, как правило, продолжаются длительное время и приводят к конечной стадии – сморщенной почке. Такие как:
- поликистоз почек (наследственное заболевание, в основном у персидских и экзотических кошек),
- воспалительные заболевания почек (пиелонефрит, гломерулонефрит),
- болезни обмена веществ (сахарный диабет кошек и собак, амилоидоз),
- мочекаменная болезнь,
- врожденное недоразвитие почек (гипоплазия)
- опухоли почки - например, лимфома,
- другие причины - например, повреждение почек токсинами.
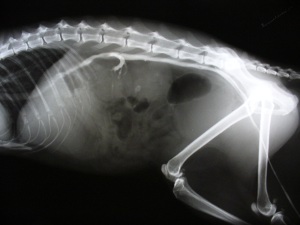
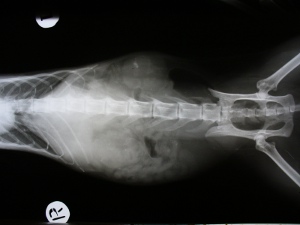
На фото: Поликистоз почек, болезни почек у кошек. Исследование контрастным веществом Омнипак 300.
Однако, в большинстве случаев, точная причина заболевания кошек неизвестна.
Патогенез
В патогенезе ХПН, независимо от почечной патологии, снижение почечных функций происходит за счет 3-х основных механизмов:
- уменьшения количества функционирующих нефронов,
- значительного снижения скорости фильтрации в каждом отдельном случае без уменьшения числа нефронов,
- сочетания первого и второго механизмов.
Следствием действия каждого из этих факторов будет снижение скорости клубочковой фильтрации - скорость, с которой происходит фильтрация веществ из крови через клубочки нефронов. Уменьшение числа функционирующих нефронов постепенно приводит к существенному изменению биохимических показателей крови и тяжелым обменным нарушениям.
Отмечается развитие уремии с накоплением потенциальных токсинов и продуктов метаболизма белков: мочевины (более 10 ммольл [2]), креатинина (более179 ммольл [3]), мочевой кислоты.
По современным представлениям синдром уремической интоксикации обусловлен не задержкой азотистых шлаков, а главным образом накоплением в крови средних молекул - белковых веществ, имеющих молекулярную массу от 300 до 500 дальтон, образующихся в результате нарушения гомеостатической функции почек [5].
Повышение в крови продуктов азотистого метаболизма - осмотически активных веществ - увеличивает осмотическую нагрузку на оставшиеся нефроны. Эти вещества, профильтровавшись в клубочках, в меньшей мере, чем в норме, реабсорбируются в канальцах. Нереабсорбировавшаяся часть их выделяется с мочой вместе с соответствующим количеством воды. Это называется осмотическим диурезом. За счет осмотического диуреза общее выделение почками воды не только сохраняется нормальным, но даже может быть увеличенным (полиурия), несмотря на значительное снижение клубочковой фильтрации. Плотность мочи при этом снижается и становится стабильной на уровне 1,008—1,015, что соответствует плотности крови и указывает на снижение концентрационной способности почек.
Полиурия приводит к потере организмом воды (дегидратация). При дегидратации снижается почечный кровоток, ухудшается клубочковая фильтрация и усугубляется ХПН. При ХПН нарушается метаболизм кальция и фосфора. По мере прогрессирования ХПН падают выделение кальция с мочой и его всасывание в кишечнике, содержание фосфатов в крови повышается. Указанные нарушения сопровождаются изменениями в костной ткани — остеодистрофией. Нарушения обмена электролитов приводят к изменениям в нейромышечной системе, сопровождающимся адинамией, параличами и другими нарушениями. ХПН сопровождается изменениями во всех видах обмена веществ. На ранних стадиях нарушается энергетический обмен -расходование энергии превышает возможности энергообразования.
Стадии почечной недостаточности кошек
1. Латентная стадия заболевания почек (ранняя).
Характеризуется снижением скорости клубочковой фильтрации, однако это не сказывается на общем состоянии животного и концентрации креатинина в крови
2. Начальная стадия ХПН.
Наблюдается умеренная азотемия, концентрация креатинина в сыворотке крови - до 250 мкмоль/л. Прогрессирование данной стадии заболевания может длиться несколько месяцев, сопровождается снижением аппетита, потерей массы тела, периодической рвотой. Компенсация может вызвать гиперпаратиреоидизм, снижение концентрационной способности почек.
3. Консервативная стадия ХПН.
Происходит дальнейшее снижение скорости клубочковой фильтрации, развивается высокая уремия, концентрация креатинина в сыворотке крови составляет 252 - 440 мкмоль/л. На данной стадии характерна полидипсия, возможно появление клинических признаков обезвоживания анемии, нарушения работы ЖКТ, метаболический ацидоз.
4. Терминальная стадия ХПН.
О терминальной стадии ХПН свидетельствуют не только высокие показатели мочевины и креатинина в крови, но и гипокальциемия (вплоть до развития судорог), симптомы уремической энцефалопатии, гиперфосфатемия, картина декомпенсированного уремического ацидоза (дыхание Куссмауля), интерстициальный отек легких. При длительной тяжелой азотемии жизнь невозможна без диализа или трансплантации почки [2].
По данным Douglas Slatter есть 3 фазы почечной недостаточности.
1 фаза. Заболевания почек, которые первично повреждают почечную ткань (гломерулонефрит, мочекаменная болезнь, гипертензия). Не оказывает существенного влияния на жизнь животного и не сказывается на концентрации креатинина в крови.
2 фаза. Почечная недостаточность с незначительными клиническими проявлениями. Уровень креатинина 179 – 354 мкмольл.
3 фаза. Уремия, с явными клиническими проявлениями и креатинином крови свыше 354 мкмольл.
В нашей практике мы условно разделили ХПН на три стадии по уровню креатинина в крови:
1. Начальная стадия - когда уровень креатинина не поднимается выше 250 мкмольл – при этом у таких животных может не быть никаких клинических проявлений болезни, или они незначительны. Таких кошек за последний год было 38% (от общего количества кошек страдающих ХПН).
2. Средняя – уровень креатинина крови до 500 мкмольл. Имеются явные клинические признаки заболевания (полиурия, полидипсия, нарушение функции ЖКТ, анемия, истощение). Таких кошек около 28%.
3. Терминальная – уровень креатинина выше 500 мкмольл. Полный набор клинических признаков, вплоть до летаргии. Таких кошек от общего числа страдающих ХПН – 34%.
Клинические признаки
- Анорексия, подавленность
- Рвота обусловленная гиперацидным гастритом, полидипсия, полиурия. Гингивит с язвами на кончике языка. Анемичные слизистые оболочки. Наблюдается вторичный гиперпаратиреоз с размягчением костей лицевого черепа.
- Констипация, обезвоживание
- При пальпации можно обнаружить изменение размеров почек, чаще всего они уменьшены, если ХПН вызвана амилоидозом, гидронефрозом, опухолями – наблюдается увеличение почек.
- Уремическая энцефалопатия: кома, тремор, эпилептиформные припадки, тетеания.
- Аритмия брадикардия. Повышение артериального давления, гипертрофия левой половины сердца. Ацидоз вызывает углубление дыхания.
- Иммунная депрессия, обызвествление мягких тканей, нарушение свертываемости крови, резистентность к инсулину (повышение уровня глюкозы в крови), нарушение работы поджелудочной железы (гиперамилаземия). Истончение волоса, плохое качество шерсти.
- У кошек с терминальной стадией ХПН наблюдается летаргия.
Диагностика
ХПН можно диагностировать болезнь животного по клиническим симптомам, но они могут быть и неспецефическими, т.к. подавленность, летаргия, отсутствие аппетита и потеря веса наблюдаются при многих заболеваниях. Для подтверждения диагноза требуются лабораторные исследования. В нашей клинике мы используем чаще всего биохимический и клинический анализы крови и анализ мочи, во многих случаях проводим ультразвуковое исследование почек.
Определяются повышенный уровень мочевины, азота мочевины и креатинина. Определение креатинина в крови имеет большее значение, чем определение мочевины, т.к уровень креатинина не подвержен влиянию диеты или уровню расщепления белков.
Также можно определять скорость клубочковой фильтрации: определяют объем и концентрацию креатинина в моче за сутки и коррелируют с уровнем креатинина в сыворотке крови.
Симптомы отсутствия аппетита наблюдаются при уровне мочевины более 25 ммольл, при содержании мочевины 40 ммольл (норма 5-10 ммольл) у животного будут наблюдаться сильное угнетенение и анорексия.
Недостаточное выведение огранического фосфора приводит к подъему его уровня в крови, в то время как уровень кальция падает (при ХПН средней тяжести уровень фосора не более 2,1 ммольл, при тяжелой форме ХНП более 3,2 ммольл).
Высвобождение кальция из костей при высоком уровне фосфора приводит к минерализации мягких тканей. У большинства кошек с ХПН наблюдается гипонатриемия иили гипокалиемия, гипоальбуминемия, гиперамилаземия. Нерегеративная анемия, гипокалиемия. Изостенурия, плотность мочи 1008 и ниже.
Преобладает следующая картина: нерегенеративная анемия вызванная снижением производства почками эритропоэтина и уменьшением срока жизни циркулирующих эритроцитов, лейкоцитоз с лимфопенией и тромбопенией.
Изостенурия (осмоляронть обычно ниже 1015), рН изменяется в кислую сторону, протеинурия, неактивный мочевой осадок, редко глюкозурия.
Повышение эхогенности почечной паренхимы, размытость границ коркового и медиального слоя, уменьшение размеров почек.
Определяется уменьшение размеров почек менее 2,5 кратной длины тела второго поясничного позвонка (L-2). Если наблюдается явный гиперпаратиреодизм, то видно снижение плотности костей, особенно верхней челюсти и кальцификация мягких тканей.
Дифференциальный диагноз
Дифференцируют от острой почечной недостаточности (ОПН), преренальной и постренальной уремии.
При ОПН отсутствует анемия, полиурия и полидипсия, уменьшение почек, зато присутствуют анамнестические признаки экстраренального основного заболевания.
Гломерулонефрит сочетается с сильной протеинурией, при этом размеры почек в норме, тенденции к отекам.
При пиелонефрите в анализе мочи активный мочевой осадок, пиурия. Почки могут быть неправильной формы, расширение лоханки и мочеточников на УЗИ. Лейкоцитоз крови.
От полидипсии без задержки мочевины, Diabetes mellitus, Dibetes isipidus centralis and renalis, психогенной тяги к питью.
При гистопатологическом исследовании почек (биопсия) при ОПН наблюдается:
- острый некроз канальцев
- острое воспаление
- значительная часть нормальной паренхимы заменена фиброзной тканью,
- обширная атрофия канальцев,
- кальцификация базальных мембран,
- хроническое воспаление (хронический интерстициальный нефрит),
- гломерулосклероз
Лечение
Чаще всего болезни почек у кошек диагностируется без ясного представления о ее причине, поэтому лечение направлено на устранение основных симптомов. Цели проводимой терапии:
- поддержание качества жизни,
- замедление дегенерации поврежденных почек и прогрессирования ХПН,
- снижение азотемии,
- снижение протеинурии,
- снижение риска гипертензии.
Анорексия и обезвоживание: внутривенное или подкожное введение растворов 0,18% натрия хлорида + 4% декстрозы. Необходимый объем вводимых растворов рассчитывается из необходимости 50 млкг24 часа
Системная гипертензия: ингибиторы АПФ или блокаторы кальциевых каналов (эналаприл 0,25-0,5 мгкг per os, каждые 12-24 часа, амлодипин 0,10-0,25 мгкг per os, каждые 24 часа).
Метаболический ацидоз: бикарбонат натрия 8-15 мгкг per os, каждые 8-12 часов.
Гипокалиемия: раствор Хартмана, Панангин.
Гиперфосфатемия: диета с низким содержанием фосфора (Royal Canine renal, Hill’s kd, Eucanuba renal, Pro Plan NF), содержание фосфора не более 0,6% от суточного рациона. Введение препаратов связывающих фосфор в ЖКТ алюминия гидроксид 30-60 мгкг в сутки с кормом.
Потеря веса: высококалорийная диета, стимуляция аппетита различными привлекателями вкуса, парэнетеральное питание, носопищеводный зонд
Протеинурия и гипоальбумиемия: ингибиторы АПФ эналаприл 0,5 мгкг per os, каждые 12-24 часа – снижают экскрецию белка почками при их повреждении. Диета насыщенная омега 3- полиненасыщенными жирными кислотами.
Иммунная супрессия: ежегодная вакцинация и оберегание животного от потенциальных источников инфекции.
Снижение аппетита и рвота: диета со сниженным уровнем белка при уровне мочевины более 40 ммолл, антагонисты Н2 рецепторов (фамотидин 0,5 мгкг per os, каждые 12-24 часа, метоклопрамид 0,2-0,4 мгкг per os, подкожно, каждые 6-8 часов.
Анемия: при гематокрите ниже 18% эритропоэтин 25-100 едкг, подкожно 1-3 раза в неделю, сульфат железа 5-20 мгкг в сутки per os.
Выводы
1) ХПН –это необратимая прогрессирующая деструкция ткани почек в результате заболеваний, которые в отсутствие диализа или трансплантации почки приводят к смерти пациента.
2) У кошек с ХПН симптомы могут отсутствовать до тех пор, пока скорость гклубочковой фильтрации не станет очень низкой.
3) Следствием ХПН является нарушение метаболизма воды и натрия, кальция и фосфора, анемия.
Диетологический подход в коррекции ХБП у кошек

На правах рекламы
Хроническая болезнь почек (ХБП) — распространенный клинический диагноз у кошек среднего и старшего возраста. ХБП — основная причина заболеваемости и смертности, особенно среди кошек в возрасте 10 лет и старше, и, похоже, ее распространенность только растет. 1 Данные, собранные в 23 ветеринарных учебных клиниках в период времени с 1990 по 2000 гг., демонстрируют, что, ХБП наиболее распространена среди пожилых кошек (33%), при этом чуть меньше трети всех случаев относится к кошкам в возрасте менее 10 лет. 2
У кошек с ранними стадиями ХБП клинические признаки могут не проявляться или быть несущественными, вследствие чего они ошибочно расцениваются хозяевами как возрастные изменения. Рутинный лабораторный анализ кошек старшей возрастной группы важен для определения ХБП на ранних стадиях. Чтобы свести к минимуму прогрессирование заболевания и отсрочить проявление уремии, необходимо раннее принятие терапевтических мер.
ДИАГНОСТИКА ХБП У КОШЕК
Хотя для ХБП и не существует чувствительных показателей, наиболее распространенным отклонением в биохимии сыворотки является повышение азота мочевины и креатинина.
Более 75% нефронов должны утратить свою функцию, прежде чем разовьется азотемия. Концентрирующая способность почек нарушается, когда 66% нефронов не функционирует, поэтому отклонения удельного веса мочи можно обнаружить раньше, чем повышение уровня азота мочевины и креатинина. У кошек с ХБП также может обнаруживаться гиперфосфатемия и/или гипокалиемия. С ХБП часто ассоциирована системная артериальная гипертензия. У кошек с ХБП рекомендуется проводить регулярный контроль давления крови.
ЦЕЛИ ПРИ КОРРЕКЦИИ ХБП У КОШЕК (ПО IRIS 6 )
1. Контроль клинических признаков уремии
2. Поддержание адекватного баланса жидкостей, электролитов, кислотно-щелочного баланса
3. Обеспечение адекватного питания
4. Сведение к минимуму прогрессирования заболевания.
ГЛОССАРИЙ ХБП
■ Хроническая болезнь почек (ХБП) — медленное прогрессирующее снижение функции почек
■ Болезнь почек — Любые структурные или функциональные повреждения почек
■ Почечная недостаточность — Неспособность выводить продукты метаболизма (азотемия)
■ Азотемия — повышение уровня мочевины и/или креатинина в сыворотке.
■ Уремия — Избыток азотистых продуктов метаболизма в крови, вызывающий рвоту, диарею, потерю массы тела, дегидратацию и изъязвления в ротовой полости.
ДИЕТОТЕРАПИЯ ХБП
Диетотерапия — основной элемент ухода за кошками с ХБП. Корм для поддержания функции почек повышает время выживаемости 4 и снижает частоту эпизодов уремии. У людей с ХБП сообщается о повышении продукции свободных радикалов и дефиците антиоксидантов, а использование пищевых добавок с антиоксидантами (витамины A, C и E) уменьшает оксидативный стресс. Добавление антиоксидантов к корму, предназначенному для сохранения функции почек, существенно уменьшает повреждение ДНК у кошек со спонтанной ХБП и может быть полезно для кошек с заболеванием почек. 5
РАЗБОР КЛИНИЧЕСКОГО СЛУЧАЯ
■ 8-летняя домашняя короткошерстная кошка
■ Индекс массы тела 3 из 5 (норма)
■ Хроническое заболевание почек стадии 2 по классификации IRIS
Владельцы Милли заметили, что теперь ее лоток приходится чистить чаще, но они не отметили повышения потребления воды. Результаты клинического анализа крови, биохимии крови и анализа мочи выявили уровень азота мочевины 32 мг/дл, креатинина 2,0 и удельный вес мочи, равный 1,017. В моче белка не обнаружено, артериальное давление было в пределах нормы (Стадия IRIS 2).
РЕКОМЕНДАЦИЯ
Хотя у Милли выявлена ранняя стадия заболевания почек, не менее важно начать использовать специальное питание. Ее перевели на рацион Hill’s ® Prescription Diet ® k/d Feline ® , смесь сухого и консервированного кормов. Владельцы также поставили больше мисок для воды по всему дому и следят за тем, чтобы в них всегда была свежая вода. Они согласились привезти ее на осмотр через 8 недель.
ИСХОД И НАБЛЮДЕНИЕ
Милли чувствовала себя хорошо на новом рационе. На повторном обследовании через 8 недель азот мочевины находился в пределах нормы, однако уровень креатинина был незначительно повышен, а удельный вес мочи составлял 1,018. Ее продолжали кормить рационом k/d Feline ® и поддерживать ее массу тела. Владельцы Милли были довольны тем, что ее заболевание почек было выявлено на ранней стадии и что они помогли замедлить его прогрессирование с помощью нового специального питания.
ИССЛЕДОВАНИЕ — ВЛИЯНИЕ СМЕНЫ РАЦИОНА НА ТЕЧЕНИЕ ХБП У КОШЕК*
■ 2-летнее двойное слепое контролируемое рандомизированное клиническое исследование было проведено с целью сравнения рациона Hill’s ® Prescription Diet ® Feline k/d ® и повседневного корма для взрослых кошек в отношении способности уменьшать уремию и снижать смертность у кошек со спонтанной ХБП.
■ 45 кошек с ХБП и легкой или умеренной степенью азотемии (концентрация креатинина в сыворотке от 2,1 до 4,5 мг/дл) были рандомизированы в 2 группы, одна из которых получала повседневный корм (23 кошки), а другая — рацион Hill’s ® Prescription Diet ® Feline k/d ® (22 кошки).
■ У кошек, получавших повседневный корм, было отмечено гораздо больше эпизодов уремии (26% кошек) в сравнении с кошками, получавшими Feline k/d ® (0% кошек) (p ® (p ® Prescription Diet ® Feline k/d ® у кошек со спонтанными ХБП, когда уровень креатинина в сыворотке превышает 2 мг/дл.
■ К полезным эффектам можно отнести уменьшение числа эпизодов уремии и снижение смертности от почечной недостаточности у кошек со спонтанной ХБП.
* Clinical evaluation of effects of dietary modification in cats with chronic kidney disease
(резюме). Ross S, Osborne CA, Polzin D, et al. J Vet Intern Med 19:433, 2005.
1. Feline renal failure: Questions, answers, questions. Lulich JP, Osborne CA, O’Brien TD, et al. Compend Contin Educ Pract Vet 14:127-153, 1992.
2. Veterinary Medical Database, Purdue University, West Lafayette, Indiana.
3. Survival of cats with naturally occurring chronic renal failure is related to severity of proteinuria. Syme HM, Markwell PJ, Pfiffer D, Elliott J. J Vet Intern Med 20:528-535, 2006.
4. Dietary management of feline chronic renal failure: Where are we now? In what direction are we headed? Polzin DJ, Osborne CA, Ross S, et al. J Feline Med Surg 2:75-82, 2000.
5. Dietary supplements of vitamins E and C and‚ β−carotene reduce oxidative stress in cats with renal insufficiency. Yu S, Paetau-Robinson I. Vet Res Comm 30:403-413, 2006.
6. Международное общество исследования почек (International Renal Interest Society - IRIS). Больше информации по адресу www.iris-kidney.com.
Хорошие решения достигаются путем сочетания клинического опыта, экспериментальных доказательств и предпочтений владельца/пациента.
РЕЗЮМЕ НЕКОТОРЫХ ИССЛЕДОВАНИЙ ПО ХБП*
Диетотерапию заболеваний почек у кошек оценивали в экспериментальных исследованиях хирургически инициированной почечной недостаточности и естественно встречающихся случаев болезни. Исследования демонстрируют, что избытка протеинов и фосфора следует избегать, необходимо также использовать добавки калия, а также то, что изменение соотношения жиров n-6:n-3 может дать положительный эффект.
III УРОВЕНЬ
■ Effects of dietary protein and calorie restriction in clinically normal cats and in cats with
surgically induced chronic renal failure. Adams LG, Polzin DJ, Osborne CA, et al. Am J Vet Res 54:1653-1662, 1993.
III УРОВЕНЬ
■ Survival of cats with naturally occurring chronic renal failure: Effect of dietary management. Elliott J, Rawlings J, Markwell PJ, et al. J Small Anim Pract 41:235-242, 2000.
■ Dietary supplements of vitamins E and C and‚ β-carotene reduce oxidative stress in cats with renal insufficiency. Yu S, Paetau-Robinson I. V
†См. систему уровней доказательности ниже
Доказательная медицина* Система уровней доказательности
Хорошо спланированные рандомизированные контролируемые клинические исследования с естественно встречающимися случаями заболевания; проспективные исследования.
Хорошо спланированные и контролируемые лабораторные исследования с естественно встречающимися случаями заболевания.
УРОВЕНЬ III
Одно из перечисленных: нерандомизированные клинические исследования, когортные исследования случай-контроль, серии случаев, приемлемые модели заболевания или существенные результаты неконтролируемых исследований.
Одно из перечисленных: лабораторные исследования in vivo, мнения экспертов, основанные на клиническом опыте, описательные исследования, исследования на других видах, патофизиологическое обоснование, отчеты комитета экспертов.

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
- Код по МКБ-10
- Эпидемиология
- Причины
- Факторы риска
- Патогенез
- Симптомы
- Стадии
- Формы
- Осложнения и последствия
- Диагностика
- Дифференциальная диагностика
- Лечение
- К кому обратиться?
- Профилактика
- Прогноз

Одним из вариантов нефротоксических поражений является азотемия – это состояние, сопровождающееся нарушением почечной функции на фоне избыточного содержания в кровотоке азотных соединений. Если течение такой патологии тяжелое, то возможно быстрое развитие острой почечной недостаточности.
Если перевести название «азотемия» с латинского языка, то оно буквально означает «азот в кровотоке». Иногда это состояние называют уремией – то есть, «мочой в кровотоке», но эти понятия не совсем одинаковы: азотемия обычно является основой уремии.
Суть патологии заключается в том, что при распаде белка выделяются такие азотистые соединения, как мочевая кислота, мочевина, креатинин, аммиак, пурины и индикан. Присутствие таких продуктов в крови и обусловливает развитие азотемии.
Код по МКБ-10
Эпидемиология
Интересно, что многие аспекты азотемии до сих пор остаются неясными. С учетом сказанного, азотемия довольно распространена, на нее приходится от 8% до 16% госпитализаций и, более того, она связана со значительно более высоким риском смерти. [1]
Азотемия является единственным достоверным критерием развития почечной недостаточности, в том числе и хронической её формы, при которой показатели сывороточного креатинина превышают 0,18 ммоль/литр, а мочевины – 8 ммоль/литр (норма – 0,12 ммоль/литр и 6 ммоль/литр соответственно). Об уремии говорят при понижении массы функционирующих нефронов менее 20-25% от необходимого количества, и при выраженной азотемии (уровень креатинина больше 0,45 ммоль/литр, при мочевине больше 25-30 ммоль/литр).
Частота первичного обнаружения азотемии составляет 5-20 случаев на сотню населения в год. Чаще всего патологию диагностируют у пациентов 45-65 лет. [2]
Причины азотемии
Кровь непрерывно фильтруется почками, что необходимо для выведения продуктов жизнедеятельности и поддержания электролитного равновесия в системе кровообращения. При уменьшении притока крови к почкам фильтрация притормаживается, что приводит к скоплению продуктов, которые должны выводиться из организма. Такое состояние может достигать уровня интоксикации.
Скопление азотистых соединений (к примеру, мочевины и креатинина) типично для состояния азотемии и способно значительно осложнить работу организма. Подобная патология провоцируется любыми нарушениями, ухудшающими почечное кровообращение – в том числе, недостаточной сердечной деятельностью, шоковым состоянием, обезвоживанием, сильной кровопотерей и пр. [3]
В целом, речь идет о таких причинах азотемии:
- расстройство почечного кровообращения, понижение перфузии вследствие падения объема циркулирующей крови, застойная сердечная функция, ослабевание системного сопротивления сосудов, понижение функционального артериального объема, что может быть вызвано сепсисом, гепаторенальным синдромом, неправильной работой почечной артерии;
- острая или хроническая почечная недостаточность, повреждение клубочков, канальцев, капилляров;
- двусторонняя обструкция мочеточника опухолями или камнями, забрюшинный фиброз, нейрогенный мочевой пузырь, обструкция мочепузырной шейки вследствие увеличения предстательной железы или аденокарциномы.
Азотемия может сочетаться и проявляться на фоне других патологий.
Факторы риска
Опасными факторами, имеющими значение в развитии азотемии, могут стать:
- травматическое шоковое состояние;
- краш-синдром, повреждение и омертвение мышечной ткани;
- электротравмы;
- термические повреждения (обморожения, ожоги);
- сильные потери крови;
- анафилактический шок;
- перитониты, панкреатиты, панкреонекрозы, холециститы;
- обезвоживание, нарушение электролитного равновесия, что может быть связано с изнурительной рвотой, поносом и пр.;
- тяжелое течение инфекционных патологий;
- бактериальный шок;
- патологии акушерства (сепсисы, эклампсия, послеродовые потери крови, нефропатия с преждевременной отслойкой плаценты и пр.);
- кардиогенный шок;
- интенсивная утрата жидкости при лихорадящих состояниях, физических перегрузках, ожогах;
- интенсивная утрата жидкости почками (при несахарном диабете, терапии мочегонными препаратами, заболеваниях почек с полиурией, декомпенсированном сахарном диабете и пр.);
- нарушенное поступление жидкости в организм.
В группу риска развития азотемии входят пациенты с повышенным уровнем артериального давления, сахарным диабетом, ожирением, а также лица в возрасте старше 50 лет, с различными заболеваниями почек (в том числе семейными), курильщики. Людям, входящим в группу риска, рекомендуется регулярно посещать врача для профилактического осмотра и сдачи основных клинических анализов. [4]
Патогенез
Мочевина является финальным продуктом белкового распада в организме, образуется в печени. В ходе выведения мочевины почками происходит выведение остатков «лишнего» азота. Частично выводится потовыми железами (что обусловливает специфический «аромат» пота).
Мочевина позволяет сохранять влагу в организме, нормализует минеральный обмен. Однако избыток этого вещества вредит тканям и органам. Его уровень зависит от равновесия процессов выработки и выведения из организма. Понижение концентрации отмечается на фоне низкобелкового питания, голодания, а также при печеночных патологиях, химических интоксикациях (мышьяком, фосфоросодержащими веществами), во время беременности или гемодиализа.
Клинически значимой считается азотемия, вызванная такими причинами:
- заболеваниями почек, при которых происходит нарушение выведения мочевины из системы кровообращения (пиелонефрит, гломерулонефрит, почечный амилоидоз, острая почечная недостаточность, гидронефроз);
- преимущественно белковым питанием, обезвоживанием, воспалительными патологиями, сопровождающимися усиленным белковым распадом;
- механической блокировкой выведения мочевины почками (камнеобразование, опухоли).
Азотемия вызывает увеличение присутствия в кровотоке мочевины, креатинина, мочевой кислоты, метилгуанидина, фосфатов и пр. Мочевина и креатинин прямо зависимы от степени дисфункции нефронов. Информация о токсичном воздействии креатинина отсутствует, а вот избыточное количество мочевины способно приводить к головной боли, апатии, миастении, артритам. С развитием хронической почечной недостаточности нарушается тубулярно-гломерулярный баланс, повышается белковый катаболизм. [5]
Симптомы азотемии
Клиническая картина при азотемии развивается по нарастающей прогрессии, в зависимости от поражения определенных органов и систем, а также от повышения уровня азотистых соединений в системе кровообращения.
Базовыми симптомами считаются такие:
- резкое уменьшение объема выделяемой мочи (олигурия), вплоть до полного прекращения (анурия);
- жажда, сухость слизистых и кожных покровов;
- появление кровотечений разного вида, кровоточивости, гематом и пр.;
- появление отеков, вплоть до генерализованной отечности мягких тканей;
- перепады показателей артериального давления;
- учащение сердцебиения.
На начальной стадии пациенты жалуются на появление слабости, утомляемость, апатию, ухудшение аппетита. Рано отмечаются признаки анемии, обусловленные кровопотерей, недостатком железа и сиженным образованием эритропоэтина. Со временем общая слабость и сонливость нарастают, появляется апатия (уремическая энцефалопатия), ослабление мышц с судорожными подергиваниями, возникает зуд кожи, парестезии, кровоточивость. Возможно развитие псевдоподагры. Симптоматика может нарастать стремительно или постепенно.
Картина тяжелой, необратимой при диализе, азотемии включает в себя выраженные диспептические явления (неукротимую рвоту, диарею, анорексию), стоматогингивит, хейлит, побледнение и пожелтение лица, сухость кожи. Значительно повышается артериальное давление, отмечается кардиомегалия, регинопатия, застойная сердечная недостаточность. Поражается костная система в виде остеопороза, остеомаляции. Неврологические симптомы представлены миопатиейи энцефалопатией.
У пациентов пожилого возраста нарастают признаки коронарного атеросклероза.
Первые признаки
Адекватное количество азота в кровотоке приравнивается к 18-40 мг/литр. Если это содержание по каким-либо причинам повышается, то говорят о развитии патологии, а именно – об азотемии.
Врачи говорят о таких основных признаках присутствия азота в крови:
- Нарушения, касающиеся пищеварительного тракта: запах кислоты или нашатырного спирта из ротовой полости, кишечные расстройства, тошнота с рвотой, профузная диарея (иногда – с кровянистыми прожилками), признаки анемии.
- Нарушения в работе нервной системы: дрожание мускулатуры рук и ног, эмоциональные перепады (апатия сменяется состоянием чрезмерного возбуждения), сонливость, затрудненное дыхание.
- Прочие нарушения (кровоточивость, сухость кожных покровов, общий зуд).
Указанные признаки, как правило, сочетаются друг с другом и говорят о развитии почечной недостаточности. Если лечебные меры не будут приняты своевременно, то картина усугубляется, а шансы на излечение снижаются.
Изменения в полости рта при азотемии
На приеме у врача при осмотре пациентов с азотемией можно отметить такие симптомы:
- общее побледнение кожи («анемический» цвет лица);
- потемнение ногтей;
- ссадины на коже, царапины, связанные с интенсивным зудом.
Пациенты жалуются на сухость в ротовой полости, боль в деснах, кровоточивость, изменение вкусовых ощущений, появление металлического привкуса и неприятного запаха. У отдельных пациентов отмечается боль в языке или внутренней стороне щек. Частота указанных патологических признаков непостоянна. К примеру, сухость в ротовой полости выявляется в 20-30% случаев, кровоточивость десен – практически в каждом втором случае, нарушение вкуса – в 25% случаев, а уремический запах изо рта можно наблюдать практически у 80% пациентов.
Достаточно распространенным сопутствующим заболеванием при азотемии становится уремический стоматит. Патология развивается при повышении мочевины в сыворотке больше чем на 150 мг/мл, но полная картина появления нарушения пока не выяснена. Патологические элементы чаще обнаруживаются на внутренней поверхности языка и слизистой ротовой полости. Стоматит плохо реагирует на лечение до нормализации уровня мочевины в крови, после чего излечивается самостоятельно на протяжении нескольких недель.
Стадии
Течение хронической азотемии подразделяется на курабельную и терминальную стадии. Курабельная стадия полностью обратима при своевременном назначении лечения и устранении причины патологии. Если же речь идет о тяжелом случае, когда период анурии продолжается в течение нескольких суток, то летальный исход может наступить в результате гиперкалиемии, ацидоза, нарушения водно-электролитного обмена.
Терминальная стадия характеризуется выраженным снижением клубочковой фильтрации с нарушением адаптивных механизмов почек. Ухудшают ситуацию повышенное артериальное давление, перикардит, нарушение кровообращения.
В терминальной стадии резко возрастает риск гибели пациента. Для продления жизни больного используют регулярный диализ. Летальный исход может наступить в результате нарушений сердечно-сосудистой деятельности, гиперкалиемии, инфекционных осложнений, сепсиса, геморрагий, а также вследствие развития уремической комы.
Формы
Азотемия имеет несколько классификаций, зависящих от причинного фактора появления нарушения. Однако все виды азотемии при почечной недостаточности обладают несколькими общими характеристиками: для них типично понижение скорости почечной клубочковой фильтрации и повышение азота мочевины в кровотоке и уровня креатинина в сыворотке. Используют индекс отношения азота мочевины к креатинину: этот показатель необходим для оценки типа азотемии. Нормальным индексным показателем считается
Copyright © 2011 - 2021 iLive. Все права защищены.
Интерпретация результатов биохимического исследования крови и корреляции показателей
Анализ крови, биохимический или клинический (общий), обязывает исследователя, помимо грамотного и достоверного исследования, логически объяснять корреляцию между показателями в исследуемом образце. Но эта практика, почему-то не проводится, что приводит или к неграмотной (недостоверной) интерпретации показателей врачём, особенно, если ветеринарный врач только начинает свою профессиональную деятельность. Также важным упущением является внутрилабораторный контроль исследований. О внутрилабораторном контроле чуть подробнее, назовём его самоконтролем исследователя.
При поступлении животного для исследования (биохимического) и соблюдении всех правил взятия крови и выдерживании животного на голодной диете, результаты исследования обязаны быть достоверными, то есть, отражать нормальные или патологические процессы в живом организме, учитывая, что живой организм является единым целым, и органы функционируют в совокупности, то и исследуемые показатели крови (отвечающие за деятельность того или иного органа) должны коррелировать (взаимозависеть) между собой. Соответственно, изменение одного из показателей, изменяет и другие. Эту особенность изменений и корреляцию исследуемых показателей в первую очередь должен замечать сам исследователь (эксперт-биохимик, врач-лаборант и т.д.), с обязательным указанием на возможную или существующую патологию лечащему врачу (при беседе по результатам исследований) или хотя бы кратким заключением. Возвращаясь к внутрилабораторному контролю исследований, можно сделать вывод, что, если будет соблюдаться правило интерпретации анализов экспертом, проводившим его, то достоверность результатов будет увеличиваться, с возможным исключением ложных выводов, т.к. сам эксперт, наблюдая разницу в результатах лабораторных данных и клинического состояния животного с дополнительными исследованиями (УЗИ, рентген и т.д.), будет обязан провести повторные исследования или заново протестировать свое оборудование с реактивами, для исключения возможной ошибки. При несоблюдении этого условия (обязательной интерпретации анализов и внутрилабораторный контроль исследований), довольно часто будет встречаться явление, когда анализы являются пувеличениео подшивкой в историю болезни, без полного их непонимания и использования в терапии. При этом общепринято отдавать рентгеновский снимок с описанием, при УЗИ делается аналогичное заключение, исключение составляет биохимический анализ. Удивляет ещё то, что в лабораториях, особенно работающих не первый год (совместно с ветеринарными клиниками), должны быть наработки по изменениям в составе крови (биохимические изменения показателей) при заболеваниях встречающиеся у животных, и часто именно по этому выдача заключений (хотя бы кратких) на биохимический анализ до сих пор в большинстве лабораторий не практикуется.
К вопросу о нормах. Они, в своей основе, относительны. Нормы должны быть у каждого исследуемого животного свои (каждый организм индивидуален), но в действительности, проводить биохимический анализ каждому животному в половозрелом возрасте, с периодичностью, хотя бы месяц, нереально. Берутся усреднённые значения по большой выборке животных (как должно делаться) и получаются нормы для животных. Поэтому в каждой лаборатории должны быть свои нормальные биохимические значения показателей крови.
Подходя к вопросу корреляции показателей между собой, исследователь или врач должен в первую очередь иметь хорошие представления о двух дисциплинах: во-первых, физиология, во-вторых, патологическая физиология. Это необходимо, как для понимания патологии в целом, так и биохимических показателей, которые выбирают для исследования. Но, необходимо помнить, что для постановки диагноза только по данным биохимического анализа недостаточно. Необходим качественно выполненный общий клинический анализ крови с обязательным просмотром и объяснением нативного мазка.
Но вернёмся к биохимическому анализу. Приступая к описанию показателей, хочется отметить, что данные, приведённые в статье, получены в результате собственных исследований.
Разберёмся с подходом, необходимым при просмотре анализа. Все показатели надо анализировать в совокупности, т.е., трансферазы отдельно не рассматриваются, а обязательно во взаимосвязи с глюкозой, креатинином, мочевиной, макро-микроэлементами, холестерином и т.д., как и перечисленные показатели в отдельности не рассматриваются. Лишних показателей не бывает, исследуемое вещество либо подтверждает предположение, либо опровергает, либо наводит на возможную патологию. Каждое животное индивидуально, при одинаковой симптоматике, могут проявляться различные заболевания. Не всегда достаточны биохимические исследования (биохимические анализы показывают функциональное состояние органа /к примеру, фильтрующую способность почек - креатинин/ или степень патологического процесса /острый или хронический гепатит/). Довольно часто нужны дополнительные методы исследования: такие как УЗИ (как метод, выявляющий органические поражения органа), рентген, бактериологические исследования и т.д. Анализируя полученный результат, надо в первую очередь распределить показатели, которые прямо указывают на патологию в органе (значительное повышение аланинаминотрасферазы – гепатит), и на показатели вспомогательные необходимые для конкретизации патологии (повышение холестерина – хронический, снижение – острый гепатит). В основе всей представленной научной литературы по клинической биохимии, основной упор делается на определение клинического значения каждого показателя, хотя одна и та же патология встречается при описании различных показателей. Например, деструктивные изменения в печени указываются при описании трансфераз – АСТ увеличивается при нормальном уровне АЛТ; уровень Ca 2+ снижается, в тоже время происходит увеличение фосфора, с увеличениеом щелочной фосфатазы и холестерола если, конечно, процесс не давний, т.к. при длительной деструкции наблюдается снижение уровня холестерола и т.д. Как уже было сказано, все показатели взаимосвязаны, поэтому, что бы уметь “прочитать” анализ, надо для себя решить, с анализа деятельности какого органа надо начать анализ результатов (печени или почек). Наиболее оптимально начинать анализировать результаты с функции почек, так как показателей, указывающих на функцию почек меньше, чем при анализе печени и связанных с изменениями трансферазами. Для исследований были выбраны следующие показатели: глюкоза, мочевина, креатинин, общий белок, альбумин, билирубины, холестерин, кальций, магний, железо, фосфор, a-Амилаза, аспартатаминотрансфераза (АСТ), аланинаминотрансфераза (АЛТ) и щелочная фосфатаза. Количество показателей для анализа можно было бы и увеличить, но в данной работе преследовалась цель - дать корреляцию этого небольшого количества показателей, для постановки предварительного диагноза, не прибегая к другим диагностики.
Далее по работе отдельных органов (патологии будет рассматриваться по степени тяжести: легкая, средняя, тяжелая и без отягощения дополнительными патологиями)
ПОЧКИ
При патологии почек характерно (начальная почечная недостаточность) повышение креатинина до 2 раз выше верхней границы нормы. При верхней границе равной 120, превышение в 2 раза будет являться 120х2= 240. Обычно сопровождается незначительным повышением мочевины (до 10 % от верхней границы нормы); незначительным повышением или в пределах нормы холестерина; если отягощено циститом идёт увеличение прямого билирубина; общий белок в пределах нормы, ближе к верхней границе; альбумин – в середине нормы (если нет воспаления где-либо); кальций с фосфором обычно не меняется, если не идёт нарушение канальцевой реабсорбции – в этом случае повышается кальций (исключая гормонально-зависимое повышение – эктопическое повышение паратгормона (эндометрит, пувеличениеатит), кальциевые подкормки), также повышается фосфор при условии образовании фосфатов в почках (это характерно и при других степенях тяжести); магний часто повышается; повышение уровня АСТ наблюдается при миоглобинурии (чаще встречается у кошек при кормлении исключительно мясом.
Почечная недостаточность средней степени сопровождается повышением креатинина от 2 до 4 раз выше верхней границы нормы, проявляется характерное повышение мочевины до 2 раз относительно верхней границы нормы; возможен увеличение глюкозы, на фоне начинающегося нефрита или нефроза, пиело- или гломерулонефрите. Воспалительный процесс биохимически отличается от средней степени почечной недостаточности. Это проявляется, хотя и косвенно по изменению Са и Р. Са 2+ при функциональной почечной недостаточности, обычно, определялся на уровне нижней границе нормы (или чуть ниже до 10%), при воспалении снижение будет значительнее; фосфор в первом случае – середина нормы или чуть выше, во втором случае – до верхней границы нормы. Идёт повышение a - Амилазы, магния, холестерола, значительно общего белка, с падением уровня альбуминов. Процесс может сопровождаться анемией (снижением железа), недостоверным повышением щелочной фосфатазы и довольно часто (при нормальном функционировании печени) снижением трансфераз, ниже нижней границы нормы (особенно АСТ, если нет миоглобинурии см. выше).
Тяжелая степень почечной недостаточности – повышение креатинина от 6 раз и выше; значительное повышение мочевины (3 и более раз); a-Амилазы (до 1,5 раз); холестерина; фосфора; часто глюкозы; значительное снижение кальция и довольно часто общего белка (потеря белка с мочой при нефротическом синдроме).
При средней и тяжелой степени почечной недостаточности довольно часто встречается развитие ДВС-синдрома, это визуально диагностируется в пробирке по образованию гелевой массы
ДИСБАКТЕРИОЗ
Отдельно заслуживают внимания трансферазы, помимо упомянутой ранее миоглобинурии, изменение этих ферментов может меняться не только при патологии печени (в основе своей).
Надо указать, что для этих ферментов характерно «колебание» внутри нормы. Это явление проявляется, когда АСТ находится на нижней границе нормы или снижено в результате не усвоения или не образования микрофлорой кишечника витаминов группы В, а АЛТ стремится к верхней границе нормы, что обусловлено токсическим воздействием на печень продуктов жизнедеятельности условно-патогенной, а также патогенной микрофлоры кишечника.
Общий белок может находиться по верхней границе нормы или выше нормы (при условии отсутствия других патологий – гепатит, панкреатит, нефропатии) – это указывает на выраженность воспалительного процесса по ЖКТ, с вероятной локализацией воспаления по отделам, в которых не идёт усвоение белка и аминокислот; в середине нормы (чаще как результат воспаления лимфоидной ткани по ЖКТ); нижняя граница нормы при гастритах и гастроэнтеритах по тонкому отделу кишечника (нарушение усвоения белка и аминокислот).
Уровень Са 2+ обычно снижается вместе с Mg (при исключении почечной недостаточности - увеличение) – синдром мальабсорбции.
Повышение уровня Fe (при отсутствии гепатита), как результат апластической анемии – недостаточное поступление В 6, В 9 и В 12, но чаще происходит снижение уровня Fe, в связи с развитием по ЖКТ гемолитической микрофлоры и, как результат, кровопотеря по желудочно-кишечному тракту, а также в результате воспалительных процессов по начальному отделу тонкого кишечника и невозможности всасывания Fe (необходима корреляция с уровнем гемоглобина и эритроцитов).
Но для постановки данного заболевания или подозрения на него, необходимо проведения копрологического, бактериологического и, по необходимости, вирусологического исследования.
ПЕЧЕНЬ
К разговору о нарушении функций печени надо начинать с уровня мочевины относительно креатинина. При увеличениее креатинина выше верхней границы нормы уровень мочевины начинает расти, как результат нарушения фильтрующей способности почек, на фоне почечной недостаточности. Также характерно повышение мочевины на фоне более выраженной почечной недостаточности. Но, при патологии печени, происходит снижение концентрации уровня мочевины относительно увеличениеа креатинина, как результат гипофункции печени по обменным процессам. При установлении дальнейшей степени и выраженности патологии печени, необходимо учитывать уровни трансфераз:
- АЛТ – снижение показателя происходит на фоне ферментативной гипофункции печени; повышение – результат воспалительных процессов печени
- АСТ – повышение, как результат деструктивных изменений в печени, с обязательной корреляцией с уровнем щелочной фосфатазы (как маркер для исключения миоглобинурии, мышечной дистрофии, сердечно-сосуд. недостаточности, дерматомиозиты).
Отдельно заслуживает внимание такое наблюдение: верхняя граница нормы или чуть выше её уровень АСТ, на фоне нижней границе нормы АЛТ, при незначительном увеличениее щелочной фосфатазы и повышение уровня фосфора – результат длительной деструкции печени приведшей к циррозированию органа и значительной ферментативной гипофункции органа
Для подтверждения возможной патологии печени, необходимо проанализировать также уровень макро-микроэлементов: деструктивные изменения – повышение фосфора, на фоне снижения Са и Mg; инфекционный или сильно выраженный гепатит – повышение уровня Fe
Изменение уровня холестерина, Глюкозы, Щелочной фосфатазы см. ряд аксиом
Костная ткань
Менее нижней границе нормы щелочной фосфатазы указывает на нарушение обновления костяка или начальное рахитическое состояние (чаще всего как следствие недостаточного поступления и синтеза Вит С по ЖКТ, а также подкормок в юном возрасте), а также остеомаляционные процессы (увеличение Са на фоне снижения фосфора – при отсутствии половых нарушений)
Превышение в 2-5 раз выше верхней границе нормы щелочной фосфатазы случаи развития «Болезни Педжета» в юном возрасте до года, преобладанием функций остеокластов над остеобластами, а также в престарелом возрасте, как результат нарушения обновления костной ткани (остеопорозные явления - повышение костной фракции щелочной фосфатазы, на фоне снижения фосфора) наиболее значимые и необходимые показатели в юном возрасте по костяку – уровень Кальция, Фосфора (соотношение и сбалансированность), в дополнение к ним уровень Магния (подтверждение недостатка макроэлементов).
Лаборатории чаще всего не выводят нормы для юного возраста, а в бланках вбивают нормы уже взрослых животных, для установления истинных норм для растущего животного можно воспользоваться экстраполяцией норм от взрослого (в полученном бланке результатов) в сравнении с нормами у растущих животных в приведённых таблицах ниже.
Читайте также: