Лечение послеоперационной серомы у собак
Опубликовано: 24.07.2024
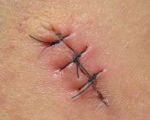
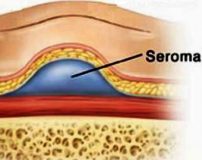
Послеоперационная серома – это скопление серозной жидкости в зоне шва, обусловленное травматизацией мягких тканей. Является осложнением хирургических вмешательств. Рассасывается самостоятельно либо принимает хроническое течение. Проявляется припухл остью в области шва, чувством распирания, неприятными ощущениями и эффектом переливания жидкости при перемене положения тела. При крупных серомах наблюдаются нарушение общего состояния, субфебрилитет. Патология может осложняться инфицированием, формированием некроза. Лечение – пункции или дренирование с активной аспирацией на фоне медикаментозной терапии. В отдельных случаях требуются повторные операции.
МКБ-10


- Причины
- Патогенез
- Классификация
- Симптомы послеоперационной серомы
- Осложнения
- Диагностика
- Лечение послеоперационной серомы
- Консервативная терапия
- Хирургическое лечение
- Прогноз
- Профилактика
- Цены на лечение
Общие сведения
Послеоперационная серома (серома шва) – распространенное осложнение раннего послеоперационного периода. Чаще всего встречается в общей хирургии, маммологии, онкологии и пластической хирургии. По различным данным, частота образования клинически значимых сером после операций, сопровождающихся значительной отслойкой мягких тканей, колеблется от 0,8% до 80% и более. Осложнение может развиваться у пациентов любого возраста и пола, чаще встречается у женщин средней и старшей возрастной группы.

Причины
Серома является полиэтиологическим состоянием, рассматривается как осложнение обширных хирургических вмешательств. Некоторые специалисты придерживаются мнения, что скопление жидкости в проекции послеоперационной раны нельзя считать осложнением, поскольку оно представляет собой нормальный процесс заживления в фазе экссудации.
В подтверждение своей точки зрения ученые приводят данные ультразвуковых исследований, согласно которым послеоперационные серомы (в том числе – клинически незначимые) обнаруживаются у 100% пациентов. Основными провоцирующими факторами образования крупных сером, требующих проведения активных лечебных мероприятий, являются:
- значительная отслойка жировой клетчатки;
- большая раневая поверхность;
- грубые хирургические манипуляции с тканями (многочисленные разрезы, захват раздавливающим инструментом и пр.);
- чрезмерное использование коагуляции;
- большая толщина подкожной жировой клетчатки (более 5 см).
К числу предрасполагающих условий относят индивидуальные особенности организма, нарушения иммунитета, сахарный диабет и хронические соматические заболевания, негативно влияющие на процесс заживления раны. Чаще всего послеоперационные серомы образуются после абдоминопластики, герниопластики, маммопластики, мастэктомии, аппендэктомии, холецистэктомии. При использовании имплантатов имеет значение раздражение окружающих тканей и развитие асептического воспаления вследствие контакта с эндопротезом.
Патогенез
Существуют различные точки зрения на патогенез сером. Согласно наиболее популярной, обширные разрезы, отслойка мягкотканных структур, раздавливание или прижигание тканей и другие факторы вызывают значительные повреждения мелких лимфатических сосудов. Лимфатические сосуды тромбируются медленнее кровеносных, в результате лимфа долгое время изливается в ткани. На этапе экссудации жидкая часть крови выходит за пределы кровеносных сосудов, что увеличивает количество жидкости в тканях.
В полостях, возникших в области послеоперационной раны, скапливается соломенно-желтая жидкость, содержащая макрофаги, тучные клетки, лейкоциты и белковые фракции. В норме эта жидкость асептическая. При попадании микроорганизмов возможно нагноение с формированием абсцесса. Крупные скопления жидкости оказывают давление на окружающие ткани, нарушают кровоснабжение, вследствие чего могут образовываться участки некроза по краю швов.
Классификация
В клинической практике используют классификацию, в основе которой лежит необходимость и тактика лечения патологии. Согласно этой систематизации выделяют три группы послеоперационных сером:
- 1 группа. Асимптоматические образования, не требующие проведения лечебных мероприятий.
- 2 группа. Симптоматические серомы, для устранения которых достаточно пункций или активного дренирования.
- 3 группа. Симптоматические скопления жидкости, требующие проведения повторной операции.

Симптомы послеоперационной серомы
Маленькие образования не вызывают неприятных ощущений и нарушений общего состояния. Единственными признаками серомы являются припухлость и положительный симптом флюктуации в области послеоперационных швов. Иногда пациенты отмечают ощущение переливания жидкости во время изменения положения тела. Гиперемия кожи в зоне швов обычно отсутствует.
Больные с крупными серомами жалуются на неинтенсивную тянущую боль, чувство давления или распирания, которые усиливаются в положении стоя. В проекции швов выявляется валикообразная флюктуирующая припухлость. Длина припухлости обычно совпадает с длиной шва, ширина может варьироваться от 2-3 до 10 и более сантиметров. Возможны локальная гиперемия, слабость, утомляемость, повышение температуры тела до субфебрильных цифр.
Осложнения
Наиболее серьезным осложнением является нагноение серомы. При большом количестве жидкости формируются крупные абсцессы. Возможно расплавление подлежащих тканей с развитием перитонита. У некоторых больных развивается сепсис. Некрозы при серомах, как правило, протекают более благоприятно, захватывают небольшие участки тканей в области швов. Хронические серомы ухудшают качество жизни, существенно увеличивают период нетрудоспособности после операций.
Диагностика
Обычно серомы развиваются в период стационарного послеоперационного лечения, поэтому диагноз выставляется лечащим врачом. Диагностика базируется на данных объективного осмотра, при необходимости назначаются дополнительные исследования. Программа обследования может включать:
- Физикальный осмотр. В пользу серомы свидетельствует наличие ограниченного выбухания тканей в сочетании с положительным симптомом флюктуации. При отсутствии инфицирования гиперемия не выявляется или незначительная, пальпация малоболезненна. При инфицировании кожа багрово-синюшная, ощупывание резко болезненно, определяется плотный отек окружающих тканей.
- УЗИ мягких тканей. Показано для подтверждения диагноза при сомнительном симптоме флюктуации, для уточнения размеров крупных сером на этапе подготовки к хирургическому вмешательству. Свидетельствует о наличии полости, заполненной жидкостью.
- Лабораторные анализы. Для изучения характера содержимого серомы проводят цитологическое исследование. При подозрении на инфицирование выполняют бакпосев жидкости для определения возбудителя, назначают общий анализ крови для оценки выраженности воспаления.

Лечение послеоперационной серомы
Лечение осуществляется в стационарных условиях. При крупных образованиях, отсутствии признаков рассасывания показана комплексная терапия, включающая в себя консервативные и оперативные мероприятия.
Консервативная терапия
Целью консервативного лечения является снижение вероятности инфицирования, устранение асептического воспаления, уменьшение количества жидкости. Применяются медикаменты следующих групп.
- Антибиотики. При отсутствии нагноения пациентам для профилактики назначают препараты широкого спектра действия внутримышечно. При появлении признаков инфицирования план антибиотикотерапии корректируют с учетом чувствительности возбудителя.
- НВПС. Нестероидные противовоспалительные средства уменьшают проявления воспаления и количество жидкости, выделяющейся в просвет полости послеоперационной серомы. Возможно внутримышечное введение или пероральный прием.
- Глюкокортикоиды. Гормональные препараты устраняют асептическое воспаление, блокируют образование жидкости. Медикаменты вводят в полость серомы после удаления жидкости.
Хирургическое лечение
Тактика хирургического лечения определяется размерами серомы, эффективностью лечебных мероприятий на предыдущих стадиях. При неосложненных серомах возможны следующие варианты:
- Пункции. Наиболее простой способ удаления жидкости. Выполняется 1 раз в несколько дней, для полного излечения обычно требуется 3-7 пункций.
- Активная аспирация. При неэффективности пункций, значительном объеме серомы в полость образования устанавливают дренаж с устройством для активной аспирации.
- Реконструктивные операции. Показаны при упорном хроническом течении сером, отсутствии результата после лечения более щадящими способами.
При нагноившихся серомах производится вскрытие, дренирование гнойной полости. При образовании участков некроза проводят перевязки до отторжения струпа и полного заживления раны. Все хирургические методы применяют на фоне консервативной терапии.
Прогноз
Прогноз в большинстве случаев благоприятный. Небольшие серомы нередко рассасываются самостоятельно в течение 1-2 недель. Эффективность пункций при серомах на фоне плановых пластических и абдоминальных операций составляет около 90%. Реконструктивные вмешательства требуются редко. Процент нагноений незначительный, осложнение чаще развивается после экстренных операций, при наличии сопутствующей патологии, излишнем весе.
Профилактика
Профилактические мероприятия включают тщательную оценку риска хирургических вмешательств, детальное предоперационное обследование, соблюдение техники проведения операций. Хирургам необходимо воздерживаться от слишком широких разрезов, грубых манипуляций с тканями, чрезмерного использования коагулятора.
Клинический случай хирургического лечения остеосаркомы лучевой кости у собаки с замещением пострезекционного костного дефекта индивидуальным эндопротезом, изготовленным методом 3D-печати II часть.
Авторы: Горшков С. С., Уланова Н. В., Козлов Е. М., Мануйлова В. В., Петрова Е. И. Ветеринарная клиника «Бэст» (Новосибирск), январь 2019 г.
Сокращения: ОС – остеогенная саркома (остеосаркома), ОСО – органосохраняющая операция, ПММ – полиметилметакрилат (костный цемент), LCP – locking compression plate (блокирующаяся компрессионная пластина), LС-DCP – (limited contact dynamic compression plate) – динамическая компрессионная пластина ограниченного контакта, SLM (Selective Laser Melting) – выборочная лазерная плавка, ПХН – позиционный хирургический направитель (синоним: хирургический направляющий шаблон [гайд], в литературе также упоминается как прецизионный персонифицированный/индивидуальный направитель [ППН]), DICOM-файл (DICOM File) – медицинский отраслевой стандарт создания, хранения, передачи и визуализации цифровых медицинских изображений и документов обследованных пациентов.
Анализ и оценка осложнений. Клинические рекомендации
Основные осложнения после выполнения ОСО, по литературным данным, включают инфицирование, местный рецидив, несостоятельность фиксации, метастатическое поражение (Withrow & Vail, 2007). Также отмечены такие осложнения, как выраженный болевой синдром, длительная хромота, временная нейропраксия и стойкий неврологический дефицит с потерей чувствительности 5 . На сегодняшний день развитие послеоперационной инфекции является наиболее частым и серьезным осложнением, которое развивается в 30–75 % случаев в первые 6 месяцев после проведения ОСО (LaRue et al., 1989; Dernell et al., 1998). Несостоятельность имплантатов отмечают до 40 % случаев, однако серьезные осложнения, требующие ревизии, происходит лишь в 10 % случаев (Liptak et al., 2006). Местный рецидив опухоли наблюдается в 20–28 % случаев (Morello et al., 2001; Withrow et al., 2004; Liptak et al., 2006).
На основании всего периода наблюдения в данном клиническом случае были выявлены следующие осложнения: скопление серомы в области реконструируемого дефекта в ранний послеоперационный период, миграция винтов.
Формирование серомы (лимфоцеле, длительная серозная экссудация) отмечали в ранний п/о период. Длительность сохранения отделяемого составила 20 дней. Серома, предположительно, не является осложнением, поскольку процесс ее формирования соответствует фазе экссудации раневого воспаления при обычном заживлении раны 6 7 . Таким образом, серома не относится к истинным инфекционным осложнениям, которые можно было бы интерпретировать в качестве прогностической оценки более длительного периода выживания. Развитие серомы в большинстве случаев связано с неизбежным формированием «мертвого» пространства после ОСО ввиду обширной резекции пораженной кости и мягких тканей. По данным ряда исследователей, основными причинами образования сером являются наличие раневой полости и реакция организма на имплантат, контакт эндопротеза с подкожно-жировой клетчаткой, обширная диссекция и мобилизация подкожно-жировой клетчатки, а также использование электрокоагуляции 6 7 . Серома служит питательной средой для патологической флоры, что может привести к последующему инфицированию.
В рандомизированных исследованиях отмечено, что использование электрокоагулятора в сравнении с обычным скальпелем во время операции повышает риск образования сером, а использование ультразвуковых ножниц при выполнения диссекции, наоборот, уменьшает риск развития данного осложнения 7 .
У данного пациента была выполнена трехкратная аспирация содержимого с интервалом 4–5 дней. В некоторых случаях может быть использовано наложение повязки по типу Роберта-Джонаса на 1–3 дня сразу после операции. На основании результатов ряда исследований в гуманной медицине стоит отметить, что компрессионный трикотаж позволяет уменьшить объем послеоперационной полости6 8. Отмечают также, что расположение в сформированной полости фибрин-коллагенового препарата (коллагеновая гемостатическая губка) после обширной резекции новообразования (НО) может быть эффективным в качестве интраоперационной меры для профилактики сером без последующего дренирования зоны хирургического вмешательства 6 .
Несостоятельность фиксации (НФ) в виде перелома, миграции имплантатов отмечают в 40 % случаев, однако тяжелые осложнения, требующие ревизионной хирургии с заменой имплантата, встречаются лишь в 10 % случаев (Liptak et al., 2006). Основные причины НФ представляют собой сочетание биологических и механических факторов, которые могут привести к ослаблению фиксации с последующим развитие миграции и/или переломов имплантатов в послеоперационный период.
Механические факторы НФ4:
- Несоответствующий размер имплантата (короткие конструкции) и его тип (неподходящий для ОСО имплантат).
- Циклические нагрузки на имплантаты, эндопротез.
- Инфицирование в результате иммуносупрессии, вызванной опухолью или самим лечением (хирургическое лечение и применение химиотерапии).
- Предоперационная лучевая терапия.
- Наличие у пациента сопутствующих заболеваний (ожирение, наличие ранее возникшего очага инфекции, эндокринопатии, неврологические или ортопедические патологии контралатеральных конечностей).
В рассматриваемом нами клиническом случае миграция двух дистальных углостабильных винтов из проксимального сегмента локтевой кости была выявлена на 82-й день (рис. 18). Значимого усиления хромоты не отмечалось, однако при пальпации на контрольном осмотре был выявлен умеренный болевой синдром. Было выполнено удаление двух углостабильных винтов. Клинического ухудшения опороспособности и нестабильности фиксации после удаления винтов отмечено не было.
Обсуждение и выводы. Клинические рекомендации
Основная цель ОСО – достижение раннего восстановления опороспособности пациента посредством широкой сегментарной резекции пораженной кости с последующей реконструкцией удаленной части кости и созданием стабильной фиксации между сохраненными сегментами конечности.
В данном клиническом случае было реализовано две технологии 3D-печати. Сегментарная резекция была выполнена с использованием «напечатанных» индивидуальных шаблонов (ПХН), что позволило с точностью до 1 мм выполнить предоперационно спланированную хирургом резекцию НО на требуемом уровне на основании замеров и костных ориентиров, а реконструкция пострезекционного костного дефекта (пРКД) была выполнена индивидуальным эндопротезом (3D-печать; SLM) из титанового сплава (Ti6AI4V).
Индивидуальные прецизионные хирургические направители (ПХН)
Использование ПХН позволяет сократить время ОСО, так как сформированные отверстия в кости для фиксации ПХН соответствуют отверстиям в уже изготовленном эндопротезе, и нужно лишь однократно высверлить отверстия в кости, а затем осуществить введение винтов. Таким образом, после выполнения резекции, удаления ПХН и последующего введения в проксимальный сегмент эндопротеза последний «надевается» дистальной частью на временно зафиксированные в кости спицы Киршнера, благодаря чему и достигается первичная репозиция остеотомированных сегментов кости в заданном положении.
Использование ПХН позволяет выполнять остеотомию с предельной точностью именно в пределах заранее спланированной области резекции.
Проводить ОСО, по нашим наблюдениям, стоит не позднее 7-10 дней с момента выполнения КТ, так как вторичные изменения в случае прогрессирования ОС (инвазия) могут изменять структуру кости и мягких тканей и и не позволить адекватно расположить как направляющие шаблоны, так и сам эндопротез.
Также для сокращения времени оперативного лечения на поверхности эндопротеза (над винтовыми отверстиями) была выполнена лазерная цифровая разметка длины вводимых винтов.
ПХН выполнены из пластика (фотополимер), к положительным качествам которого можно отнести возможность стерилизации (автоклавирование) и легкость в применении.
На основании литературных данных и опыта авторов, использование позиционных хирургических направителей может быть сопряжено с рядом осложнений, связанных с некорректной установкой имплантата на кости, и, соответственно, с ошибочным определением уровня и линии остеотомии, а также с несостоятельностью (разрушением) ПХН при выполнении остеотомии10. Данные осложнения могут быть связаны с допущением хирургом ошибок при 3D-планировании. Профилактика ряда осложнений возможна при накоплении опыта работы с планированием 3D-объектов при ОСО, ПХН и непосредственно с планировщиком.
К недостаткам использования ПХН стоит отнести их хрупкость (перелом ПХН) при изменении угла пропила и избыточном давлении во время остеотомии, а также при остеотомии на уровне «края паза» ПХН. В подобных случаях авторами статьи отмечено, что выполнение остеотомии через «пропиливание ПХН» путем остеотомии кости и самого паза в ПХН не приведет к его ятрогенному расколу, а за счет биосовместимости фотополимера предотвратит инфицирование и позволит осуществить операцию на должном уровне с требуемой точностью и в полном объеме. Это особенно актуально при коррекции костных деформаций для выполнения презиционной остеотомии. Данные осложнения являются ятрогенными и нивелируются по мере накопления опыта работы с такими имплантатами.
Использование индивидуальных эндопротезов из титанового сплава (Ti6AI4V) для реконструкции пРКД, изготовленных методом аддитивных технологий, на сегодняшний день является приоритетным направлением в онкоортопедии. Стоит отметить, что благодаря большой прочности и высокой устойчивости к коррозии титан и его сплавы практически не имеют конкурентов в имплантологии, так как не изменяют своих свойств под влиянием агрессивных биологических сред организма и сами не оказывают токсического воздействия на живые ткани14. Высказаны предположения, что использование эндопротезов из металла вместо аллотрансплантатов снижает частоту возникновения инфицирования при ОСО 15 .
Применение технологий трехмерной печати в производстве имплантатов обеспечивает их высокую прецизионность и персонифицированность, а также возможность создания протезов любой формы, сложности и размеров исходя из требований хирурга для конкретного пациента.
К важным конструктивным особенностям 3D-эндопротезов относится возможность создания пористой структуры титана в местах контакта с костью, что впоследствии позволяет достигать остеоинтеграции. Данных условий невозможно добиться каким-либо другим способом производства, кроме аддитивных методов.
Конфигурация 3D-имплантата
По мнению авторов статьи, конфигурация эндопротеза «ИМ стержень, фиксируемый методом «плотной посадки» (press-fit) + блокируемая пластина (экстрамедуллярная фиксация)» позволяет нивелировать основные силы, воздействующие на область «кость – эндопротез», и добиваться адекватной аксиальной поддержки, равномерно распределять нагрузку и создавать более прочное соединение, чем при аналогичных техниках, используемых в монорежиме.
По результатам биомеханических исследований, ИМ стержень обеспечивает большую площадь контакта с костью, что приводит к снижению концентрации изгибающих нагрузок на проксимальные винты в лучевой кости 12 13 .
Создание углостабильных отверстий в эндопротезе позволяет добиваться более жесткой фиксации, особенно у пациентов с тонкими кортикальными слоями кости 5 12 15 .
К недостаткам метода можно отнести отсутствие модульности эндопротеза. При необходимости интраоперационно изменить уровень резекции или положение эндопротеза стоит отметить, что сделать это невозможно, поскольку эндопротез представляет собой единую монолитную конструкцию. Профилактировать данное осложнения можно посредством выполнения тщательного предоперационного планирования. Как уже отмечалось, проводить ОСО стоит не позднее 7–10 дней с момента выполнения КТ, так как в течение этого периода времени, несмотря на химиотерапию, может возникнуть инвазия НО в мягкотканный и/или костный компонент, что неизбежно приведет к невозможности реализации стабильной фиксации эндопротеза, а в худшем случае - к местному рецидиву и ампутации в случае неполной резекции (загрязненные края).
Использование двух пластин для фиксации на уровне костей пясти (3 и 4) под углостабильные винты, обеспечивает более стабильную фиксацию в сравнении с стандартными кортикальными винтами и позволяет достигать ранней опороспособности посл ОСО 13 .
По опыту авторов статьи, несмотря на создание более жесткой конструкции эндопротеза в сравнении с LC-DCP-конструкциями за счет добавления углостабильных отверстий, корректная бикортикальная фиксация винтов на уровне пястных костей в большинстве случаев не достигается. Это связано с невозможностью введения винтов под необходимым углом (что чаще всего требуется осуществлять на практике) и приводит к разрушению одного из кортикальных слоев пястных костей. Введение же углостабильных винтов возможно лишь под углом 90° (рис. 20). Таким образом, авторы пришли к выводу, что в данном случае при ОСО, а также при создании артродеза на уровне пястных и плюсневых костей в подобных хирургических вмешательствах более оправданно использование стандартных кортикальных винтов, так как их введение можно выполнить под требуемым углом.
Предоперационное планирование ОСО на основании данных КТ с использованием программного обеспечения типа Polygon Medical Engineering и в тесном сотрудничестве с биоинженерами представляет следующий этап развития онкоортопедии и реконструктивной хирургии, позволяющий добиваться предсказуемо запланированных результатов и отказаться от «импровизационной» хирургии – наиболее распространенного подхода в современной ветеринарной медицине.
По наблюдению авторов, транскортикальное введение винтов в локтевую кость через лучевую часто сопряжено с последующим их переломом или миграцией, что в данном клиническом случае привело к асептической нестабильности винтов и к их удалению (рис. 21, 22). Однако это не стало причиной общей нестабильности имплантата в отдаленный период (рис. 23, 24). Имеются данные о том, что при использовании модульной системы фиксации у собаки при ОСО было отмечено осложнение в виде несостоятельности фиксации в локтевом компоненте эндопротеза, которое может быть связано с наличием физиологической пронации-супинации лучевой кости относительно локтевой. В дальнейшем требуются оценка и анализ данного типа осложнений с целью недопущения развития клинически значимой несостоятельности фиксации.
Заключение
В последнее время органосохранная хирургия уже является стандартом лечения ОС аппендикулярного скелета у собак во всем мире (с учетом правильного
подбора кандидатов и без ущерба для онкологического радикализма). Использование компьютерной 3D-реконструкции позволяет точно спланировать области хирургической резекции, вычислить объем резецируемого фрагмента с последующим его замещением.
Использование аддитивных технологий, в частности персонифицированных ПХН и эндопротезов, создаваемых с применением 3D-печати, позволяет прецизионно и одномоментно замещать костные дефекты любой формы, сложности и размеров, возникающие после удаления опухоли, и упрощать технику операции, сокращая время оперативного вмешательства.
Предоперационное планирование, адекватный подбор кандидатов, а также пред- и послеоперационная химиотерапии при выполнении ОСО имеют решающее значение и позволяют улучшить результаты лечения пациентов с аппендикулярной ОС. Создание 3D-моделей (макетов-копий) костей на основании данных КТ уже вошло в мировую медицинскую практику и используется для 3D-печати фрагментов костей и конечностей целиком с целью предоперационного планирования и отработки предстоящей операции.
Изготовление индивидуальных эндопротезов с применением аддитивных технологий для замещения обширных костных дефектов после перенесенных ОСО у животных на сегодняшний день весьма актуально и имеет огромный потенциал, даже больший, чем в гуманной медицине, в связи с широкой породной вариабельностью анатомических особенностей аппендикулярного скелета у собак.

Что такое опухоль?
Разрастание патологической ткани, которая похожа на обычную ткань организма. Опухоли или неоплазии или новообразования могут вырастать из любой ткани.
Как часто вы встречаетесь с опухолями молочной железы у животных?
20% всех обратившихся в клинику животных – животные с новообразованиями, чаще всего с опухолями молочной железы (ОМЖ) , реже – опухоли селезенки, печени, кожи, костей.
У каких животных чаще встречаются ОМЖ, в каком возрасте?
Чаще у кошек старше 4-5 лет, у не стерилизованных, и у тех, кому владельцы применяли гормональные препараты для подавления течки. У собак – суки старше 5 лет, не стерилизованные, но чаще всего их опухоли не связаны с применением половых гормонов, собакам их дают крайне редко.
Есть ли стадии у опухолей молочной железы?
Конечно, есть, как и любых других опухолей. Стадия, которую поставит врач на приеме будет зависеть от размера опухолей, вовлеченности в процесс регионарных лимфоузлов, наличия отдалённых метастазов.
Какие исследования необходимо провести животному перед операцией?
Обязательно перед операцией сдавать общий и биохимический анализы крови, делать УЗИ сердца, УЗИ органов брюшной полости и рентген грудной клетки. Так же после операции необходимо сделать гистологическое исследование опухоли. Анализы крови нужны, чтобы знать, как в целом работает организм, нет ли почечной недостаточности. Сделать УЗИ сердца собаке или кошке нужно для выявления скрытых врожденных или приобретенных патологий. УЗИ органов брюшной полости– для выявления опухолей или метастазов во внутренних органах. Рентген для животных в области грудной клетки – для исключения метастазов в легкие. Если на этих исследованиях находятся отдаленные метастазы, операция не целесообразна. Если метастазов нет, по анализам и другим исследованиям все хорошо, то обязательно нужно настраиваться на оперативное вмешательство с последующим исследованием опухоли.
Всегда ли нужна операция?
Да, всегда. Операция проводится, чтобы опухоль не увеличивались и не разрастались. Т.к. опухоль имеет свойство созревать и вскрываться как абсцесс. Даже если владельцы не соглашаются на операцию ввиду того, что опухоль маленькая и находится на одном месте не один год, все равно необходимо ее удалить. Такая на первый взгляд безобидная опухоль может дать метастазы в легкие, а изменения будут заметны только лишь на последних стадиях. Появится кашель, или животное откажется от еды, и только лишь на УЗИ или рентгене можно обнаружить, наличие метастазов.
Когда проводят химиотерапию собаке или кошке?
Химиотерапию проводят только после результатов гистологического исследования. Желательно это делать всегда, если опухоль оказалась злокачественной. Даже после удачной операции, опухоли могут вырасти на том же месте. Химиотерапия полного выздоровления не даст, однако
мы с помощью этих препаратов сможем остановить процесс дальнейшего появления злокачественных клеток.
Оказывает ли влияние стерилизация кошек и собак на развитие ОМЖ?
У кошки и собаки, стерилизованных до первой течки, риск развития опухолей молочной железы снижен на 70%, по сравнению с нестерилизованными. Если кошка или собака были стерилизованы после первой течки – риск снижается на 30%, если же после второй – риск остается одинаковым у стерилизованные и у не стерилизованных.
Что делать если опухоль молочной железы вскрылась?
Необходимо приехать в клинику, чтобы врач мог оценить характер и локализацию раны, ее обширность. Так же необходимо оценить состояние животного, чтобы решить с владельцем, можно ли в данном состоянии прооперировать животное. Если нет – то врач выпишет мази с антибиотиком или антибиотики для системного использования.
Что такое неоперабельная ОМЖ?
Опухоль больших размеров, и не хватает здоровой ткани, чтобы после операции закрыть рану. Обширная опухоль, проросшая в мышечную ткань, костную ткань, и если имеется поражение внутренних органов.
От чего зависит площадь операции?
От расположения первичной опухоли. У кошек независимо от расположения, удаляются все молочные пакеты по одной стороне. У собак расположение опухоли играет роль, т.к. иногда возможно удалить половину. Площадь операции может оценить врач на приеме. Если у кошки на второй стороне молочной железы узелков новообразования нет, для улучшения качества жизни и здоровья пациента, все равно рекомендовано удаление второй стороны пакетов молочной железы через месяц после первой операции. У собак чаще всего удаляется половина пакетов с новообразованиями.
Что такое мастэктомия? Какая она бывает?
Мастэктомия – удаление молочной железы. При выполнении локальной мастэктомии удаляется непосредственно сама опухоль. Делается это только в том случае, если животное старое, в основном такие операции выполняются для улучшения качества жизни животного, и для возможности забора материала для гистологического исследования.
Регионарная мастэктомия возможна только у собак. Удаляется 3 молочных пакета из 5 по одной стороне. При унилатеральной мастэктомии удаляется одна сторон молочной железы, при билатеральной – две стороны
Обязательно ли вместе с удаление ОМЖ стерилизовать животное?
Не обязательно. За исключением наличия кисты или новообразования яичника и при воспалительных процессах в матке.
Бывает ли ОМЖ у самцов?
Очень редко. Лечение такое же, как у само – удаление опухолей с последующим исследованием.
Какой прогноз после удаления ОМЖ?
Прогноз будет зависеть от вида опухоли. Если опухоль доброкачественная, прогноз благоприятный. Если злокачественная, прогноз сомнительный или неблагоприятный. При наличии злокачественной опухоли, мы можем продлить жизнь животному на недолгий срок – от 3 месяцев до 2 -3 лет. Однако у нас есть случаи, когда животные прожили 6-7 лет после операции. Для животного это почти половина жизни.
Например, кошке 16 лет. Можно ли в таком возрасте делать операцию?
Можно. В нашей клинике были проведены несколько десятков операцией у кошек старше 15 лет, 6 операций кошкам в возрасте 20 – 23 года. Все операции закончились благоприятно, жизнь животного мы продлили в среднем на 2 года.
Какие послеоперационные осложнения могут развиваться?
Во время удаления молочной железы, убирается большой объем тканей, и такие раны заживают дольше, чем от кастрации или стерилизации собак и кошек. Чаще всего хозяева не до конца понимают вид операции. Возникновение обширных гематом (что является нормой) воспринимают это как критическую ситуацию. Так же послеоперационная серома – скопление жидкости в области паха тоже является нормой.
Какие исследования нужно проходить животному после удаления ОМЖ?
Обязательно каждые 3 -6 месяцев делать УЗИ органов брюшной полости, рентген грудной клетки для раннего выявления метастазов. При наличии метастазов мы ничем животному помочь не сможем, однако владельцы будут морально готовы к неблагоприятному исходу.
Всегда ли необходимо гистологическое исследование?
Это исследование нам поможет выявить какая опухоль – доброкачественная или злокачественная. Если она злокачественная, то нам необходимо знать, какой вид опухоли, чтобы можно было подобрать препараты для химиотерапии.
Владельцы сделали биопсию, чтобы потом удалить опухоль. Опухоль оказалась доброкачественной. Нужно ли ее удалять или можно оставить?
Такую опухоль лучше удалить, потому что доброкачественные опухоли тоже может продолжить рост, или через какой-то время стать злокачественными. Этот момент перехода никакими анализами, кроме биопсии невозможно отследить.
Что такое паллиативные операции?
Это операции, которые направлены на улучшение качества жизни животного, но не несут никакого лечебного эффекта. Например, мы можем удалить вскрывшуюся опухоль у старого животного с метастазами. Эта опухоль не вылечит животное, однако значительно облегчит жизнь и животному и владельцам.
Ветеринарный хирург Василькин Александр Станиславович
Собака после наркоза, последствия наркоза

Наркоз — нагрузка для организма во время операции. Зачастую именно реакция организма на введение анестезии и определяет тяжесть реабилитационной терапии в первые послеоперационные сутки.
В нашей клинике операции проводятся в сопровождении ветеринарных врачей-анестезиологов, что снижает процент негативного влияния наркоза на организм собаки.
Выход из состояния наркоза происходит в ветеринарной клинике под наблюдением врачей. Именно пробуждение считается одним из ответственных моментов, так как в случае, если что-то пойдет не так, любимцу понадобится экстренная помощь ветеринарных специалистов.
Перед тем, как вы увезете собаку домой, внимательно выслушайте и запишите все рекомендации ветеринарного врача по уходу в послеоперационный период. Так как во время операции собаки снижается температура тела, то при пробуждении животное испытывает озноб. Поэтому перед транспортировкой домой собаку лучше укрыть одеялом, таким образом, озноб уменьшится.
Возможные осложнения после операции собаки
После операции мы рассчитываем на положительную динамику, но иногда бывают и осложнения, о которых необходимо знать. Какие осложнения в послеоперационный период могут быть, и к чему должны быть готовы владельцы животного?
- Понижение общей температуры тела, слизистые оболочки бледные или синюшные, затрудненное дыхание;
- Судороги, отек в области морды и шеи. Такая реакция может указывать об аллергической реакции на какой-либо препарат. Требуется срочная коррекция назначений и введение антигистаминного средства;
- Постоянная рвота. Однократная - двукратная рвота может быть, но если ее количество составляет более 2 раз,- нужно немедленно обратиться в клинику;
- Отек и покраснение в области раны, гнойные истечения с неприятным запахом или кровотечение из шва.
При проявлении данных симптомов обратитесь немедленно в ветеринарную клинику за помощью.
Уход за швами собаки после операции

У собак после операции регенерация тканей, если нет патологии, происходит обычно быстро. Важным моментом является обработка швов, которую необходимо проводить 1-2 раза в день. Используем при этом не содержащие спирт дезинфицирующие средства. Рекомендуем использовать "Хлоргексидина биглюконат" или "Алюминиум спрей". Алюминиум спрей создает защитную пленку, не пересушивая шов, способствует быстрому заживлению и затягиванию краев шва.
Место, где располагается шов, нужно защитить специальной послеоперационной попоной. При чрезмерном любопытстве собаки к попоне (пытается снять, разгрызть), можно надеть защитный воротник, который не даст животному дотянуться до проблемного места. Попону необходимо носить животному в течение 10-14 дней, попона меняется по мере загрязнения, поэтому лучше приобрести несколько сменных попон.
Уход за собакой после операции в домашних условиях
Собака после операции нуждается в правильном послеоперационном уходе. Подстилку необходимо разместить на полу, в теплом помещении без сквозняков. Для создания комфортного места используйте электрическую грелку, так как после операции у животного снижается температура тела. Обеспечьте доступ к воде. Кормление можно осуществлять только по рекомендации вашего лечащего врача.

Если проводилась операция на желудочно-кишечном тракте, кормление осуществляют мелкими дробными порциями, используя специализированные корма (Purina Proplan, Royal Canin, Monge, Hill’s, Eukanuba и др.). Предпочтительнее использовать влажные паштеты или размачивать сухой корм, формируя паштетообразную консистенцию. При проведении других оперативных вмешательств кормление может проводиться в обычном режиме, только спустя 3-4 часа после операции.
Хомутинник Екатерина Игоревна Главный ветеринарный врач. Кандидат ветеринарных наук. Специализация: хирургия мягких тканей, абдоминальная и торакальная хирургия, эндохирургия.
Период реабилитации собаки зависит от конкретного случая, поэтому владелец должен быть готов к тому, что период реабилитации после операции может быть затяжным. При благоприятном течении реабилитационного периода восстановление организма животного проходит в кратчайшие сроки, обычно в течение 7 дней.
Если у вас еще остались вопросы после прочтения нашей статьи, вы можете получить всю необходимую информацию об уходе за собакой после операции у наших специалистов.
Получить консультацию специалиста по любому вопросу
Оставьте свой номер, чтобы получить консультацию
или звоните +7 (812) 646-76-26
Работаем 24 часа в сутки. Без выходных.
Мы принимаем к оплате



ул.Коллонтай, д.30, к. 1,
м.Проспект Большевиков,
+7 812 646 76 26
email: drpetsspb@mail.ru

п.Колтуши, Школьный переулок, д. 1,
м.Улица Дыбенко,
+7 812 983 40 41
email: drpetsspb@mail.ru

Послеоперационная серома – это скопление серозной жидкости в зоне шва, обусловленное травматизацией мягких тканей. Является осложнением хирургических вмешательств. Рассасывается самостоятельно либо принимает хроническое течение. Проявляется припухл остью в области шва, чувством распирания, неприятными ощущениями и эффектом переливания жидкости при перемене положения тела. При крупных серомах наблюдаются нарушение общего состояния, субфебрилитет. Патология может осложняться инфицированием, формированием некроза. Лечение – пункции или дренирование с активной аспирацией на фоне медикаментозной терапии. В отдельных случаях требуются повторные операции.
МКБ-10



- Причины
- Патогенез
- Классификация
- Симптомы послеоперационной серомы
- Осложнения
- Диагностика
- Лечение послеоперационной серомы
- Консервативная терапия
- Хирургическое лечение
- Прогноз
- Профилактика
- Цены на лечение
Общие сведения
Послеоперационная серома (серома шва) – распространенное осложнение раннего послеоперационного периода. Чаще всего встречается в общей хирургии, маммологии, онкологии и пластической хирургии. По различным данным, частота образования клинически значимых сером после операций, сопровождающихся значительной отслойкой мягких тканей, колеблется от 0,8% до 80% и более. Осложнение может развиваться у пациентов любого возраста и пола, чаще встречается у женщин средней и старшей возрастной группы.

Причины
Серома является полиэтиологическим состоянием, рассматривается как осложнение обширных хирургических вмешательств. Некоторые специалисты придерживаются мнения, что скопление жидкости в проекции послеоперационной раны нельзя считать осложнением, поскольку оно представляет собой нормальный процесс заживления в фазе экссудации.
В подтверждение своей точки зрения ученые приводят данные ультразвуковых исследований, согласно которым послеоперационные серомы (в том числе – клинически незначимые) обнаруживаются у 100% пациентов. Основными провоцирующими факторами образования крупных сером, требующих проведения активных лечебных мероприятий, являются:
- значительная отслойка жировой клетчатки;
- большая раневая поверхность;
- грубые хирургические манипуляции с тканями (многочисленные разрезы, захват раздавливающим инструментом и пр.);
- чрезмерное использование коагуляции;
- большая толщина подкожной жировой клетчатки (более 5 см).
К числу предрасполагающих условий относят индивидуальные особенности организма, нарушения иммунитета, сахарный диабет и хронические соматические заболевания, негативно влияющие на процесс заживления раны. Чаще всего послеоперационные серомы образуются после абдоминопластики, герниопластики, маммопластики, мастэктомии, аппендэктомии, холецистэктомии. При использовании имплантатов имеет значение раздражение окружающих тканей и развитие асептического воспаления вследствие контакта с эндопротезом.
Патогенез
Существуют различные точки зрения на патогенез сером. Согласно наиболее популярной, обширные разрезы, отслойка мягкотканных структур, раздавливание или прижигание тканей и другие факторы вызывают значительные повреждения мелких лимфатических сосудов. Лимфатические сосуды тромбируются медленнее кровеносных, в результате лимфа долгое время изливается в ткани. На этапе экссудации жидкая часть крови выходит за пределы кровеносных сосудов, что увеличивает количество жидкости в тканях.
В полостях, возникших в области послеоперационной раны, скапливается соломенно-желтая жидкость, содержащая макрофаги, тучные клетки, лейкоциты и белковые фракции. В норме эта жидкость асептическая. При попадании микроорганизмов возможно нагноение с формированием абсцесса. Крупные скопления жидкости оказывают давление на окружающие ткани, нарушают кровоснабжение, вследствие чего могут образовываться участки некроза по краю швов.
Классификация
В клинической практике используют классификацию, в основе которой лежит необходимость и тактика лечения патологии. Согласно этой систематизации выделяют три группы послеоперационных сером:
- 1 группа. Асимптоматические образования, не требующие проведения лечебных мероприятий.
- 2 группа. Симптоматические серомы, для устранения которых достаточно пункций или активного дренирования.
- 3 группа. Симптоматические скопления жидкости, требующие проведения повторной операции.

Симптомы послеоперационной серомы
Маленькие образования не вызывают неприятных ощущений и нарушений общего состояния. Единственными признаками серомы являются припухлость и положительный симптом флюктуации в области послеоперационных швов. Иногда пациенты отмечают ощущение переливания жидкости во время изменения положения тела. Гиперемия кожи в зоне швов обычно отсутствует.
Больные с крупными серомами жалуются на неинтенсивную тянущую боль, чувство давления или распирания, которые усиливаются в положении стоя. В проекции швов выявляется валикообразная флюктуирующая припухлость. Длина припухлости обычно совпадает с длиной шва, ширина может варьироваться от 2-3 до 10 и более сантиметров. Возможны локальная гиперемия, слабость, утомляемость, повышение температуры тела до субфебрильных цифр.
Осложнения
Наиболее серьезным осложнением является нагноение серомы. При большом количестве жидкости формируются крупные абсцессы. Возможно расплавление подлежащих тканей с развитием перитонита. У некоторых больных развивается сепсис. Некрозы при серомах, как правило, протекают более благоприятно, захватывают небольшие участки тканей в области швов. Хронические серомы ухудшают качество жизни, существенно увеличивают период нетрудоспособности после операций.
Диагностика
Обычно серомы развиваются в период стационарного послеоперационного лечения, поэтому диагноз выставляется лечащим врачом. Диагностика базируется на данных объективного осмотра, при необходимости назначаются дополнительные исследования. Программа обследования может включать:
- Физикальный осмотр. В пользу серомы свидетельствует наличие ограниченного выбухания тканей в сочетании с положительным симптомом флюктуации. При отсутствии инфицирования гиперемия не выявляется или незначительная, пальпация малоболезненна. При инфицировании кожа багрово-синюшная, ощупывание резко болезненно, определяется плотный отек окружающих тканей.
- УЗИ мягких тканей. Показано для подтверждения диагноза при сомнительном симптоме флюктуации, для уточнения размеров крупных сером на этапе подготовки к хирургическому вмешательству. Свидетельствует о наличии полости, заполненной жидкостью.
- Лабораторные анализы. Для изучения характера содержимого серомы проводят цитологическое исследование. При подозрении на инфицирование выполняют бакпосев жидкости для определения возбудителя, назначают общий анализ крови для оценки выраженности воспаления.

Лечение послеоперационной серомы
Лечение осуществляется в стационарных условиях. При крупных образованиях, отсутствии признаков рассасывания показана комплексная терапия, включающая в себя консервативные и оперативные мероприятия.
Консервативная терапия
Целью консервативного лечения является снижение вероятности инфицирования, устранение асептического воспаления, уменьшение количества жидкости. Применяются медикаменты следующих групп.
- Антибиотики. При отсутствии нагноения пациентам для профилактики назначают препараты широкого спектра действия внутримышечно. При появлении признаков инфицирования план антибиотикотерапии корректируют с учетом чувствительности возбудителя.
- НВПС. Нестероидные противовоспалительные средства уменьшают проявления воспаления и количество жидкости, выделяющейся в просвет полости послеоперационной серомы. Возможно внутримышечное введение или пероральный прием.
- Глюкокортикоиды. Гормональные препараты устраняют асептическое воспаление, блокируют образование жидкости. Медикаменты вводят в полость серомы после удаления жидкости.
Хирургическое лечение
Тактика хирургического лечения определяется размерами серомы, эффективностью лечебных мероприятий на предыдущих стадиях. При неосложненных серомах возможны следующие варианты:
- Пункции. Наиболее простой способ удаления жидкости. Выполняется 1 раз в несколько дней, для полного излечения обычно требуется 3-7 пункций.
- Активная аспирация. При неэффективности пункций, значительном объеме серомы в полость образования устанавливают дренаж с устройством для активной аспирации.
- Реконструктивные операции. Показаны при упорном хроническом течении сером, отсутствии результата после лечения более щадящими способами.
При нагноившихся серомах производится вскрытие, дренирование гнойной полости. При образовании участков некроза проводят перевязки до отторжения струпа и полного заживления раны. Все хирургические методы применяют на фоне консервативной терапии.
Прогноз
Прогноз в большинстве случаев благоприятный. Небольшие серомы нередко рассасываются самостоятельно в течение 1-2 недель. Эффективность пункций при серомах на фоне плановых пластических и абдоминальных операций составляет около 90%. Реконструктивные вмешательства требуются редко. Процент нагноений незначительный, осложнение чаще развивается после экстренных операций, при наличии сопутствующей патологии, излишнем весе.
Профилактика
Профилактические мероприятия включают тщательную оценку риска хирургических вмешательств, детальное предоперационное обследование, соблюдение техники проведения операций. Хирургам необходимо воздерживаться от слишком широких разрезов, грубых манипуляций с тканями, чрезмерного использования коагулятора.
Читайте также:

