Миоперицитома у собак лечение
Опубликовано: 16.05.2024
Продолжение. Начало в №1/2020
Обсуждение
Опухоли сердца являются нечастыми патологиями у собак, их встречаемость, по опубликованным данным, составляет около 0,2%.
Среди опухолей сердца у собак наиболее распространенными являются гемангиосаркома (69% случаев), опухоли основания аорты, лимфома, эктопическая ткань щитовидной железы.
Гораздо реже встречаются меланома, мастоцитома, бластома, мезотелиома, миксома, миксосаркома, мезенхимома, неклассифицируемая опухоль миофибробластного происхождения, фиброма, фибросаркома, рабдомиома, рабдомиосаркома, лейомиома, лейомиосаркома, хондросаркома, остеосаркома, параганглиома, гамартома, липома, опухоль нервных оболочек.
Некоторые из них имеют специфическую локализацию, что облегчает диагностику, однако встречаются и эктопические поражения (гемангиосаркома, локализующаяся в левом предсердии вместо правых отделов).
ПЭКомы – мезенхимальные опухоли, представленные гистологически и иммуногистохимически периваскулярными эпителиоидными клетками (ПЭК), которые являются иммунореактивными к маркерам меланомы (Melan A, HMB-45) и гладкой мышечной ткани (SMA), экспрессируют виментин, рецепторы эстрогена. Типичной структурной характеристикой ПЭКомы является организация отходящих от стенки сосуда клеток, часто инфильтрирующих медию мелких и средних сосудов. Перивазальная популяция клеток в основном имеет овоидную форму, в то время как периферическая – веретенообразную. В обоих случаях в клетках имеется маленькое, расположенное в центре округлое или овальное ядро, иногда встречается полиморфизм. Цитоплазма чаще всего прозрачная или слегка эозинофильная, резко эозинофильной в перинуклеарной зоне она бывает нечасто. Периферическая популяция иногда содержит липидные включения, что позволяет им мимикрировать под липобласты. Часто опухоль имеет липоматозный тип, поскольку состоит из большого количества компонентов жировой ткани (около 70%). Реже встречается ангиоматозный (с преобладанием сосудов) и миоматозный (с содержанием клеток жировой ткани меньше 10%) типы.
Классификация
В медицинской литературе в группу ПЭКом включают ангиомиолипомы, светлоклеточные/«сахарные» опухоли легкого, лимфангиолейомиомы, светлоклеточные миомеланоцитарные опухоли круглой связки матки/серповидной связки печени, брюшно-тазовые саркомы из периваскулярных эпителиоидных клеток (поджелудочная железа, кишечник и прямая кишка, брюшина, матка, влагалище, бедро, сердце, носовая полость, заглазничное пространство). Часто данные опухоли не являются злокачественными, однако в гуманной медицине описано несколько случаев малигнизации неоплазии и системного поражения организма 2 .
Ангиомиолипома – это, как правило, доброкачественная опухоль, в основном характеризующаяся макроскопически одиночным округлым очагом от нескольких миллиметров до 35 см, имеющим гладкую поверхность и отграниченным от окружающей ткани.
Одной из самых опасных форм ангиомиолипомы является ПЭКоматоз (чаще встречается при туберозном склерозе), который начинается с матки и захватывает большое количество окружающих тканей брюшной полости. Данная патология, как правило, не дает метастатического поражения, но возможна малигнизация с мультифокальным поражением.
В ветеринарной литературе опухоли эндотелиальных клеток включают сосудистую гамартому, ангиоматоз, гемангиому, лимфангиому, гемангиосаркому и лимфангиосаркому. Гемангиосаркомы и лимфангиосаркомы часто объединяют в ангиосаркомы. Также описано наличие в этих опухолях фибробластов, перицитов и компонентов гладкой мускулатуры 27 .
Эпидемиология
Чаще всего ангиомиолипомы (наиболее распространенный тип ПЭКомы, который встречается менее чем в 1% случаев всех опухолей) поражают почки, значительно реже – легкие и крайне редко – другие ткани (печень, кожу, кости, сердце). В гуманной медицине установлено, что наиболее часто данные новообразования встречаются у женщин среднего возраста, однако светлоклеточные миомеланоцитарные опухоли серповидной связки отмечаются преимущественно у девочек от 3 лет до 21 года (средний возраст – 11 лет).
В патогенезе любой опухоли превалирующую роль играют мутации в генном аппарате. В данном случае, поскольку ангиомиолипома связана с комплексом туберозного склероза, в опухолях будут обнаружены характерные изменения 22, 2 . В первую очередь это мутации зародышевой линии в генах TSC1 или TSC2, расположенных на хромосомах 9q34 и 16p13.3, которые кодируют белки гамартин и туберин соответственно 21, 2, 23 . Туберин и гамартин взаимодействуют друг с другом и образуют цитоплазматический комплекс 25 .
Частые потери гетерозиготности вариабельных участков локуса гена TSC2 (16p13, туберин) демонстрируются в наследственных и спорадических ангиомиолипомах. Туберин является членом клеточного сигнального пути и участвует в трансляции РНК (путь mTOR), обеспечивая потенциальную терапевтическую мишень 5 .
Было высказано предположение о том, что белок p53 играет определенную роль в злокачественном прогрессировании ангиомиолипом, так как в нескольких исследованиях была показана мутация p53 исключительно в эпителиоидных клетках ангиомиолипомы 17, 19 .
Гистологические особенности
Помимо классической картины, были описаны другие, более редкие морфологические варианты, такие как эпителиоидные, атипичные, онкоцитарные, прозрачные и кистозные клетки 1, 3, 8, 13, 19, 21 .
Классическая гистологическая картина представлена зрелой жировой тканью, гладкомышечными волокнами и толстостенными сосудами различного калибра. Часто опухоль имеет трабекулярное строение и участки гемопоэза. Гладкомышечные волокна представлены веретеновидными или эпителиоидными клетками. Липоматозный компонент состоит из зрелой жировой ткани, но он может содержать вакуолизированные адипоциты, наводящие на мысль о липобластах 9, 24 .
Сосуды не имеют выраженного эластического компонента. Мышечные клетки мигрируют из стенки сосудов 1, 9, 13 .
У эпителиоидных ангиомиолипом эпителиоидные клетки обычно характеризуются полигональной формой с прозрачной эозинофильной цитоплазмой и округлыми (до овальных) ядрами с увеличенными везикулами, часто с выраженными ядрышками и различной степенью ядерной атипичности 1, 3, 9, 13 .
На данный момент даже у человека не разработаны критерии злокачественности ПЭКом ввиду редкой встречаемости данной разновидности опухолей.
Считается, что размер новообразования более 8 см и количество митозов более 1 на 50 ПЗ являются признаками злокачественности. Были описаны метастазирование опухоли и ее инвазия в сосуды.
Иммуногистохимические особенности
Ультраструктурные особенности
Дифференциальный диагноз
В список дифференциальных диагнозов включены любые новообразования, для которых характерна указанная локализация.
По гистологическим характеристикам следует предполагать карциному, онкоцитому, меланому, саркому, эпителиоидную опухоль периферических нервных оболочек, гепатобластому, гастроинтестинальную стромальную опухоль и гемангиосаркому.
Сочетание мышечных и меланоцитарных маркеров при отсутствии экспрессии цитокератина и эпителиального мембранного антигена позволяет исключить онкоцитому, гемангиосаркому и карциному. Однако некоторые почечные карциномы, представленные двумя морфологическими видами, могут проявлять меланоцитарные маркеры при отсутствии эпителиального мембранного антигена 1, 15, 18 .
Эозинофильные варианты онкоцитомы и карциномы имеют несколько общих морфологических особенностей с ангиомиолипомой, но их можно дифференцировать по маркеру меланомы и окрашиванию кератинов 9, 23 .
Первичную опухоль от метастатического поражения можно дифференцировать с помощью маркера HepPar-1 и окрашивания низкомолекулярного кератина.
Менее 40% эпителиоидных ангиомиолипом могут иметь цитоплазматический S100 без ядерного окрашивания, что отличает их от меланомы. В злокачественных меланомах может отсутствовать окрашивание S100, в таких случаях их различия зависят от дополнительных маркеров 26 .
Гастроинтестинальные опухоли экспрессируют CD117, что является отличием от ангиомиолипом 1 . Примечательно то, что меланомы и эозинофильные почечные эпителиальные опухоли также могут экспрессировать CD117 4, 14 .
Выявленной локализации в клиническом случае, описанном в рамках этой статьи (№2/2020), наиболее соответствуют несколько типов неоплазий: гемангиосаркома, мезотелиома, мезенхимома, миксома, рабдомиома и рабдомиосаркома. Однако менее вероятны из них гемангиосаркома, которая чаще локализуется в правых отделах, рабдомиома и рабдомиосаркома, поражающие внешнюю стенку органа, мезотелиома и миксома, затрагивающие клапанный аппарат сердца. Проведение субэндомиокардиальной биопсии также позволило исключить большинство перечисленных новообразований ввиду наличия в образце ткани адипоцитов без каких-либо клеток иного происхождения. В связи с отсутствием в литературе ранее описанных новообразований периваскулярных эпителиоидных клеток у животных данный диагноз не рассматривался.
Клинические признаки
Лечение
Поскольку большинство ангиомиолипом являются доброкачественными 1, 3, 12, 13, 18 , пациентам в большинстве случаев следует контролировать новообразование через регулярные интервалы времени с помощью ультразвуковой визуализации 12 .
В некоторых ситуациях может потребоваться резекция. Однако были описаны случаи злокачественной трансформации опухоли с эпителиоидным или саркоматозным перерождением 13 .
С целью лечения злокачественной ПЭКомы прибегают к хирургическому ее удалению. Этот же метод является основным для лечения метастатического поражения и рецидивов. Ни химиотерапия, ни лучевая терапия не показали должной эффективности.
Есть данные о попытках гормонотерапии с ограниченным и непродолжительным ответом. Также у человека возможно применение таргетной терапии для ингибирования mTOR, однако на сегодняшний день собрано недостаточное количество материалов для ретроспективного исследования, которое могло бы подтвердить эффективность того или иного метода 29 .
Гемангиоперицитома — весьма редкая опухоль, впервые описанная А.Р. Stout и M. R. Murray в 1942 г. К 1998 г. сообщалось о 300 случаях гемангиоперицитомы.
Гемангиоперицитома возникает в любом возрасте — от 3 дней до 92 лет, чаще улиц 38-58 лет, с одинаковой частотой у представителей обоего пола. Выделяют младенческий и взрослый варианты опухоли, клинически и гистологически настолько сходные с младенческим миофиброматозом, что отдельными авторами расцениваются как различные стадии одного процесса.
Гемангиоперицитома чаще всего поражает скелетные мышцы нижних конечностей (34,5%), забрюшинное пространство (24,5%) и область головы и шеи (17%). Она является причиной около 1% опухолей центральной нервной системы и около 3% опухолей орбиты. Опухоль поражает забрюшинное пространство, скелетные мышцы нижних конечностей, глазницу и, очень редко, кожу. Младенческая гемангиоперицитома, встречающаяся с рождения или на первом году жизни, проявляется солитарными или множественными дермальными или подкожными узлами.
Этиология гемангиоперицитомы не ясна. Ретровирусоподобные частицы, обнаруженные в гемангиоперицитомоподобных опухолях у мышей, в гемангиоперицитомах человека идентифицированы не были. Причины возникновения опухоли также связывают с механической травмой или наследственной предрасположенностью: описан семейный случай гемангиоперицитомы с аутосомно-рецессивным путем передачи.
В ранних исследованиях, основанных на результатах световой и электронной микроскопии, гемангиоперицитома расценивалась как опухоль, происходящая из перицитов — модифицированных гладкомышечных клеток, находящихся в стенках капилляров и венул. Однако в связи с отрицательным иммуногистохимическим окрашиванием большинства гемангиоперицитом взрослых на актин и другие мышечные маркеры, их происхождение в настоящее время связывают с недифференцированной мезенхимальной клеткой.
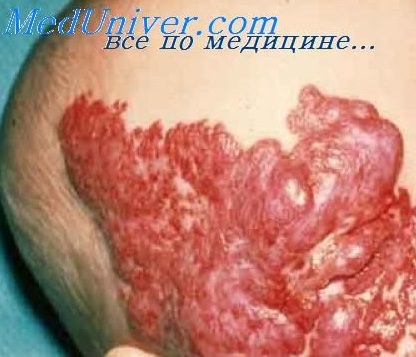
Причины и клиника гемангиоперицитом.
Клинически гемангиоперицитома представляет собой бугристое опухолевидное образование, обычно солитарное, диаметром от 0,5 до 2 см (иногда крупного размера — 35x25 см), различной (мягкой, тестоватой, плотной) консистенции, покрытое неизмененной или синюшно-красной кожей, безболезненное и медленно растущее. Боль (тупая и продолжительная) отмечается при сдавлении опухолью нерва. При определенной локализации опухоли больного могут беспокоить кашель, одышка, тошнота, задержка мочи, гидронефроз, дизурия или запоры; наличием опухоли также могут быть обусловлены телеангиэктазии. одностороннее варикозное расширение вен, геморрой, кровоподтеки, повышение температуры кожи, эндокринные (гипогликемия идр.) и неврологические проявления (при внутричерепных гемангиоперицитомах — головная боль, нарушение походки и равновесия). Опухоль может изъязвляться и давать инфильтрирующий рост, но метастазирует редко.
Макроскопически гемангиоперицитома хорошо отграничена от окружающих тканей или заключена в тонкую капсулу, цвет ее на разрезе варьирует от песочного и серого до розовато-белого, иногда он может быть фиолетовым или красновато-коричневым. Часто встречаются участки некроза, кровоизлияния и явления кистозной дегенерации. При иссечении опухоли нередки профузные кровотечения из окружающего ее большого сплетения крупных сосудов.
Гистологическое строение гемангиоперицитом.
При гистологическом исследовании неопластические перициты выглядят как веретенообразные или овальные клетки со скудной эозинофильной цитоплазмой и плохо очерченными границами. Наибольший диаметр овальных или округлых клеток составляет 7-13 мм. Опухолевые клетки располагаются вне сосудистых каналов, которые очерчены одним слоем эндотелиальных клеток. Опухолевые клетки часто сдавливают сосудистые пространства в виде «оленьих рогов», они отделены от эндотелиальных клеток периваскулярной базальной мембраной — признак, который лучше всего проявляется при окрашивании на ретикулиновые волокна. Ретикулиновые и коллагеновые волокна также обволакивают отдельные опухолевые клетки. Клетки гемангиоперицимтомы всегда располагаются случайным образом, этот признак отличает их от гломусных опухолей, имеющих концентрическое строение, и от синовиальных сарком и фибросарком, в которых опухолевые клетки встречаются в виде узлов и тяжей. Ядра гемангиоперицитомы пузырьковидные и содержат мелкие вакуоли В пределах одной опухоли интенсивность ядерного окрашивания, форма и размеры ядер почти не отличаются, что придает ей монотонный вид. Часты митозы, которые указывают на злокачественное течение. Клеточная анаплазия ассоциируется с большей агрессивностью опухоли.
Сосуды гемангиоперицитом сильно отличаются по калибру. Ткань, окружающая опухоль, содержит расширенные вены. Крупные сосудистые каналы и синусоидные сосуды распространяются радиально внутрь из перикапсулярной ткани, разветвляясь на капилляры или прекапилляры. Эта богатая васкуляризация приводит к выраженной кровоточивости. В опухоли часто видны мелкие очаги кровоизлияний.
И ммуногистохимические характеристики генмангиоперицитомы неспецифичны, но могут помочь в ее отличии от многих гистологически сходных опухолей, а также используются для более точной идентификации происхождения клеток опухоли. Клетки гемангиоперицитомы окрашиваются виментином, маркером мезенхимального происхождения. Наличие положительного окрашивания на фактор XIII во всех исследованных опухолях подтверждает их происхождение из перицитов. В связи с тем, что фактор XIII также экспрессируется злокачественной фиброзной гистиоцитомой, было высказано предположение о тесном родстве этих опухолей. Действительно, эти две опухоли невозможно отличить даже при использовании не только световой и электронной микроскопии, но и иммуногистохимических исследованиях. Иммунореактивность менингиальных, периферических и врожденных вариантов гемангиоперицитом одинакова, что подтверждает общность их происхождения. Хотя ультраструктурные исследования показывают некоторые признаки гладкомышечной дифференцировки, гладкомышечное происхождение гемангиоперицитом не подтверждается их иммунофенотипом. Окрашивание на десмин и актин в этих опухолях положительно лишь иногда. Однако низкий уровень положительного окрашивания на актин не исключает возможности, что перициты проходят дедифференцировку в процессе трансформирования в гемангиоперицитоме.
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут бы
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут быть также личинки других аскарид — кошки (T. mystax), коровы, буйвола, (T. vitulorum). Однако роль этих возбудителей в патологии человека практически не изучена
- Биология возбудителя
Половозрелые формы T. canis — крупные раздельнополые черви длиной 4 — 18 см локализуются в желудке и тонком кишечнике животных (собак). Интенсивность инвазии у собак может быть очень высокой, особенно у молодых животных. Средняя продолжительность жизни половозрелых особей составляет 4 месяца, максимальная — 6 месяцев. Самка паразита за сутки откладывает более 200 тыс. яиц. В 1 г фекалий может содержаться 10 000—15 000 яиц, так что в почву попадают миллионы яиц, обусловливая тем самым высокий риск заражения токсокарозом.
 |
Яйца токсокар округлой формы, крупнее яиц аскариды (65—75 мкм). Наружная оболочка яйца толстая, плотная, мелкобугристая. Внутри яйца располагается темный бластомер.
Цикл развития возбудителя следующий. Выделившиеся яйца токсокар попадают в почву, где, в зависимости от влажности и температуры почвы, созревают за 5—36 суток, становясь инвазионными. Инвазионность яиц сохраняется в почве длительное время, в компосте — несколько лет.
Жизненный цикл токсокары сложный. Выделяют основной цикл и два варианта вспомогательных. Основной цикл происходит по схеме: окончательный хозяин (псовые) — почва — окончательный хозяин (псовые). Передача инвазии осуществляется геооральным путем. Вспомогательный цикл (вариант 1) идет трансплацентарно, в этом случае паразит в личиночной стадии переходит от беременной самки к плоду, в организме которого совершает полную миграцию, достигая в кишечнике щенка половозрелой стадии. Инвазированный щенок становится функционально полноценным окончательным хозяином, источником инвазии.
Вспомогательный цикл (вариант 2) осуществляется по цепи: окончательный хозяин (псовые) — почва — паратенический хозяин. Паратеническим (резервуарным) хозяином могут быть грызуны, свиньи, овцы, птицы, земляные черви. Человек также выступает в роли паратенического хозяина, но не включается в цикл передачи инвазии, являясь для паразита биологическим тупиком. Дальнейшее развитие возбудителя происходит при условии, что паратенический хозяин будет съеден собакой или другим окончательным хозяином. Механизм передачи инвазии при этом варианте — геооральный — ксенотрофный.
В зависимости от возраста хозяина реализуются разные пути миграции личинок токсокар. У молодых животных (щенков до 5 недель) почти все личинки совершают полную миграцию с достижением половозрелых форм в кишечнике и выделением яиц во внешнюю среду. В организме взрослых животных большая часть личинок мигрирует в соматические ткани, где сохраняет жизнеспособность несколько лет. В период беременности и лактации у беременных сук возобновляется миграция личинок. Мигрирующие личинки через плаценту попадают в организм плода. Личинки остаются в печени пренатально инвазированных щенков до рождения, а после рождения личинки из печени мигрируют в легкие, трахею, глотку, пищевод и попадают в желудочно-кишечный тракт, где через 3—4 недели достигают половозрелой стадии и начинают выделять во внешнюю среду яйца. Кормящие суки могут передавать щенкам инвазию также через молоко.
У человека цикл развития возбудителя, его миграция осуществляется следующим образом. Из яиц токсокар, попавших в рот, затем в желудок и тонкий кишечник выходят личинки, которые через слизистую оболочку проникают в кровеносные сосуды и через систему воротной вены мигрируют в печень, где часть из них оседает, инцистируется или окружается воспалительными инфильтратами, образуя гранулемы. Часть личинок по системе печеночных вен проходит фильтр печени, попадает в правое сердце и через легочную артерию — в капиллярную сеть легких. В легких часть личинок также задерживается, а часть, пройдя фильтр легких, по большому кругу кровообращения заносится в различные органы, оседая в них. Личинки токсокар могут локализоваться в различных органах и тканях — почках, мышцах, щитовидной железе, головном мозге и др. В тканях личинки сохраняют жизнеспособность многие годы и периодически, под влиянием различных факторов, возобновляют миграцию, обусловливая рецидивы заболевания.
- Географическое распространение и эпидемиология
Токсокароз — широко распространенная инвазия, она регистрируется во многих странах. Показатели пораженности плотоядных являются высокими во всех странах мира. Средняя пораженность собак кишечным токсокарозом, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах у части животных достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз. Распространенность инвазии в различных регионах точно неизвестна, поскольку токсокароз не подлежит обязательной регистрации. Совершенно очевидно, что токсокароз имеет широкую геграфию распространения, и число больных значительно выше официально регистрируемых.
| Токсокароз широко распространен и регистрируется во многих странах. Средняя пораженность кишечным токсокарозом собак, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз |
Основным источником инвазии для человека являются собаки, особенно щенки. Заражение происходит при непосредственном контакте с инвазированным животным, шерсть которого загрязнена инвазионными яйцами, или при попадании в рот земли, в которой были яйца токсокар. Особенно подвержены заражению дети во время игры в песке или с собакой. Наибольший риск заражения у детей, страдающих геофагией. Взрослые заражаются при бытовом контакте с инвазированными животными или в процессе профессиональной деятельности (ветеринары, собаководы, работники коммунальной службы, шоферы, землекопы и др.). У человека возможно заражение также при поедании сырого или плохо обработанного термически мяса паратенических хозяев. Описаны случаи заражения токсокарозом при употреблении в пищу печени ягненка. Не исключается возможность трансплацентарной и трансмаммарной передачи инвазии и у человека.
- Патогенез и патологическая анатомия
Патогенез токсокароза сложный и определяется комплексом механизмов в системе паразит — хозяин. В период миграции личинки травмируют кровеносные сосуды и ткани, вызывая геморрагии, некроз, воспалительные изменения. Ведущая роль принадлежит иммунологическим реакциям организма в ответ на инвазию. Экскреторно-секреторные антигены личинок оказывают сенсибилизирующее действие с развитием реакций немедленного и замедленного типов. При разрушении личинок в организм человека попадают соматические антигены личинок. Аллергические реакции проявляются отеками, кожной эритемой, увеличением резистентности дыхательных путей к вдыхаемому воздуху, что клинически выражается развитием приступов удушья. В аллергических реакциях принимают участие тучные клетки, базофилы, нейтрофилы, но основную роль играют эозинофилы. Пролиферация эозинофилов регулируется Т-лимфоцитами при участии медиаторов воспалительных реакций, выделяемых сенсибилизированными лимфоцитами, нейтрофилами, базофилами. Образующиеся иммунные комплексы привлекают в очаг поражения эозинофилы. Вокруг личинок токсокар кумулируются сенсибилизированные Т-лимфоциты, привлекаются макрофаги и другие клетки — формируется паразитарная гранулома.
Патоморфологическим субстратом токсокароза является выраженное в различной степени гранулематозное поражение тканей. При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими. При токсокарозе находят многочисленные гранулемы в печени, легких, поджелудочной железе, миокарде, лимфатических узлах, головном мозге и других органах.
- Клиническая картина токсокароза
Клинические проявления определяются интенсивностью инвазии, распределением личинок в органах и тканях, частотой реинвазии и особенностями иммунного ответа человека. Симптоматика токсокароза малоспецифична и имеет сходство с клиническими симптомами острой фазы других гельминтозов. Заболевание обычно развивается внезапно и остро или после короткой продромы проявляется в виде легкого недомогания. Появляется температура — субфебрильная в легких случаях и высокая до 39°С и выше, иногда с ознобом, — в тяжелых случаях инвазии. Могут наблюдаться кожные высыпания в виде крапивницы или полиморфной сыпи, иногда отеки типа Квинке. В остром периоде наблюдается легочный синдром различной степени тяжести: от легких катаральных явлений до острого бронхита, пневмонии, тяжелых приступов удушья. Особенно тяжело легочный синдром протекает у детей раннего возраста. Рентгенологически выявляется усиление легочного рисунка, «летучие» инфильтраты, картина пневмонии. Наряду с этим у части больных отмечается увеличение печени, иногда и селезенки. Лимфаденопатия более выражена у детей. Иногда имеет место абдоминальный синдром в виде приступов болей в животе, симптомов диспепсии. Возможно развитие миокардита, панкреатита. Известны случаи поражения щитовидной железы, проявляющиеся симптомами опухоли. Возможно поражение мышечной ткани с развитием болезненных инфильтратов по ходу мышц. При миграции личинок в головной мозг развиваются симптомы поражения ЦНС: упорные головные боли, эпилептиформные приступы, парезы, параличи. У детей заболевание сопровождается слабостью, легкой возбудимостью, нарушением сна.
Наиболее характерным лабораторным показателем является повышенное содержание эозинофилов в периферической крови. Относительный уровень эозинофилии может колебаться в широких пределах, достигая в ряде случаев 70 — 80% и более. Повышается содержание лейкоцитов (от 20х109 до 30х109 на 1 л). При исследовании пунктата костного мозга выявляется гиперплазия зрелых эозинофилов. У детей нередко отмечается умеренная анемия. Некоторые исследователи отмечают прямую корреляцию между тяжестью клинических проявлений инвазии и уровнем эозинофилии и гиперлейкоцитоза периферической крови. Характерным лабораторным признаком является также ускорение СОЭ, гипергаммаглобулинемия. В случаях поражения печени наблюдается повышение билирубина, гиперферментемия.
В хронической стадии болезни острые клинические и лабораторные признаки затухают. Наиболее стабильным лабораторным показателем остается гиперэозинофилия периферической крови.
Выделяют субклиническое, легкое, среднетяжелое и тяжелое течение токсокароза. Возможна так называемая бессимптомная эозинофилия крови, когда явные клинические проявления инвазии отсутствуют, но наряду с гиперэозинофилией выявляются антитела к антигенам T.canis.
Одной из наиболее серьезных проблем, связанных с токсокарозом, является его взаимосвязь с бронхиальной астмой. При сероэпидемиологических исследованиях установлено, что у больных бронхиальной астмой нередко обнаруживаются антитела к антигенам T.canis классов Ig G и Ig E. В зависимости от остроты паразитарного процесса, его длительности и длительности клинических проявлений бронхиальной астмы преобладает тот или другой класс иммуноглобулинов. Имеются клинические наблюдения, свидетельствующие об улучшении течения бронхиальной астмы или выздоровлении после ликвидации токсокарозной инвазии.
- Диагностика
Паразитологический диагноз устанавливается редко и только по наличию в тканях характерных гранулем и личинок и их идентификации при исследовании биопсийного и секционного материала. Это возможно при пункционной биопсии печени, легких, оперативном вмешательстве. Обычно диагноз токсокароза устанавливается на основании данных эпидемиологического анамнеза, клинической симптоматики и гематологических проявлений. Используют также иммунологические реакции, позволяющие выявлять антитела к антигенам токсокар. Обычно применяют ИФА с секреторно-экскреторным антигеном личинок токсокар второго возраста. В настоящее время в России выпускается коммерческий диагностикум. Диагностическим титром считают титр антител 1:400 и выше (в ИФА). Титр антител 1:400 свидетельствует об инвазированности, но не болезни. Титр антител 1:800 и выше свидетельствует о заболевании токсокарозом. Практика показывает, что прямая корреляция между уровнем антител и тяжестью клинических проявлений токсокароза существует не всегда. Не всегда имеется и корреляция между уровнем антител и гиперэозинофилии крови.
При постановке диагноза и определении показаний к специфической терапии следует учитывать, что токсокароз протекает циклически с рецидивами и ремиссиями, в связи с чем возможны значительные колебания клинических, гематологических и иммунологических показателей у одного и того же больного.
М. И. Алексеева и соавт. (1984) разработали алгоритм диагностики токсокароза, основанный на оценках в баллах значимости клинических симптомов и сопоставлении клинико-эпидемиологических и лабораторных показателей. Этот метод может быть перспективен при проведении массовых обследований населения.
Дифференциальный диагноз проводят с миграционной стадией других гельминтозов (аскаридоз, описторхоз), стронгилоидозом, эозинофильной гранулемой, лимфогранулематозом, эозинофильным васкулитом, метастазирующей аденомой поджелудочной железы, гипернефромой и другими заболеваниями, сопровождающимися повышенным содержанием эозинофилов в периферической крови. Следует иметь в виду, что у больных с системными лимфопролиферативными заболеваниями и серьезными нарушениями в системе иммунитета иммунологические реакции могут быть ложно положительными. В этих случаях необходим тщательный анализ клинической картины заболевания.
| При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими |
Глазной токсокароз. Патогенез этой формы токсокароза до конца не ясен. Существует гипотеза об избирательном поражении глаз у лиц с инвазией низкой интенсивности, при которой не развивается достаточно выраженная иммунная реакция организма из-за слабого антигенного воздействия небольшого числа поступивших в организм личинок токсокар.
Эта форма токсокароза чаще наблюдается у детей и подростков, хотя описаны случаи заболевания и у взрослых.
Для токсокароза характерно одностороннее поражение глаз. Патологический процесс развивается в сетчатке, поражается хрусталик, иногда параорбитальная клетчатка. В тканях глаза формируется воспалительная реакция гранулематозного характера. Патологический процесс часто принимают за ретинобластому, проводят энуклеацию глаза. При морфологическом исследовании обнаруживают эозинофильные гранулемы, иногда — личинки токсокар.
Клинически поражение глаз протекает как хронический эндофтальмит, хориоретинит, иридоциклит, кератит, папиллит. Глазной токсокароз — одна из частых причин потери зрения.
Диагностика глазного токсокароза сложна. Количество эозинофилов обычно нормальное или незначительно повышено. Специфические антитела не выявляются или выявляются в низких титрах.
- Лечение токсокароза
Разработано недостаточно. Применяют противонематодозные препараты — тиабендазол (минтезол), мебендазол (вермокс), медамин, диэтилкарбамазин. Эти препараты эффективны в отношении мигрирующих личинок и недостаточно эффективны в отношении тканевых форм, находящихся в гранулемах внутренних органов.
Минтезол (тиабендазол) назначают в дозах 25—50 мг/кг массы тела в сутки в три приема в течение 5—10 дней. Побочные явления возникают часто и проявляются тошнотой, головной болью, болями в животе, чувством отвращения к препарату (в настоящее время препарат в аптечную сеть России не поступает).
Вермокс (мебендазол) назначают по 200 —300 мг в сутки в течение 1—4 недель. Побочные реакции обычно не наблюдаются.
 |
Медамин применяют в дозе 10 мг/кг массы тела в сутки повторными циклами по 10 — 14 дней.
Диэтилкарбамазин назначают в дозах 2 — 6 мг/кг массы тела в сутки в течение 2 — 4 недель. (В настоящее время препарат в России не производится, не закупается за рубежом. — Прим. ред.)
Альбендазол назначают в дозе 10 мг/кг массы тела в сутки в два приема (утро — вечер) в течение 7 — 14 дней. В процессе лечения необходим контроль анализа крови (возможность развития агранулоцитоза) и уровня аминотрансфераз (гепатотоксическое действие препарата). Небольшое повышение уровня аминотрансфераз не является показанием к отмене препарата. В случае нарастающей гиперферментемии и угрозы развития токсического гепатита требуется отмена препарата.
Критерии эффективности лечения: улучшение общего состояния, постепенная регрессия клинических симптомов, снижение уровня эозинофилии и титров специфических антител. Следует отметить, что клинический эффект лечения опережает положительную динамику гематологических и иммунологических изменений. При рецидивах клинической симптоматики, стойкой эозинофилии и положительных иммунологических реакциях проводят повторные курсы лечения.
Прогноз для жизни благоприятный, однако при массивной инвазии и тяжелых полиорганных поражениях, особенно у лиц с нарушениями иммунитета, возможен летальный исход.
- Профилактика
Включает соблюдение личной гигиены, обучение детей санитарным навыкам.
Важным профилактическим мероприятием является своевременное обследование и дегельминтизация собак. Наиболее эффективно преимагинальное лечение щенков в возрасте 4 — 5 недель, а также беременных сук. Для лечения собак используют противонематодозные препараты. Необходимо ограничение численности безнадзорных собак, оборудование специальных площадок для выгула собак.
Следует улучшить санитарно-просветительскую работу среди населения, давать информацию о возможных источниках инвазии и путях ее передачи. Особого внимания требуют лица, по роду деятельности имеющие контакты с источниками инвазии (ветеринарные работники, собаководы, землекопы и другие).
ГЕМАНГИОПЕРИЦИТОМА (haemangiopericytoma; греч, haima кровь+ angeion сосуд + peri- возле, около + kytos сосуд, клетка + -oma) — сосудистая опухоль, образованная множеством капилляров, окруженных веретенообразными и круглыми клетками — перицитами.
Термин «Гемангиоперицитома» предложен Стаутом и Марри (А. P. Stout, М. R. Murray). Существует мнение, что Г. гистогенетически связана с хеморецепторным аппаратом, т. е. относится к нейроэктодермальным опухолям типа параганглиом (см.). Различают дифференцированную и недифференцированную Г.


Дифференцированная Г. встречается редко, может возникать в любом возрасте, часто у детей. Как правило, характеризуется медленным ростом, обычно достигает крупных размеров, сохраняя при этом четкие контуры и подвижность. Локализуется преимущественно в коже, мягких тканях туловища и конечностей, реже — в забрюшинном пространстве, средостении, сальнике, языке и внутренних органах (печень, кишечник, мозг и др.)* Макроскопическое строение — опухоль узловатой формы, на разрезе розовато-красного цвета, пористого строения, с обилием подходящих к ней сосудов. Микроскопически характеризуется большим количеством капилляров, выстланных эндотелием и окруженных округлыми, овальными или веретенообразными клетками с темными ядрами и светлой цитоплазмой (рис. 1). Клетки оплетены густой сетью аргирофильных волокон. Основным отличием Г. от капиллярной ангиомы является массивная пролиферация периваскулярных клеток, которые большинство исследователей относит к перицитам.
Дифференцированные Г., как правило, отграничены от мягких тканей слоем гиалинизированной ткани, к-рая, однако, на многих участках проращена опухолевыми клетками, что свидетельствует о местнодеструирующем росте. Дифференцированные Г. являются потенциально злокачественными опухолями, т. к. обладают высокой склонностью к рецидивам после недостаточно широкого хирургического иссечения. В редких случаях дифференцированные Г. могут давать отдаленные метастазы
Недифференцированная Г. (син.: гемангиоперицитарная саркома, перителиальная саркома, перителиома, периэндотелиома) является злокачественной опухолью. На ранней стадии развития недифференцированную Г. клинически и даже на основании морфол, исследования бывает трудно отличить от дифференцированной. Опухоль встречается редко, локализуется преимущественно в мягких тканях конечностей, реже в забрюшинной клетчатке, внутренних органах, костях. В большинстве случаев недифференцированные Г., локализующиеся в мягких тканях, сохраняют четкие контуры и только в поздних стадиях поражаются кожа, кости, сосудистонервные образования. При микроскопическом исследовании наблюдается полиморфизм клеток; среди клеток преобладают веретенообразные формы, наблюдается обилие фигур деления (рис. 2), прорастание клеток в просвет сосудов, инфильтрация окружающих тканей. Отличается агрессивным ростом, часто метастазирует (до 15% в регионарные лимфатические узлы и до 50% в легкие) и рецидивирует (в 40—50% случаев).
Лечение обеих форм хирургическое, прогноз неблагоприятный — после лечения ок. 50% больных живут до 5 лет и лишь 20% — до 10 лет.
Библиография: Клименков А. А. Отдаленные результаты лечения злокачественных опухолей мягких тканей, в кн.: Опухоли опорно-двигательного аппарата, под ред. H. Н. Трапезникова, в. 3, с. 43, М., 1971; Переслегин И. А. и др. Лучевая терапия гемангиоперицитом, Мед. радиол., т. 13, № 1, с. 15, 1968; Руководство по патологоанатомической диагностике опухолей человека, под ред. Н. А. Краевского и А. В. Смольянникова, с. 68, М., 1971.

Главное меню
Пиометра (гнойный эндометрит матки)
Пиометра
(гнойный эндометрит матки, гнойная матка)
С патолого-анатомической точки зрения изменения изменения в матке можно разделить на три основные группы:
пиометра (скапливание гноя в матке)
хронический эндометрит (гнойный эндометрит без скапливания секрета в матке)
железисто-кистозная гиперплазия эндометрия (кистозное вырождение маточных желёз).
Этиология и патогенез этих явлений в настоящее время изучены недостаточно. На основании эксперементальных исследований и клинических наблюдений можно сделать вывод о многообразии причин возникновения пиометры и эндометрита. Сравнение анамнеза и изменений в матке позволяет сделать вывод о том, что все клинические случаи можно разделить на две группы:
самки с нормальным половым циклом («типичная пиометра»);
самки с эндокринными нарушениями («хронический эндометрит или железисто-кистозная гиперплазия эндометрия»).
Типичная пиометра
Причины заболевания
Типичная пиометра предположительно вызывается первичными инфекционными процессами. Примерно в конце эструса или начале проэструса бактерии поднимаются через открытую шейку матки в матку и вызывают воспаление. Повышение уровня прогестерона вызывает закрытие матки и одновременно уменьшает устойчивость эндометрия к бактериальным инфекциям. Количество бактерий в матке увеличивается, и возникает эндометрит с гиперсекрецией маточных желёз. Постепенно матка наполняется гнойным секретом. Токсины из содержимого матки всасываются и вызывают токсемию. Острая фаза воспаления чаще всего протекает незаметно, фаза токсемии проявляется различным образом. При анализе содержимого матки животного, страдающего пиометрой, обнаруживаются преимущественно неспецифические бактерии (главным образом E. coli, а так же стафилококки, клебсиеллы, пастереллы и др.).
В некоторых случаях пиометра может развиваться как осложнение при прерывании беременности с помощью эстрогенов или после сдвигания течки с помощью гестагенов продлённого действия. После долгосрочного подавления половой функции с помощью гестагенов у самок чаще наблюдается мукометра (накопление в матке бактериологически стерильной слизи).
Симптомы
Во многих случаях опорожнение содержимого матки происходит раньше проявления других признаков заболевания (открытая форма пиометры). Такие пациенты попадают к врачу по поводу неожиданных выделений гноя из влагалища. Часто владельцы замечают, что животное в последнее время больше пьёт воды. В большинстве случаев общее состояние животного удовлетворительное. При осмотре заметно, что волоски шерсти в области влагалища склеены гнойным секретом, и если выделения пахнут то иногда их ошибочно принимают за понос. Эти симптомы хорошо видны на следующей фотографии:

В более редких случаях пиометра сопровождается тяжёлой токсемией и приводит к нарушениям общего состояния (температура, апатия, обезвоживание, слабость задних конечностей и т. п.). Но такое течение более характерно для закрытой формы пиометры. В некоторых случаях наблюдается увеличенный в объёме живот, повышение температуры тела.
Диагностика.
Для диагностики пиометры применяют вагиноскопическое обследование, осмотр слизистой влагалища, фронтальную рентгенографию, УЗИ матки, пальпацию и другие методы.
В результатах лабораторных исследований анализ содержания лейкоцитов показывает изменения, типичные для хронической инфекции, т. е. Лейкоцитоз средней или высокой степени с нейтрофилией и моноцитозом. Анализ содержания эритроцитов не показывает изменений. Биохимические показатели в большинстве случаев в норме. Иногда бывает повышенным уровень мочевины.
В отдельных случаях пиометра приводит к тяжелой токсемии с угнетением костного мозга, что может выражаться в анемии и лейкопении периферической крови.
Осложнением при пиометре является гнойный перитонит, который может быть вызван спонтанным разрывом матки, ятрогенным разрывом при пальпации или распространившимся через яйцевод заражением брюшной полости.
Лечение.
Медикаментозное лечение пиометры малоэффективно и особенно у кошек чаще всего не приводит к выздоровлению. Зачастую в результате лечения наступает временное улучшение состояние, а вскоре заболевание возобновляется. Поэтому если животное не представляет племенной ценности и не подлежит разведению то наиболее эффективным и правильным методом следует считать стерилизацию методом овариогистерэктомии.
Хронический эндометрит
Причины заболевания.
Причиной хронического эндометрита являются спонтанные или ятрогенно обусловленные расстройства механизмов гормонального регулирования. Вторичное влияние оказывает бактериальное заражение.
Симптомы.
Обращение к врачу происходит по поводу выделений из влагалища, которые появились после прошедшей течки и продолжаются в течении нескольких дней или недель. В большинстве случаев выделения менее обильные чем при пиометре. По качеству они могут варьировать от кровянисто-серозных или коричнево-водянистых до слизисто-гнойных, часто с вкраплениями сгустков крови.
У животных, страдающих хроническим эндометритом, часто ранее уже наблюдались нарушения полового цикла (затяжная или нечётко выраженная течка.
Общее самочувствие зависит от индивидуальных особенностей, не смотря на то, что изменения матки незначительны по сравнению с пиометрой.
Лечение.
Лечение аналогично железисто-кистозной гиперплазии эндометрия.
Железисто-кистозная гиперплазия эндометрия
Причина заболевания.
Как и при хроническом эндометрите, причиной этого заболевания является нарушение баланса половых стероидов, которое приводит к кистозному вырождению эндометрия с бактериальным заражением или без него.
Симптомы.
Клинические признаки при железисто-кистозной гиперплазии эндометрия такие же как и при хроническом эндометрите.
Лечение.
Как при железисто-кистознной гиперплазии так и хроническом эндометрите является удаление яичников и матки (овариогистерэктомия).
Фотоотчёт.
Фотография здоровой матки и яичников кошки, без патологий. Фото сделано в операционной ветклиники Котофей во время плановой стерилизации (овариогистерэктомии).

Фотографии маток животных с патологиями сделаны в операционной ветклиники Котофей.
На этой фотографии изображена воспаленная матка, удаленная во время операции. Этот орган не только болел и доставлял страдания животному, но и за счёт большого количества гноя являлся источником интоксикации организма. После операции животное прошло полную реабилитацию под наблюдением наших врачей, довольно быстро восстановилось и чувствует себя замечательно.

На следующей фотографии - изображение воспалённой матки кошки. Содержимое матки лабораторно не исследовалось, но по нашему мнению диагноз - гематометра. Объём операции включал в себя не только удаление воспалённой матки и яичников (овариогистерэктомия), но и удаление опухоли молочной железы вместе с молочным пакетом (мастэктомия), что бывает нередко в таких случаях. На фото слева виден удалённый молочный пакет. После операции животное успешно прошло реабилитацию.

На этой фотографии ещё один случай пиометры. Это фото гнойной матки у собаки, во время операции. Операция и послеоперационный период пройдены успешно, собака радует хозяев.

Врачи ветклиники Котофей.
При написании статьи использована информация из свободных источников, в том числе из учебника Hans G. Niemand, Peter F. Suter: ”Praktikum der Hundeklinik”.
Фотографии сделаны в операционной ветеринарной клиники Котофей.
Читайте также:

