Тимома у собаки лечение
Опубликовано: 09.05.2024
К первичным новообразованиям средостения относятся опухоли и кисты, развившиеся из тканей, эмбриогенетически присущих медиастинальному пространству, в том числе и тимусу.
Тимома - опухоль, развивающаяся из клеточных элементов тимуса.
Тимомы встречаются чаще у кошек, чем у собак [1]. Тимусная лимфома, как проявление первичной опухоли грудной полости и средостения, относится к лимфопролиферативным заболеваниям у кошек и собак с характерными признаками течения заболевания [4, 6].
Свободные выпоты в грудную полость с клиническими признаками проявления респираторной недостаточности, являются одной из форм проявления лимфопролиферативных заболеваний и в частности тимусных лимфом.
Основной проблемой остаётся диагностика и выбор методов лечения данной патологии.
Клинический случай
Обследование. На клинический прием поступило животное кошка в возрасте 4-х лет с жалобами владельцев на затрудненное дыхание в течение 60 суток. За последние 15 суток отмечено стойкое ухудшение состояния с прогрессированием дыхательной недостаточности.
Клиническое обследование показало двустороннее нарушение дыхания с одышкой смешанного типа, снижение дыхательных шумов лёгких при аускультации.
При проведении лабораторных исследований крови и мочи выраженных изменений не выявлено за исключением умеренного снижения уровня лимфоцитов.
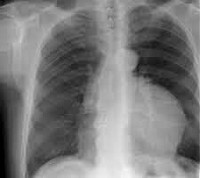
Дополнительные инструментальные методы диагностики (УЗИ, рентген) показали: неоднородное округлое новообразование в краниальной части средостения, наличие свободной жидкости в плевральной полости, дорсальное смещение трахеи в краниальной части, формирование коллапса каудальных долей легких (рис. 1).
При проведении торакоцентеза аспирировано 113 мл серозно-геморрагического транссудата.
При цитологическом исследовании аспирата были обнаружены клетки воспаления, многочисленные лимфоциты в различной стадии дифференцировки и наличие единичных бластных клеток.
Наличие бластных клеток в периферической крови не обнаружено.
Прицельная трансторакальная биопсия показала новообразование тимуса без явно выраженных атипичных свойств ткани лимфоцитарного типа (рис. 2).
Дополнительно животное было обследовано на предмет вирусных инфекций кошек: вирусный перитонит, вирусный лейкоз, иммунодефицит.
Лечение. На основании проведенного исследования был поставлен предварительный диагноз – тимусная лимфома. В качестве метода лечения на первом этапе предложена химиотерапия по схеме:
1. Циклофосфан - 300 мг/м 2 внутримышечно через три дня
2. Винкристин - 0,75 мг/м 2 внутривенно 1 раз в 15 дней
3. Преднизолон - 2 мг/кг перорально 1 раз в день
После двухнедельного курса химиотерапии и отсутствия ремиссии, которую определяли по наличию транссудата в грудной полости, была проведена коррекция схемы химиотерапии и добавлена L-аспарагиназа в дозе 400Е.
Через 15 дней была проведена оценка и отмечено отсутствие положительной динамики.
На основании клинического течения заболевания предложено и проведено оперативное вмешательство в объеме тимэктомии.
При ревизии грудной полости обнаружено: свободный серозно-геморрагический выпот, двусторонний ателектаз краниальных и срединных долей легких с проявлениями фиброзирующего плеврита, ригидность перикарда, слипчивый перикардит и опухоль тимуса, локализующаяся в естественном анатомическом положении (рис. 3).
Нами было проведено тотальное удаление новообразования (тимуса) с участком висцеральной плевры и жировой ткани краниального средостения.
С целью предотвращения синдрома диастолической дисфункции была проведена парциальная перикардэктомия (рис. 4а, б).
Проведение декортикации (удаление фиброзных шварт легкого) ателектазированных долей легких было затруднительно.
Операционная рана ушивалась стандартно по общим принятым методикам.
В постоперационном периоде, после снятия швов, проведен однократный курс химиотерапии.
Результат и обсуждение. Через 20 суток общее состояние животного удовлетворительно, определяется незначительное количество экссудата в плевральной полости на рентгенограмме, однако признаков респираторной недостаточности не отмечено (рис. 5 а).
Через 400 суток после оперативного вмешательства признаков наличия свободной жидкости в грудной полости не обнаружено, общее состояние животного удовлетворительно (рис. 5 б).
Вилочковая железа (тимус) является частью иммунной и эндокринной систем. Будучи центральным органом иммунной системы, она, прямо или опосредованно (через систему Т-лимфоцитов) обеспечивает развитие и функционирование иммунокомпетентной ткани, взаимодействует с органами нейроэндокринной системы [1]. Одним из методов лечения миастении гравис (нервно-мышечное заболевание, характеризующееся резко выраженной слабостью) является тимэктомия [3].
В ходе акцидентальной инволюции тимуса, проявляется формирование железистоподобных или солидных эпителиальных структур с повышенной митотической активностью [6].
В тимусе развивается целый ряд разнообразных по гистогенезу, прогнозу и клиническим проявлениям новообразований, что обусловлено особенностями его строением. Зачастую вовлекаются в патологический процесс окружающие тимус лимфатические узлы, что также относят к опухолям тимуса.
Морфологически по происхождению тимомы разделяются на лимфоцитарные и эпителиальные.
Тимомы достаточно редко способствуют образованию свободной жидкости в плевральную полость, как правило, механически воздействуют на трахею и вызывают респираторную недостаточность (рис. 6).
Опухоли средостения часто приводят к выпотам, но даже цитологическая интерпретация полученного выпота иногда не дает точного ответа, чтобы поставить окончательный диагноз. Возможность проведения прицельной трансторакальной биопсии позволило нам поставить диагноз и определить тактику лечения.
В клинической практике, как правило, проявление медиастинальных форм лимфосарком (подтверждённое наличием бластных клеток) не требуют хирургического вмешательства и лечатся консервативно с использованием химиотерапии [4, 5].
В нашем случае клиническое течение, распространённость процесса и морфологическое обоснование позволило провести оперативное вмешательство и получить хороший положительный результат хирургического лечения.
1. Джаррет У., Макки Л. Международная гистологическая классификация опухолей домашних животных. 1975. Том 50, 23-33.
2. Bonnard P., Dralez F. A propos d"un cas de thymome chez un chat. Point Vet 23:1089-1094, 1992
3. Drachman D.B. Myasthenia gravis; medical progress. N Engl J Med 1994. 330:1797.
4. Carpenter J.L., Holzworth J. Thymoma in 11 cats. J Am Vet Med Assoc 1982. 181:248-251.
5. Day M.J. Review of thymic pathology in 30 cats and 36 dogs. J Small Anim Pract 1997. 38:393-403.
6. Gores B.R., Berg J., Carpenter J.L., Aronsohn M.G. Surgical treatment of thymoma in cats: 12 cases (1987-1992). J Am Vet Med Assoc 1994 Jun 1; 204(11):1782-5.
Контактные телефоны:8 (495) 740-48-59


- Что такое тимома
- Частота возникновения патологии
- Причины развития
- Основные факторы риска
- Патогенные условия развития
- Симптоматика
- Стадии
- Формы
- Возможные осложнения
- Диагностические мероприятия
- Дифференциальные обследования
- Лечение
- Прогноз выживаемости
Тимома представляет собой достаточно редкую онкопатологию. Она предусматривает расположение новообразования в эпителиальной ткани тимуса, который является лимфоидно-железистым органом иммунной системы. Такое заболевание встречается нечасто. При этом его диагностику лучше проводить как можно быстрее для обеспечения эффективного проведения терапевтических мероприятий.
Код по МКБ-10
C37 Злокачественнаяопухоль вилочковой железы;
E32 Патологии вилочковой железы.
Частота возникновения патологии
Доля данной онкопатологии среди других типов онкологических болезней составляет менее 1 %. ВОЗ отмечает 0,15 случаев развития опухоли данного органа на 100 000 пациентов. В Китае такое заболевание выявляется чаще, так статистика составляет 6,3 случая на 100 000 пациентов.
На 90 % раковых патологий вилочковой железы приходится тимома переднего средостения. В 20 % случаев новообразование располагается в верхней части грудной клетки, под грудиной.
В не более 4 % случаев локализация опухоли предусматривает другие части, но онкопатология также относится к типу тимомы.
Причины развития онкопатологии
В медицине нет строгой классификации причин возникновения опухолей вилочковой железы. Однако зачастую она развивается у людей зрелого возраста, в одинаковом соотношении мужчин и женщин.
У молодых людей и детей такое заболевание бывает реже. При этом вилочковая железа наиболее активно функционирует именно в детском возрасте, так как при формировании иммунной системы организму необходим большой объем Т-лимфоцитов, вырабатываемых тимусом.
Наибольшего объема данный орган достигает в подростковом возрасте. Со взрослением постепенно он уменьшается, как и его активность.
Основные факторы риска образования онкопатологии
Нет материалов о наследственных, экологических аспектах, влияющих на возникновение рака данного типа. Согласно статистике, основными моментами становятся возраст, этническая принадлежность. Других факторов на данный момент в медицине не определено.
Риски возникновения патологии повышаются с возрастом. Зачастую тимома диагностируется у людей 40–50 лет, после 70 лет.
Патогенные условия развития онкологии
В медицинском сегменте нет достоверных материалов по рискам и патогенезу возникновения заболевания. Однако медики постоянно проводят работы в выяснении данных факторов, рассматривая различные аспекты, включая ультрафиолетовое, радиационное воздействие на организм человека.
Тимус вырабатывает T-лимфоциты, обеспечивает их транспортировку в периферические лимфоидные органы, а также стимулируется выработка антител B-лимфоцитами. Также железой осуществляется секреция гормонов, необходимых для регулирования дифференцировки лимфоцитов, процессы взаимодействия T-клеток в вилочковой железе и тканями других систем.
Тимома представляет собой разновидность эпителиальных новообразований. Она развивается достаточно медленно, предусматривает пролиферацию нормальных и схожих с нормальными клеток. Медики говорят о том, что видоизмененные раковые клетки при тимоме могут не предусматривать признаков злокачественных неоплазий, что является особенностью данной онкопатологии. Злокачественные явления при данном типе рака присутствуют только в 30–40 % клинических случаев, выражаются инвазией в другие участки, органы и ткани.
Существует определенная взаимосвязь неоплазий такого типа с аутоиммунными патологиями, например, полимиозит и дерматомиозит, диффузный токсический зоб, системная красная волчанка, аплазия эритроцитов (у половины пациентов), пернициозная или мегалобластная анемия (болезнь Аддисона), гипогаммаглобулинемия (у 10% пациентов), буллезные дерматозы (пузырчатка), синдром Шегрена, неспецифический язвенный колит, болезнь Кушинга, склеродермия, тиреоидит Хашимото, синдром Гуда (комбинированный В- и Т-клеточный имммунодефицит), неспецифический аортоартериит (синдром Такаясу), гиперпаратиреоидизм (избыток паратиреоидного гормона), болезнь Симмондса (пангипопитуитаризм).
Симптоматика возникновения патологии
Среди симптомов развития онкозаболевания можно отметить, что в 30–50 % случаев они отсутствуют. Зачастую новообразования определяются в ходе проведения рентгенографии грудной клетки, КТ, реализуемых для других задач.
При проявлении симптоматики первыми признаками становятся дискомфорт, ощущение давления в грудной клетке, загрудинных участках, дополняемое постоянным кашлем, отдышкой, болевым синдромом, а также признаками синдрома верхней полой вены. В этом случае необходимо обратиться к рентгенологу.
В случае миастении при онкопатологии возникают жалобы на спонтанную усталость, слабость, сложности в движении верхних конечностей, двоение в глазах, опущение век, затруднения при глотании. Такие аспекты также требуют незамедлительного обращения к специалисту, проведения диагностических мероприятий.
Стадии онкопатологии
В соответствии с ростом неоплазии и ее распространенности на другие системы, ткани, органы определяются стадии онкозаболевания:
I – новообразование находится на определенном участке, нет инвазии в жировые и другие ткани;
IIA – микроскопическая инвазия в жировую ткань;
IIB – макроскопическая инвазия неоплазии;
III – крупные инвазии в соседствующие органы;
IVA – распространение плевральных или перикардиальных метастазов;
IVB – распространение лимфо- или гематогенных метастазов в другие участки тела помимо грудных.
Формы онкопатологии
Такой тип новообразования сложно предугадать, определить поведение опухоли. Она может развиваться как обычная онкология, проникая в окружающие ткани, а также бессимптомно находиться в капсуле соединительной ткани. Они могут быть как доброкачественными, так и злокачественными. Последние предусматривают распространение опухоли в другие участки, агрессивное воздействие на организм и системы. В большинстве западные медики относят онкопатологию к злокачественным новообразованиям.
Специалисты Всемирной Организации Здравоохранения отмечают несколько типов развития онкозаболевания в соответствии с систематизацией материалов и гистологическим типом опухоли.
A – медуллярная. Предусматривает овальную форму, нахождение неоплазии в капсуле, состоит из раковых эпителиальных клеток вилочковой железы, без ядерной атипии.
AB – смешанная. Состоит из веретенообразных, округлых клеток эпителия, лимфоцитарных, эпителиальных клеток.
B1 – кортикальная. Предусматривает клетки, сходные с эпителиальными элементами тимуса, его коры, а также мозговым веществом железы.
B2 – корковая. Онкологические ткани предусматривают набухшие элементы из эпителиоретикулярных клеток, пузырчатых ядер, компонентов T-клеток, B-клеточных фолликулов, неоплазии могут образовываться возле сосудов железы.
B3 – эпителиальная, сквамоидная. Опухоль образована пластинчато-растущими, полигональными эпителиоцитами, лимфоцитами, относится к дифференцированной карциноме железы.
C – карцинома с гистологической атипией клеточных элементов.
При затрагивании онкологическими клетками сторонних органов, тканей патология является злокачественной.
Возможные осложнения при онкопатологии
Влияние злокачественного образования на другие органы регулирует осложнения и последствия развития онкопатологии. То есть в основном воздействие обусловлено ухудшением работы тех или иных органов, систем из-за развития тимомы.
Зачастую метастазирование происходит в лимфоузлы, плевру, перикард, диафрагму. Внегрудное проявление метастазов осуществляется в кости, мышцы скелета, перечень, брюшную стенку, однако такое явление возникает редко.
При развитии тимомы у пациента увеличивается риск возникновения онкопатологии, вторичных образований неоплазий в легких, лимфоузлах, щитовидке в четыре раза. То есть тимома может провоцировать рецидив других онкозаболеваний.
Также после полного удаления опухоли вилочковой железы может возникнуть рецидив. В соответствии со статистикой, после 10 лет тимома может вновь возникать в 10–30 % случаев. Однако на этот фактор оказывает влияние ряд аспектов, таких как сроки диагностики и резекции опухоли.
Диагностические мероприятия
Помимо осмотра у доктора и анамнеза исследования предусматривают ряд диагностических мероприятий. Оные необходимы для определения связанных патологий, паранеопластического синдрома, а также развития опухоли, распространения метастазов. К анализам при подозрении на рак вилочковой железы относятся общий, полный анализ крови, на антитела, уровень тиреоидных гормонов, паратгормона, АКГТ и прочее.
Для определения опухоли реализуется рентген грудной клетки, КТ, УЗИ. В некоторых случаях пациентам назначают также осуществление диагностики посредством торакальной МРТ, ПЭТ.
На снимке рентгенографии данная онкопатология представляется в виде волнистой или ровной овальной тени, представленной мягкими тканями. Она располагается немного в сторону середины грудины.
На КТ она диагностируется на участке средостения в виде крупного скопления неопластической ткани.
Посредством тонкоигольной аспирационной биопсии медики получают кусочек ткани новообразования, что позволяет выполнить исследования. Работы проводятся с применением КТ для точного забора материала. Такой метод не позволяет полноценно определить тип онкоткани. Осуществить данные манипуляции можно только после резекции и последующих гистологических мероприятий.
Дифференциальные обследования
Такого типа диагностика реализуется с учетом наличия патологий, связанных с тимусом, таких как тимомегалии, тимолипомы, лимфомы, гиперплазии, узловые формы загрудинного зоба, перикардиальная киста, туберкулез внутригрудных лимфоузлов.
Терапия тимомы
Зачастую терапия данного заболевания на первой стадии производится посредством резекции неоплазии, тимуса (тимэктомии). Это позволяет устранить риск возникновения метастазов и развития онкоклеток, их инвазии в сторонние ткани.
При второй стадии также реализуется удаление тимуса, последующее назначение лучевой терапии адъювантного типа. Это осуществляется для лечения онкообразований высокого уровня риска.
При стадиях развития патологии IIIA- IIIB, IVA методы терапии совмещаются. Проводятся операции по устранению метастазов в частях грудной клетки, также назначаются химиотерапевтические курсы до и после проведения хирургических мероприятий. Если устранение неоплазии не дало результата, докторами проводится перфузионная химио-, лучевая, таргетная терапия. Такие инструменты также применяются при инвазии опухоли в сторонние ткани, органы.
Зачастую при назначении химиотерапевтических курсов назначаются цитостатические медикаменты, противораковые препараты в соответствии со стадией онкопатологии. При неоперабельности онкологии также проводятся курсы химиотерапии для замедления развития опухоли.
При стадии IVB реализуется составление плана терапии в соответствии с особенностями организма и другими аспектами. Общих рекомендаций к лечению на данной стадии онкопатологии не разработано.
Прогнозирование
Такой тип онкологической неоплазии развивается достаточно медленно. Безусловно, благоприятный прогноз на устранение онкопатологии связан с ранней диагностикой опухоли, а также ранними стадиями ее развития.
Для третьей и четвертой стадии прогноз будет менее благополучным. Американская статистика American Cancer Society утверждает, что при устранении опухоли на первой стадии выживаемость в течение 5 лет составляет 100 %, на второй она предусматривает 90 %, на третьей предполагает 74 %, четвертой менее 25 %.
Отделы средостения и анатомия
Бранхиогенная, или жаберная, киста (branchiogenous cyst) – это врожденная киста, возникающая из остатков существовавших в эмбриональный период жаберных карманов. Редкая находка, описанная у кошек и собак. Располагается в краниальном средостении или в мягких тканях шеи, выглядит как тонкостенная киста, содержащая жидкость, может достигать значительных размеров. В средостении кисты развиваются из остатков жаберных карманов, из которых формируется тимус (в шее – из других жаберных карманов).
Эмфизема средостения (пневмомедиастинум) – это появление свободного газа в клетчатке средостения.
Газ может попасть в средостение несколькими путями:
- При перфорации грудного отдела трахеи (например, как осложнение при интубации) или при перфорации грудного отдела пищевода (например, инородным телом).
- При разрыве альвеол (например, при искусственной вентиляции легких) газ распространяется вдоль легочных сосудов и бронхов, расслаивая окружающую их ткань, и оказывается в средостении.
- Из расположенных краниальнее клетчаточных и межфасциальных пространств шеи, которые сообщаются с клетчаткой средостения. Нередко при перфорации глотки, гортани или шейного отдела трахеи (например, при ранениях шеи), газ попадает в окружающие трахею клетчаточные пространства, а по ним мигрирует в средостение. В месте перфорации трахеи может возникать эффект клапана, то есть газ при движении или вдохе легко проникает в окружающие трахею ткани, но не может вернуться из тканей в просвет трахеи, что приводит к накоплению большого количества газа в клетчаточных пространствах. Клетчаточное пространство средостения сообщается с лежащей за диафрагмой забрюшинной клетчаткой, газ может продолжить распространяться в нее с образованием пневморетроперитонеума (рис. 3). Кроме того, газ из средостения может мигрировать в полость перикарда.
- Бактериальный газ (например, при перфорации пищевода).
Гематома тимуса, гематома средостения
Гематома тимуса (кровотечение из тимуса) описано у молодых собак (в основном в возрасте до 1 года, несколько случаев – у пациентов в возрасте 2–3 лет) как кровотечение из ткани тимуса после травмы или без видимой травмы. После разрыва медиастинальной плевры кровь продолжает поступать в плевральные полости. Гематома развивается быстро, большинство описанных случаев диагностированы посмертно. В качестве одной из возможных причин рассматривают отравление антикоагулянтами.
Кроме того, у собак описаны случаи развития расслаивающей аневризмы аорты. В качестве частой причины развития данного заболевания у собак и диких животных указывают нематоду Spirocerca lupi, которая поражает стенку пищевода. Гематома средостения и гемоторакс могут развиться при разрыве аневризмы.
Реактивная лимфаденопатия
В средостении различают три группы лимфоузлов: стернальные (лежащие непосредственно над первыми сегментами грудины), лимфоузлы краниального средостения (расположены в краниальном средостении выше и каудальнее) и трахеобронхиальные (подковообразный лимфоузел, расположенный сразу за бифуркацией трахеи, и два бронхиальных – справа и слева).
Реактивная лимфаденопатия – это увеличение лимфоузлов, реагирующих на острое или хроническое, региональное или общее воспаление. Такие лимфоузлы на КТ при внутривенном контрастировании обычно слабо и однородно усиливаются.
Бактериальная или грибковая инфекция может поражать и сами лимфоузлы, в результате чего может сформироваться гранулема или абсцесс лимфоузла. Такие лимфоузлы на КТ при внутривенном контрастировании могут значительно усиливаться по периферии с интактными или неоднородно усиливающимися центральными массами.
Медиастинит
Воспаление средостения развивается при общем инфекционном процессе или при попадании микрофлоры непосредственно в средостение (например, при травме пищевода). На КТ можно выявить уплотнение (отек) жировой клетчатки средостения, появление свободной жидкости и бактериального газа в средостении и увеличение лимфоузлов.
Новообразования (тимома, лимфома, опухоли основания сердца)
Тимомы могут достигать гигантских размеров и смещать прилегающие органы (рис. 4). Распространяясь каудально, они чаще уходят в левую половину грудной клетки. Тимомы, как правило, имеют кистозный центр, содержащий жидкость, и тонкую, мягкотканную стенку, неровную по внутренней границе и неоднородно усиливающуюся при контрастировании. При тимомах может развиваться миастения гравис, которая иногда является причиной мегаэзофагуса. При УЗИ грудной клетки тимома может быть похожа на ткань печени, что в ряде случаев приводит к постановке ошибочного диагноза «диафрагмальная грыжа».
Лимфома в средостении может поражать тимус или лимфатические узлы (рис. 5). Лимфатические узлы при лимфоме увеличиваются во много раз, обычно сохраняя свою форму.
Реже встречаются другие опухоли: карцинома эктопической щитовидной железы, хемодектома, мезенхимальные и прочие опухоли.
Встречаются метастазы в лимфоузлах (например, метастазы опухолей молочной железы или печени в стернальные лимфоузлы, опухолей легких – в бронхиальные и трахеальные лимфоузлы).
КТ с контрастированием позволяет оценить васкуляризацию опухоли (что важно для планирования биопсии и хирургического вмешательства), выявить метастазы. Под контролем КТ можно провести тонкоигольную биопсию или core-биопсию.
Пищевод
Пищевод хорошо визуализируется на КТ при наличии газа в его просвете. При необходимости газ вводят искусственно (инсуффляция просвета пищевода).
Общие и локальные расширения просвета пищевода хорошо определяются на КТ. Возможны ошибки при диагностике стриктур и сужений на КТ, поэтому необходимо подтверждать такие находки эндоскопически (эзофагоскопия).
Эзофагит можно заподозрить на КТ при наличии локального утолщения стенки пищевода.
Опухоли пищевода определяются как массы, связанные со стенкой пищевода.
На КТ-ангиографии можно выявить варикоз пищеводных вен (при повышении давления в системе воротной вены).
Параэзофагеальная эмпиема (абсцесс, киста)
В каудальном средостении, вентральнее аорты, справа от пищевода, расположена серозная средостенная полость (в зарубежной литературе она может называться infracardiac bursa или Sussdorf's space). Эта полость может воспалиться со скоплением выпота, также из нее может образовываться асептическая киста (рис. 6). Возможными путями инфицирования считают контакт с воспаленными каудальной и добавочной долями правого легкого, миграцию инородных тел из легких (ости злаков), миграцию инородных тел из пищевода, гематогенный путь. У собак с этой патологией часто обнаруживают долевую пневмонию каудальной/добавочной долей правого легкого или медиастинит, но не выявляют патологических изменений в пищеводе.
Грудной лимфатический проток проходит через все средостение (по нему лимфа из каудальной половины тела попадает в переднюю полую вену) и обычно состоит из нескольких ветвей. Для его визуализации (как правило, это требуется при планировании операций по поводу хилоторакса) проводят лимфографию, то есть вводят рентгеноконтрастный препарат в просвет протока (местом введения может быть лимфатический сосуд брыжейки, паренхима семенника, толща мякиша тазовой конечности).
Европейская клиника
Тимома — это общее название для группы опухолей вилочковой железы (тимуса). Чаще всего они носят доброкачественный характер. На долю злокачественных опухолей приходится около 30% тимом. Выраженность клинической картины может быть самой разной, от бессимптомного течения до выраженной миастении и симптомов компрессии органов средостения.
Вилочковая железа частично находится в нижней части шеи, частично — в верхней части средостения. В органе выделяют два типа тканей — эпителиальную (железистую), которая отвечает за синтез тимических гормонов, и лимфоидную, которая представлена Т-лимфоцитами различной степени зрелости.
Таким образом, тимус является уникальным органом, который с одной стороны является железой внутренней секреции, а с другой — органом иммунной системы. В норме вилочковая железа проявляет активность в детском возрасте, играет роль депо Т-лимфоцитов и координирует работу эндокринной и иммунной систем. По мере взросления, тимус замещается жировой тканью. И у людей старше 50 лет сохраняется только 10% активных клеток.
- Причины возникновения тимомы
- Виды тимомы
- Стадии тимомы
- Диагностика тимомы
- Симптомы злокачественного новообразования вилочковой железы
- Лечение тимомы
- Последствия удаления тимомы
- Прогнозы выживаемости
Причины возникновения тимомы
Причины возникновения тимомы неизвестны. Предполагается, что в этом процессе могут принимать участие следующие факторы:
- Нарушения в эмбриональном периоде развития.
- Нарушение синтеза тимопоэтина.
- Нарушение иммунных механизмов.
- Инфекционные заболевания.
- Воздействие ионизирующего излучения.
- Травматические повреждения органов средостения.
- Некоторые аутоиммунные и эндокринные патологии: синдром Иценко-Кушинга, диффузный токсический зоб, миастения и др.
Виды тимомы
Единой классификации тимом на сегодняшний день нет, ввиду большого разнообразия опухолей, развивающихся в вилочковой железе. В 1999 году ВОЗ предложила морфологическую классификацию, в основе которой лежит соотношение лимфоцитарных и эпителиальных клеток. По этой классификации выделяют 6 видов опухоли:
- Тимома типа А — опухолевая ткань представлена дифференцированными клетками без признаков атипии, практически всегда отграничена от окружающих тканей капсулой. Клетки веретенообразные или овальные. Это благоприятный, доброкачественный вариант тимомы, 15-летняя выживаемость при которой составляет 100%.
- Тимома типа АВ морфологически схожа с типом А, но имеются единичные очаги патологических лимфоцитов.
- Тимома типа В — в опухолевой ткани преобладают дендритные и эпителиоидные клетки. Тип В будет разделяться в зависимости от соотношения эпителиальных и лимфоидных клеток, а также от выраженности их атипизма.
- Тимома типа В1 (преимущественно кортикальный тип). По структуре напоминает кортикальный слой вилочковой железы, очаговыми вкраплениями медуллярных клеток.
- Тимома типа В2 (кортикальный тип). В ткани опухоли имеются эпителиальные клетки с признаками атипии и везикулами в ядре.
- Тимома типа В 3 (эпителиальный тип). Опухоль представлена атипичными эпителиальными клетками. Некоторые авторы расценивают ее как высокодифференцированный рак вилочковой железы.
- Тимома типа С — рак тимуса. Представлен разнообразными гистологическими типами рака — светлоклеточный, плоскоклеточный, веретеноклеточный и др. Склонен к агрессивному течению, прорастает в соседние органы, дает метастазы в печень, кости и лимфатические узлы.
Тимомы типа А, АВ и В1 относят к доброкачественным новообразованиям тимуса, тип В2 и В3 — это злокачественные тимомы с относительно благоприятным течением, когда при своевременном обращении возможно полное излечение и 20-летняя продолжительность жизни составляет 40-60%. Тип С называют карциномой тимуса 2-го типа. Как мы уже говорили, это агрессивная опухоль, склонная к быстрому росту и метастазированию.

Стадии тимомы
Для характеристики распространения тимомы применяется классификация Masaoka-Koga. В ее основу положена оценка вовлеченности тканей и органов средостения, а также наличие лимфогенных и гематогенных метастазов.
- 1-2 стадия тимомы — опухоль прорастает за пределы своей капсулы, затрагивает плевру и клетчатку средостения.
- 3 стадия тимомы — опухоль прорастает в перикард, затрагивает легкое или магистральные сосуды, находящиеся в средостении.
- 4А стадия — имеется опухолевая диссеминация по плевре или перикарду.
- 4В стадия — имеются лимфогенные или гематогенные метастазы.
Диагностика тимомы
Заподозрить наличие опухоли можно по характерным клиническим симптомам, после чего пациент направляется на диагностические исследования. Рентген грудной клетки является неспецифическим методом диагностики и позволяет только увидеть расширение тени средостения.
Компьютерная томография с контрастированием — более информативный метод. Он позволяет получить информацию о наличии новообразования, определить его злокачественность, и даже дифференцировать его природу — отличить тимому от лимфомы и др. МРТ не является рутинным методом диагностики тимом, но может использоваться по показаниям, например, при наличии у пациента аллергии на йодсодержащий контраст, применяемый при КТ.
Окончательный диагноз выставляется после морфологического изучения опухолевой ткани. Как правило, ее получают после радикальной операции. Если это невозможно, рассматривают вариант проведения биопсии. Для этого может использоваться толстоигольная или хирургическая биопсия, которая проводится во время лапароскопических операций. Морфологическая верификация необходима для подбора оптимального метода лечения.
Симптомы злокачественного новообразования вилочковой железы
Какое-то время злокачественная опухоль вилочковой железы может протекать бессимптомно. На данном этапе обнаруживается случайно, при проведении обзорной рентгенографии грудной клетки или флюорографии. По мере развития процесса, будет возникать и нарастать неспецифическая симптоматика, которая связана с локальным воздействием опухоли на органы груди и средостения:
- Кашель.
- Боль в области груди.
- Одышка. Она может быть результатом компрессии органов дыхания, или миастенического синдрома, при котором наблюдается слабость мышц из-за нарушений нейромышечных связей.
- Синдром верхней полой вены — нарушение венозного оттока от головы и плечевого пояса из-за компрессии верхней полой вены. Проявляется цианозом кожи и отечностью верхней половины тела, а также расширением вен.
- Нарушение иммунной системы. Тимус является органом, в котором проходят определенные стадии своего развития Т-лимфоциты. При опухолевых процессах происходит нарушение их дифференцировки, что чревато развитием иммунодефицитов или аутоиммунных заболеваний. Самым частым из них является миастения — нарушение нервно-мышечной проводимости, развивающейся из-за воздействия антител на рецепторы ацетилхолина. При этом возникает мышечная слабость и патологическая утомляемость. Миастения характерна для типа лимфом В1-В3 и С.
- Аплазия костного мозга.
- Повышение температуры тела и ночные поты. Эти симптомы затрудняют дифдиагностику, поскольку более характерны для лимфом.
- На поздних стадиях присоединяется канцерогенная интоксикация: общая слабость, потеря аппетита, снижение массы тела.
Лечение тимомы
Лечение доброкачественной тимомы и злокачественной тимомы 1-2 стадии подразумевает хирургическое удаление вилочковой железы. Операция может быть выполнена в следующем объеме:
- Тотальное удаление тимуса вместе с окружающей жировой клетчаткой и лимфатическими узлами.
- Расширенное удаление тимуса — помимо вышеперечисленного объема, проводится еще резекция плевры и полное удаление переднестернальной жировой клетчатки.
При местно-распространенных злокачественных тимомах есть вероятность невозможности проведения радикального вмешательства, поэтому лечение рекомендуют начинать с адъювантной терапии. Обычно используется индукционная химиолучевая терапия с препаратами: циклофосфамидом, доксорубицином и цисплатином.
Объем операции будет зависеть от того, какие органы вовлечены в процесс. Может потребоваться резекция легочной ткани, перикарда, протезирование крупных кровеносных сосудов. Такие операции проводятся только на базе специализированных центров, в которых созданы условия для обширных вмешательств на органах грудной клетки. Для уменьшения развития рецидивов проводят послеоперационную лучевую терапию. При неоперабельных опухолях, ключевым методом лечения является химиолучевая терапия.
Последствия удаления тимомы
У пациентов, перенесших удаление вилочковой железы, есть риск развития миастенического криза — грозного состояния, при котором нарушается нервно-мышечная проводимость, из-за чего развивается сильная слабость мышц, сопровождающаяся параличами, нарушением дыхания и глотания. В тяжелых случаях возможен летальный исход. Для лечения пациентов применяется искусственная вентиляция легких и антихолинэстеразные препараты длительными курсами.
Прогнозы выживаемости
Прогнозы зависят от гистологического вида тимомы. При доброкачественных тимомах результаты лечения благоприятны, например, при типе В1 20-летняя выживаемость составляет около 90%. У пациентов со злокачественными вариантами тимомы прогноз будет зависеть от стадии распространения опухоли. При 2 стадии 5-летний рубеж переживают около 90% больных, при 3 стадии до 70% и при неоперабельных опухолях только 10%.
Тимома – гетерогенная группа новообразований, различных по гистогенезу и степени зрелости, берущих начало из эпителиальной ткани вилочковой железы. Варианты клинического течения тимомы могут быть различны: от бессимптомного до выраженного (компрессионный, болевой, миастенический, интоксикационный синдром). Топографо-анатомический и этиологический диагноз устанавливается с помощью лучевых методов (рентгенография, КТ средостения), трансторакальной пункции, медиастиноскопии, исследования биоптата. Лечение хирургическое: удаление тимомы вместе с вилочковой железой и жировой клетчаткой переднего средостения, дополненное по показаниям химиолучевой терапией.
- Строение и функции вилочковой железы
- Классификация тимом
- Симптомы тимомы
- Диагностика
- Лечение тимом
- Цены на лечение
Общие сведения
Тимома – органоспецифическая опухоль средостения, происходящая из клеточных элементов мозгового и коркового вещества тимуса. Термин «тимома» был введен в употребление в 1900 году исследователями Grandhomme и Scminke для обозначения различных опухолей вилочковой железы. Тимомы составляют 10-20% всех новообразований медиастинального пространства. В 65-70% случаев тимомы имеют доброкачественное течение; инвазивный рост с прорастанием плевры и перикарда отмечается у 30% пациентов, отдаленное метастазирование – у 5%. Несколько чаще тимомы развиваются у женщин, болеют преимущественно лица 40-60 лет. На детский возраст приходится менее 8% опухолей тимуса.
Причины формирования опухолей вилочковой железы неизвестны. Предполагается, что тимомы могут иметь эмбриональное происхождение, быть связаны с нарушением синтеза тимопоэтина или иммунного гомеостаза. Факторами, провоцирующими рост и развитие опухоли, могут служить инфекционные заболевания, радиационное воздействие, травмы средостения. Замечено, что тимомы часто сочетаются с различными эндокринными и аутоиммунными синдромами (миастенией, дерматомиозитом, СКВ, диффузным токсическим зобом, синдромом Иценко-Кушинга и др.).

Строение и функции вилочковой железы
Вилочковая железа, или тимус располагается в нижней части шеи и переднем отделе верхнего средостения. Орган образован двумя асимметричными долями – правой и левой. В свою очередь, каждая доля представлена множеством долек, состоящих из коркового и мозгового вещества и заключенных в соединительнотканную строму. В вилочковой железе различают два типа ткани – эпителиальную и лимфоидную. Эпителиальные клетки секретируют тимические гормоны (тимулин, a-, b-тимозины, тимопоэтины и пр.), лимфоидная ткань состоит из Т-лимфоцитов различной степени зрелости и функциональной активности.
Таким образом, вилочковая железа одновременно является железой внутренней секреции и органом иммунитета, обеспечивающим взаимодействие эндокринной и иммунной систем. После 20 лет тимус подвергается возрастной инволюции; после 50 лет паренхима тимуса на 90% замещается жировой и соединительной тканью, сохраняясь в виде отдельных островков, лежащих в клетчатке средостения.
Классификация тимом
В онкологии различают три типа тимом: доброкачественную, злокачественную тимому 1-го типа (с признаками атипии, но относительно доброкачественным течением) и злокачественную тимому 2-го типа (с инвазивным ростом).
- Доброкачественная тимома (50-70% опухолей тимуса) макроскопически имеет вид одиночного инкапсулированного узла, диаметром не более 5 см. С учетом гистогенеза внутри этой группы выделяют медуллярную (тип А), смешанную (тип АВ) и преимущественно кортикальную (тип В1) тимому.
- Тимома типа А (медуллярная) составляет 4–7% доброкачественных опухолей вилочковой железы. В зависимости от строения может быть солидной и веретеноклеточной-крупноклеточной, практически всегда имеет капсулу. Прогноз благоприятный, 15-летняя выживаемость составляет 100%.
- Тимома типа АВ (кортико-медуллярная) встречается у 28–34% пациентов. Сочетает в себе очаги кортикальной и медуллярной дифференцировки. Имеет удовлетворительный прогноз; 15-летняя выживаемость – более 90%.
- Тимома типа В1 (преимущественно кортикальная) встречается в 9–20% случаев. Часто имеет выраженную лимфоцитарную инфильтрацию. Более чем у половины пациентов сопровождается миастеническим синдромом. Прогноз удовлетворительный; 20-летняя выживаемость - более 90%.
- Злокачественная тимома 1-го типа (20-25% случаев) представляет собой одиночный или множественные дольчатые узлы без четкой капсулы. Размер опухоли чаще не превышает 4-5 см, однако иногда встречаются новообразования больших размеров. Отличается инвазивным ростом в пределах железы. В гистологическом отношении представлена кортикальной тимомой (тип В2) и высокодифференцированной карциномой.
- Тимома типа В2 (кортикальная) составляет около 20–36% тимом. Гистологические разновидности вариабельны: темноклеточная, светлоклеточная, водянисто-клеточная и др. В большинстве случаев протекает с миастенией. Прогностически менее благоприятна: 20 лет живут менее 60% больных.
- Тимома типа В3 (эпителиальная) развивается у 10–14% пациентов. Часто обладает гормональной активностью. Прогноз хуже, чем при кортикальной разновидности; 20-летняя выживаемость менее 40%.
- Злокачественная тимома 2-го типа (рак тимуса, тимома типа C) составляет до 5% всех наблюдений. Отличается выраженным инвазивным ростом, высокой метастатической активностью (дает метастазы в плевру, легкие, перикард, печень, кости, надпочечники). Выделяют 6 гистологических типов рака тимуса: плоскоклеточный, веретеноклеточный, светлоклеточный, лимфоэпителиальный, недифференцированный, мукоэпидермоидный.
В зависимости от удельного веса лимфоидного компонента в тимоме дифференцируют лимфоидные (более 2/3 всех клеток опухоли представлено Т-лимфоцитами), лимфоэпителиальные (Т-лимфоциты составляют от 2/3 до 1/3 клеток) и эпителиальные тимомы (Т-лимфоцитами представлено менее 1/3 всех клеток).
Основываясь на степени инвазивного роста, выделяют 4 стадии тимомы:
- I стадия - инкапсулированная тимома без прорастания жировой клетчатки средостения
- II стадия – прорастание элементов опухоли в медиастинальную клетчатку
- III стадия - инвазия плевры, легкого, перикарда, крупных сосудов
- IV стадия – наличие имплантационных, гематогенных или лимфогенных метастазов.
Симптомы тимомы
Клинические проявления и течение тимомы зависит от ее типа, гормональной активности, размеров. Более чем в половине случаев опухоль развивается латентно и обнаруживается во время профилактического рентгенологического исследования.
Инвазивные тимомы вызывают компрессионный медиастинальный синдром, который сопровождается болями за грудиной, сухим кашлем, одышкой. Сдавление трахеи и крупных бронхов проявляется стридором, цианозом, дыхательной недостаточностью. При синдроме компрессии верхней полой вены возникает одутловатость лица, синюшность верхней половины туловища, набухание шейных вен. Давление растущей опухоли на нервные узлы обусловливает развитие синдрома Горнера, осиплость голоса, элевацию купола диафрагмы. Сдавливание пищевода сопровождается расстройством глотания – дисфагией.
По различным данным, от 10 до 40% тимом сочетаются с миастеническим синдромом. Больные отмечают снижение мышечной силы, быструю утомляемость, слабость мимических мышц, двоение в глазах, поперхивание, нарушения голоса. В тяжелых случаях может развиться миастенический криз, требующий перехода к ИВЛ и зондовому питанию.
В поздних стадиях злокачественной тимомы появляются признаки раковой интоксикации: лихорадка, анорексия, снижение массы тела. Нередко тимоме сопутствуют различные гематологические и иммунодефицитные синдромы: апластическая анемия, тромбоцитопеническая пурпура, гипогаммаглобулинемия.
Диагностика
Диагностика тимомы проводится торакальными хирургами с привлечением онкологов, рентгенологов, эндокринологов, неврологов. При клиническом осмотре может выявляться расширение вен грудной клетки, выбухание грудины в проекции опухоли; увеличение шейных, надключичных, подключичных лимфоузлов; признаки компрессионного синдрома и миастении. Физикальное исследование обнаруживает расширение границ средостения, тахикардию, свистящие хрипы.
На рентгенограмме грудной клетки тимома имеет вид объемного образования неправильной формы, расположенного в переднем средостении. КТ грудной клетки значительно расширяет объем информации, полученный при первичной рентгендиагностике и в ряде случаев позволяет поставить морфологический диагноз. Уточнение локализации и взаимоотношения новообразования с соседними органами при КТ средостения позволяет в дальнейшем выполнить трансторакальную пункцию опухоли средостения, что чрезвычайно важно для гистологического подтверждения диагноза и верификации гистологического типа тимомы.
Для визуального исследования средостения и выполнения прямой биопсии проводится диагностическая медиастиноскопия, парастернальная торакотомия или торакоскопия. Диагноз миастении уточняется с помощью электромиографии с введением антихолинэстеразных препаратов. Дифференциально-диагностические мероприятия позволяют исключить другие объемные процессы в средостении: загрудинный зоб, дермоидные кисты и тератомы средостения.
Лечение тимом
Лечение опухолей вилочковой железы проводится в отделениях торакальной хирургии и онкологии. Хирургический метод является основным в лечении тимомы, поскольку только тимэктомия обеспечивает удовлетворительные отдаленные результаты. При доброкачественных тимомах оперативное вмешательство заключается в удалении опухоли вместе с вилочковой железой (тимомтимэктомия), жировой клетчаткой и лимфатическими узлами средостения. Такой объем резекции диктуется высоким риском рецидива опухоли и миастении. Операция выполняется из срединного стернотомического доступа.
При злокачественных новообразованиях тимуса операция может дополняться резекцией легкого, перикарда, магистральных сосудов, диафрагмального нерва. Послеоперационная лучевая терапия показана при II и III стадиях тимомы. Кроме этого, облучение является ведущим методом лечения неоперабельных злокачественных тимом IV стадии. В настоящее время большее значение в лечении инвазивных тимом получает трехэтапное лечение, включающее неоадъювантную химиотерапию, резекцию опухоли и лучевую терапию.
В послеоперационном периоде у больных, перенесших тимэктомию, может случиться миастенический криз, который требует проведения интенсивной терапии, трахеостомии, ИВЛ, длительного назначения антихолинэстеразных препаратов.
Отдаленные результаты лечения доброкачественных тимом хорошие. После удаления опухоли исчезают или значительно уменьшаются симптомы миастении. У больных злокачественной тимомой, прооперированных на ранних стадиях, 5-летняя выживаемость достигает 90%, на III стадии – 60-70%. Неоперабельные формы онкологического заболевания имеют плохой прогноз с летальностью 90% в течение ближайших 5 лет.
Читайте также:

